
КАТЕГОРИИ:
АстрономияБиологияГеографияДругие языкиДругоеИнформатикаИсторияКультураЛитератураЛогикаМатематикаМедицинаМеханикаОбразованиеОхрана трудаПедагогикаПолитикаПравоПсихологияРиторикаСоциологияСпортСтроительствоТехнологияФизикаФилософияФинансыХимияЧерчениеЭкологияЭкономикаЭлектроника
Общие представления об адсорбции.
В общем случае явления, связанные с самопроизвольным перераспределением веществ между различными частями гетерогенной системы, называют сорбцией. Сорбция (от лат sorbio-сгущать)- это изменение (как правило, увеличение) концентрации компонента либо у поверхности раздела фаз (адсорбция), либо в объеме одной из фаз (абсорбция). Сорбция может трактоваться как образование раствора. Поверхностная сорбция одно из важнейших сорбционных явлений. Наибольшее практическое значение имеет адсорбция на поверхности твердых тел. Адсорбция может происходить на поверхностях раздела:
твердое тело - газ,
твердое тело - раствор,
раствор - газ.
Твердое тело, у поверхности которого происходит адсорбция, называется адсорбентом, адсорбированное вещество - адсорбат, а адсорбирующий компонент жидкого раствора называется адсорбтив.
Физическая и химическая адсорбция. Адсорбцию принято делить на физическую и химическую (хемосорбцию). Резкой границы между ними не существует, хотя в предельных случаях они различаются легко. Физическая адсорбция обусловлена межмолекулярными (ван-дер-ваальсовыми) силами и не происходит химического взаимодействия между адсорбатом и адсорбентом. и молекулы адсорбата на поверхности не теряют своей индивидуальности. Попадая на поверхность адсорбента, молекула адсорбата удерживается силовым полем поверхности в течение некоторого времени, а затем десорбируется. В начальный период скорость адсорбции намного превышает скорость десорбции, но постепенно эта разница уменьшается, скорости выравниваются, то есть наступает адсорбционное равновесие, и молекулы адсорбата образуют на поверхности адсорбента адсорбционный слой. При этом свободная энергия поверхности уменьшается.
Химическая адсорбция называется также активированной адсорбцией, так как она подобно химическим реакциям характеризуется определенной энергией активации, то есть некоторым избытком энергии по сравнению со средней энергией всех молекул, необходимым для осуществления химической реакции.
Энергия активации вычисляется из зависимости постоянной скорости реакции k и температуры по формуле Аррениуса:
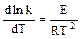
где E - энергия активации, определяющих число эффективных столкновений, равное общему числу столкновений, умноженному на  и поэтому, показывающий резкий рост реагирующих (активных) молекул с повышением температуры.
и поэтому, показывающий резкий рост реагирующих (активных) молекул с повышением температуры.
Таким образом, наиболее существенное различие между двумя типами адсорбции заключается в природе сил, вызывающих ее. Силы, действующие между адсорбентом и адсорбатом, аналогичны силам, проявляющимся в процессах кондeнсации; при хемосорбции силам, действующим при химических реакциях. При достаточно низких температурах ван-дер-вальсова адсорбция наблюдается для любых веществ, тогда как хемосорбция не для всех веществ.
Равновесие при физической адсорбции устанавливается быстро и обратимо. При этом возможны следующие варианты физической адсорбции:
1. Адсорбция неполярного адсорбата на неполярном адсорбенте – это универсальное дисперсионное взаимодействие, существующее в любых системах, где есть электроны. Оно, в частности, не зависит от температуры, и сила взаимодействия между двумя молекулами не зависит от присутствия других молекул. Кроме того, дисперсионные силы аддитивны, поэтому, например, в пористых средах их вклад в адсорбцию существенно возрастает.
2. Адсорбция неполярного адсорбата на полярном адсорбенте (например, ионные кристаллы) – здесь добавляются электрические силы притяжения молекул адсорбата, которые индуцируются в диполи в электрическом поле адсорбента – т.н. индукционное притяжение. Аналогично проявляется адсорбция и при взаимодействии полярного адсорбата с неполярным адсорбентом.
3. Адсорбция полярного адсорбата на полярном адсорбенте сопровождается ориентационным кулоновским взаимодействием диполей адсорбата с электрическим полем адсорбента. Причем и индукционные и ориентационные силы не являются аддитивными: присутствие других молекул в поле взаимодействия двух молекулярных диполей ослабляет это взаимодействие, что имеет место в пористых средах с развитой поверхностью адсорбента.
В целом энергия взаимодействия складывается из трех указанных видов взаимодействия. Наибольший вклад (для неполярных молекул - основной) вносит дисперсионное взаимодействие.
Дата добавления: 2014-10-31; просмотров: 158; Мы поможем в написании вашей работы!; Нарушение авторских прав |