
КАТЕГОРИИ:
АстрономияБиологияГеографияДругие языкиДругоеИнформатикаИсторияКультураЛитератураЛогикаМатематикаМедицинаМеханикаОбразованиеОхрана трудаПедагогикаПолитикаПравоПсихологияРиторикаСоциологияСпортСтроительствоТехнологияФизикаФилософияФинансыХимияЧерчениеЭкологияЭкономикаЭлектроника
Электрофилъные реакции
К электрофильным относятся все химические превращения HD по центральному атому серы, имеющему две пары свободных электронов. Электрофильные реакции, в особенности окисление и хлорирование, используются главным образом для дегазации HD. Некоторые реакции HD как диалкилсульфида могут быть положены в основу его индикации.
Кислород воздуха в обычных условиях не взаимодействует с HD, хотя при высокой температуре ОВ горит на воздухе. Любые окислители (перекись водорода, влажный хлор, азотная кислота, перманганаты, хромовая кислота, гипохлориты щелочных и щелочноземельных металлов) превращают HD в β,β'-дихлордиэтилсульфоксид и β,β'-дихлордиэтилсульфон согласно схеме:
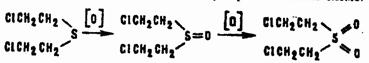
Сульфоксид и сульфон ядовиты, но, будучи твердыми веществами (температура плавления соответственно 110 и 56 °С), не обладают способностью к кожной резорбции.
В избытке окислителей процесс не заканчивается на образовании сульфоксида и сульфона. Последний превращается в β-хлорэтансульфокислоту, которая в жестких условиях претерпевает полную деструкцию:
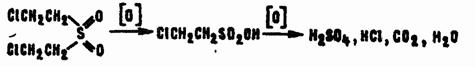
Из всех продуктов окисления наиболее опасен β,β'-дихлордиэтилсульфон, токсичность которого соизмерима с токсичностью HD и объясняется дегидрохлорированием в щелочной среде:

Дивинилсульфон способен присоединяться по кратной углерод-углеродной связи к нуклеофильным реагентам, в том числе к окси- и аминогруппам структурных белков клеточных мембран. Следовательно, для дегазации HD необходимо брать сильные окислители в большом избытке.
Для разложения HD на местности и поверхностях, устойчивых к действию окислителей, пригодны гипохлориты щелочных и щелочноземельных металлов. В водных растворах и суспензиях они окисляют и хлорируют HD, при этом направление процесса определяется значением рН среды. В щелочной среде преимущественно имеег место окисление, в нейтральной и кислой средах—хлорирование.
В сильно разбавленных щелочных растворах гипохлоритов из HD образуется главным образом β,β'-дихлордиэтилсульфоксид. Однако достаточно небольшого избытка гипохлорита, чтобы окислить сульфоксид в сульфон. В большом избытке гипохлорита HD полностью разлагается:
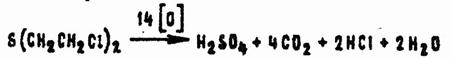
Применительно к основному гипохлориту кальция данная схема может быть представлена уравнением:
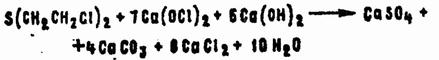
Сухие хлорная известь и ДТС ГК также окисляют и хлорируют HD. Реакции сопровождаются сильным разогреванием смеси, а нередко воспламенением и горением HD. Среди продуктов обнаруживают хлористый водород, углекислый газ, серный ангидрид, хлориды серы, дихлорэтан, хлороформ, хлораль.
Для дегазации HD пригодны нерастворимые в воде, но растворяющиеся в органических веществах (например, в дихлорэтане) полихлорсодержащие N-хлорамиды арилсульфокислот или реагирующий с водой, но устойчивый в неводных средах хлористый сульфурил. Первой стадией реакции всех хлорирующих агентов в любых средах является присоединение катиона хлора к нуклеофильному атому серы HD с образованием кристаллического хлористого бис-(2-хлорэтил)хлорсульфония:

Реакция происходит уже при температуре 0°С и сопровождается выделением тепла.
Последующие стадии процесса различаются в зависимости от среды. В водных растворах вследствие гидролиза продукта реакции (3.7) и стабилизации катиона сульфония образуется β,β'-дихлордиэтилсульфоксид:
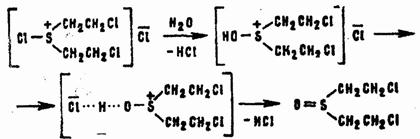
В неводных средах хлористый бис-(2-хлорэтил)хлорсульфоний стабилизируется по схеме:
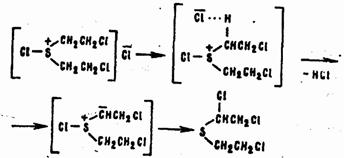
В избытке хлорирующего средства процесс на этом не останавливается. Образуются жидкие α,α,β,β'-тетрахлордиэтилсульфид, α,α,α,β,β'-пентахлордиэтилсульфид и другие полихлорированные сульфиды. Все они склонны к элиминированию хлористого водорода, причем склонность эта тем сильнее, чем больше атомов хлора содержит молекула сульфида. Направления дегидрохлорирования ясны из схем реакций:
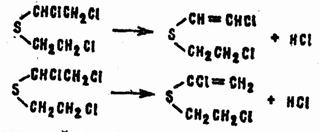
Процесс, описанный на примере хлора, применительно к хлористому сульфурилу в дихлорэтане может быть выражен уравнением:

Аналогично реагируют в неводных средах полихлорсодержащие N-хлорамиды арилсульфокислот, например:

Водорастворимые соли N-монохлорамидов арилсульфокислот реагируют с HD иначе:
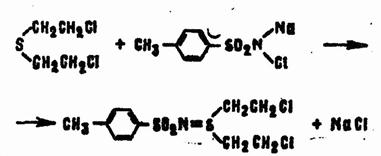
Реакция HD с монохлораминами в водном или водно-спиртовом растворе происходит быстро даже при низкой температуре, поэтому может использоваться для дегазации ОВ, в частности на кожных покровах.
Подобно другим сульфидам, HD способен присоединять к себе соли которых тяжелых металлов, например:
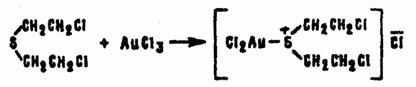
Многие из образующихся сульфониевых соединений имеют специфическую окраску, очень мало растворимы или практически нерастворимы в воде, поэтому реакции HD с хлоридами меди, цинка, титана, ртути, платины, золота находят применение для обнаружения и определения но.
Дата добавления: 2015-04-15; просмотров: 134; Мы поможем в написании вашей работы!; Нарушение авторских прав |