
КАТЕГОРИИ:
АстрономияБиологияГеографияДругие языкиДругоеИнформатикаИсторияКультураЛитератураЛогикаМатематикаМедицинаМеханикаОбразованиеОхрана трудаПедагогикаПолитикаПравоПсихологияРиторикаСоциологияСпортСтроительствоТехнологияФизикаФилософияФинансыХимияЧерчениеЭкологияЭкономикаЭлектроника
Химические свойства. В отсутствие влаги дихлорангидрид угольной кислоты стабилен
В отсутствие влаги дихлорангидрид угольной кислоты стабилен. Практически все его химические превращения основаны на нуклеофильном замещении атомов хлора на другие группы.
Газообразный CG почти не гидролизуется влагой воздуха, что и позволяет применять его для заражения атмосферы. Лишь в очень влажном воздухе облако CG за счет частичного гидролиза приобретает белесоватость.
Фосген, растворенный в воде, быстро гидролизуется даже при низкой температуре с образованием угольной и соляной кислот:

При температуре 0°С в 100 г воды за 20с разлагается 1 г CG. Щелочи сильно ускоряют реакцию:

Фосген энергично реагирует как с жидким, так и с газообразным аммиаком с образованием нетоксичных мочевины и хлористого аммония:

Эту реакцию можно использовать для дегазации CG в местах застоя (низинах, закрытых помещениях) посредством распыления аммиачной воды. Однако к этой рекомендации следует подходить осмотрительно: по зарубежным данным, скорость разложения газообразного фосгена аммиачно-воздушной смесью меньше, чем можно было ожидать, и время полного уничтожения ОВ измеряется часами.
Легко происходят реакции фосгена с первичными и вторичными аминами. Например, с анилином количественно образуется дифенилмочевина:

Реакция используется в аналитических целях.
На получение мочевины и некоторых ее производных расходуется значительная доля всего производимого промышленностью фосгена. Мочевина используется как удобрение и добавка к кормам для жвачных животных. На ее основе получают мочевинно-формальдегидные смолы, меламин, циануровую кислоту, ряд лекарственных средств.
Другим направлением мирного использования фосгена является его взаимодействие с солями первичных аминов с образованием изоцианатов:

Органические изоцианаты алифатического и ароматического рядов служат промежуточными продуктами синтеза полиуретанов, которые применяются для производства пенопластов, волокон, искусственной кожи, эластомеров, лаков, клеев, герметиков. Достаточно сказать, что в 1980 г. мировое производство полиуретанов составило 3,6 млн т.
Третичные амины образуют с фосгеном продукты присоединения, разлагающиеся водой. Реакция с полициклическим гексаметилентетрамином (уротропином) в первую мировую войну лежала в основе защитного действия от фосгена так называемого «влажного противогаза» (ватно-тканевой маски, пропитанной раствором уротропина):

При взаимодействии CG с первичными и вторичными спиртами образуются эфиры угольной кислоты (карбонаты). При этом один атом хлора замещается быстро:

Продукты замещения одного атома хлора в фосгене низшими алифатическими спиртами (метиловым или этиловым) обладают сильным слезоточивым действием и в первую мировую войну применялись в качестве ОВ раздражающего действия. Метиловый эфир хлоругольной кислоты служит исходным продуктом для синтеза вещества DP (дифосгена).
Другой атом хлора замещается намного медленнее первого. В результате образуются устойчивые средние карбонаты:

В присутствии оснований (акцепторов хлористого водорода) можно заместить один или оба атома хлора в фосгене на остаток любого спирта или фенола. Так же легко реагируют алкоголяты или феноляты:

Способность фенолятов быстро образовывать сложные эфиры с фосгеном дает возможность использовать эти вещества в качестве поглотителей в средствах защиты органов дыхания.
Третичные спирты при взаимодействии с CG не превращают его в средний карбонат: промежуточно образующийся эфир хлоругольной кислоты разлагается с выделением хлористого алкила, например:

Как хлорангидрид кислоты CG вступает в реакцию Фриделя-Крафтса, образуя кетоны, что используется в синтезах красителей дифенил- и трифенилметанового ряда.
Реакция с йодистым натрием в безводном ацетона используется для количественного определения фосгена. Выделившийся свободный йод оттитровывают тиосульфатом натрия:

При температуре 200—400 °С фосген реагирует с окислами и сульфидами металлов, переводя их а хлориды, например:

Реакция используется для получения безводных хлоридов металлов. Хлорирующее действие фосгена объясняется его термической диссоциацией, которая начинается при температуре 200°С. При температуре 800 °С фосген полностью диссоциирует:
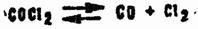
Однако при взрыве термическая деструкция CG незначительна, поэтому возможно его применение в боеприпасах взрывного типа.
Дата добавления: 2015-04-15; просмотров: 162; Мы поможем в написании вашей работы!; Нарушение авторских прав |