
КАТЕГОРИИ:
АстрономияБиологияГеографияДругие языкиДругоеИнформатикаИсторияКультураЛитератураЛогикаМатематикаМедицинаМеханикаОбразованиеОхрана трудаПедагогикаПолитикаПравоПсихологияРиторикаСоциологияСпортСтроительствоТехнологияФизикаФилософияФинансыХимияЧерчениеЭкологияЭкономикаЭлектроника
Контрольная работа 1. Химическая термодинамика
Химическая термодинамика. Химическая кинетика и равновесие
Вариант 8
1. Что называется стандартным изменением энергии Гиббса, единица измерения энергии Гиббса?
2. Сколько теплоты выделится при разложении 54 г глюкозы по реакции:
С6Н12О6 (кр) ® 2С2Н5ОН (ж) + 2СО2 (г), если:
ΔfH˚298 (С6Н12О6 кр) = -1273,00 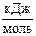 ;
;
ΔfH˚298 (С2Н5ОН ж) = -276,98 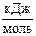 ;
;
ΔfH˚298 (CO2 г) = -393,51 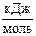 .
.
3. Определите изменение энтропии реакции при стандартных условиях:
4NH3 (г) + 3О2 (г) ® 6Н2О (ж) + 2N2 (г)
4. В какую сторону сместится равновесие реакции:
2СО (г) + О2 (г) « 2СО2 (г); ΔrH° = -566,0 кДж
при повышении температуры, при понижении давления?
5. Температурный коэффициент скорости некоторой реакции равен 2. На сколько градусов надо повысить температуру, чтобы скорость химической реакции увеличилась в 16 раз?
6. При установлении равновесия реакции:
4HCl (г) + O2 (г) « 2Cl2 (г) + 2Н2О (г)
концентрации веществ – участников реакции равны соответственно ( 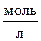 ):
):
[HCl] = 0,1; [O2] = 0,05; [Cl2] = 0,9; [H2O] = 0,9.
Рассчитайте константу равновесия и исходную концентрацию хлороводорода.
Дата добавления: 2015-04-16; просмотров: 73; Мы поможем в написании вашей работы!; Нарушение авторских прав |