
КАТЕГОРИИ:
АстрономияБиологияГеографияДругие языкиДругоеИнформатикаИсторияКультураЛитератураЛогикаМатематикаМедицинаМеханикаОбразованиеОхрана трудаПедагогикаПолитикаПравоПсихологияРиторикаСоциологияСпортСтроительствоТехнологияФизикаФилософияФинансыХимияЧерчениеЭкологияЭкономикаЭлектроника
Энтропия заңы мен даму процессінің қарама-қайшылығын талдау.
Энтропия (грек. еntropіa – бұрылыс, айналу) – тұйық термодинамикалық жүйедегі өздігінен жүретін процестің өту бағытын сипаттайтын күй функциясы. Энтропияның күй функциясы екендігі термодинамиканың екінші бастамасында тұжырымдалады. Энтропия ұғымын термодинамикаға 1865 ж. Р.Клаузиус енгізген. Оның физикалық мәнін қарастыру үшін изотермиялық процесс кезіндегі жылу мөлшерінің Q жылу беруші дененің температурасына Т қатынасын қарастырады.  қатынасын келтірілген жылу мөлшері деп атайды. Процестің өте кіші бөлігіндегі келтірілген жылу мөлшері
қатынасын келтірілген жылу мөлшері деп атайды. Процестің өте кіші бөлігіндегі келтірілген жылу мөлшері  ға тең. Кез-келген қайтымды процесс кезінде денеге берілетін келтіріген жылу мөлшері нольге тең:
ға тең. Кез-келген қайтымды процесс кезінде денеге берілетін келтіріген жылу мөлшері нольге тең:
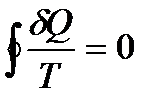
Тұйық интегралдың нольге тең болуы интегралданып тұрған  шамасы бір функцияның толық дифференциалы екендігін көрсетеді. Дифференциалы
шамасы бір функцияның толық дифференциалы екендігін көрсетеді. Дифференциалы  ға тең күй функциясы энтропия деп аталады және S-пен белгіленеді:
ға тең күй функциясы энтропия деп аталады және S-пен белгіленеді: 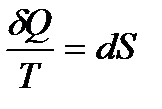
Бұл функция жүйенің күйіне байланысты, ал жүйе сол күйге қандай жолмен келгеніне байланысты емес.
Термодинамикада қайтымды процесс үшін: ΔS = 0,
ал қайтымсыз процесс үшін өседі: ΔS > 0.
Бұл өрнектерді біріктіріп, Клаузиус теңсіздігін алуға болады: ΔS ≥ 0.
Жазылған өрнектер тұйық жүйелер үшін де орындалады. Тұйық жүйенің энтропиясы өседі (қайтымсыз процесс) немесе тұрақты болады (қайтымды процесс).
Егер жүйе тепе-теңдік жағдайда бір күйден екінші күйге өтсе, онда энтропияның өзгерісін төмендегідей анықтауға болады:
 .
.
Физикада энтропия белгілі бір жүйедегі реттіліктің шамасын білдіреді. Жану сияқты қайтымсыз процестер энтропия мөлшерін көбейтеді. Бұл дегеніміз энергияның процестен кейін жүйе ішінде бірқалыпты таралатындығын білдіреді. Кванттық болашақ мектебі энтропия ұғымын ерекше мағынада қолданады. Энтропия хаосқа ену шамасын анықтауда, әсіресе қоғамдық және жеке тарапта, қолданылады. Энтропия шығармашылықтың қарама-қайшылығы болып табылады. Энтропияның жоғарылауы немесе төмендеуі мағынаны жоғалтып ұқсастықты жоғарылатады. Қоғамдық жаппай күйреу және оның ізімен өркениеттен нақты бағытталған тіршілік етуге ұмтылыс дәл осы мағынадағы энтропияның жоғарылауының айқын мысалы болып табылады.
Дата добавления: 2015-01-01; просмотров: 216; Мы поможем в написании вашей работы!; Нарушение авторских прав |