
КАТЕГОРИИ:
АстрономияБиологияГеографияДругие языкиДругоеИнформатикаИсторияКультураЛитератураЛогикаМатематикаМедицинаМеханикаОбразованиеОхрана трудаПедагогикаПолитикаПравоПсихологияРиторикаСоциологияСпортСтроительствоТехнологияФизикаФилософияФинансыХимияЧерчениеЭкологияЭкономикаЭлектроника
Карбоновые кислоты
Карбоновые кислоты содержат карбоксильную группу  , онаможет быть связана с алкильным или арильным радикалом. Число карбоксильных групп определяет основность кислот.
, онаможет быть связана с алкильным или арильным радикалом. Число карбоксильных групп определяет основность кислот.
При составлении названия карбоновой кислоты алифатического ряда по номенклатуре ИЮПАК за основу берут наиболее длинную углеродную цепь, включающую карбоксильную группу. Нумерацию цепи начинают с атома углерода карбоксильной группы. К названию углеводорода по числу атомов углерода в главной цепи прибавляют суффикс -овая кислота.

Для первых членов гомологического ряда карбоновых кислот используют тривиальные названия. Их применяют и для замещенных карбоновых кислот, обозначая положения заместителей буквами a, b, g и т. д.

Для построения названия производных кислот следует знать названия ацилов и ацилатов этих кислот (табл. 4).
|
Таблица 4
|
Карбоновая кислота (acid)

| Ацил

| Ацилат

|
Муравьиная, метановая 
| Формил, метаноил

| Формиат, метаноат

|
Уксусная, этановая

| Ацетил, этаноил

| Ацетат, этаноат

|
Пропионовая, пропановая

| Пропионил, пропаноил

| Пропионат, пропаноат

|
Масляная, бутановая

| Бутирил, бутаноил

| Бутират, бутаноат
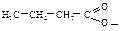
|
Валериановая, пентановая

| Валерил, пентаноил

| Валерат, пентаноат

|
Бензойная
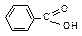
| Бензоил
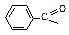
| Бензоат

|
(о-, м-, п-)Толуиловая

| (о-, м-, п-)Толуил

| (о-, м-, п-)Толуилат

|
Названия кислот алициклического и гетероциклического рядов образуют путем прибавления к названию углеводорода или гетероарена окончания -карбоновая кислота.

|
Карбоксильная группа представляет собой сочетание карбонильной и гидроксильной групп. Карбоксильный атом углерода находится в sp2-гибридном состоянии и связан с другими атомами s-связями. Они лежат в одной плоскости под углом 120о друг к другу. Остающаяся р-орбиталь атома углерода перекрывается с р-орбиталью атома кислорода, при этом образуется p-связь. Одна из неподеленных электронных пар атома кислорода гидроксильной группы образует единую p-электронную систему с p-электронами двойной связи С=О. Делокализация электронной плотности в карбоксильной группе показана на примере мурвьиной кислоты.

Действительно, сравнение длин связей  в спирте и
в спирте и  в кислоте показывает, что эта связь в кислоте короче.
в кислоте показывает, что эта связь в кислоте короче.

В то же время связь  в кислотах длиннее, чем та же связь в карбонильных соединениях.
в кислотах длиннее, чем та же связь в карбонильных соединениях.

В результате такого распределения электронной плотности атом углерода карбоксильной группы менее склонен к реакциям с нуклеофильными реагентами, чем углерод карбонильной группы альдегидов и кетонов.
Карбоновые кислоты полярны и подобно спиртам могут образовывать водородные связи друг с другом и с другими соединениями. Поэтому алифатические кислоты по растворимости похожи на спирты: кислоты С1-С4 смешиваются с водой, растворимость валериановой кислоты незначительна, а высшие кислоты практически не растворимы в воде. Ароматические карбоновые кислоты – твердые соединения, плохо растворимые в воде.
Температуры кипения карбоновых кислот выше, чем температуры кипения спиртов с близкой молекулярной массой. Отмеченное различие объясняется большей полярностью карбоновых кислот и более прочными водородными связями, которые они образуют в соответствующих димерах. Димеры карбоновых кислот устойчивы даже в газообразном состоянии.
|

Значения теплот димеризации велики. Например, значение теплоты димеризации муравьиной кислоты в газовой фазе составляет минус 58,5 кДж/моль (минус 14 ккал/моль).
Муравьиная и уксусная кислоты обладают раздражающим запахом. Масляная, валериановая и капроновая кислоты имеют неприятный запах. Высшие жирные и ароматические кислоты не имеют запаха, поскольку обладают малой летучестью.
Дата добавления: 2014-12-30; просмотров: 165; Мы поможем в написании вашей работы!; Нарушение авторских прав |