
КАТЕГОРИИ:
АстрономияБиологияГеографияДругие языкиДругоеИнформатикаИсторияКультураЛитератураЛогикаМатематикаМедицинаМеханикаОбразованиеОхрана трудаПедагогикаПолитикаПравоПсихологияРиторикаСоциологияСпортСтроительствоТехнологияФизикаФилософияФинансыХимияЧерчениеЭкологияЭкономикаЭлектроника
МЕТАЛЛА
Цель работы. Приобретение навыков экспериментального определения
эквивалентной и молярной массы двухвалентного металла
по объему вытесненного водорода.
В основе работы лежит способность активных металлов (Mg, Al, Zn, Fe и др.) вытеснять водород из разбавленных растворов кислот (HCl, H2SO4) по реакции
2 Me + 2n H+ = 2 Men+ + n H2↑.
Зная массу металла и, измерив объем выделившегося в реакции водорода, по закону эквивалентов можно определить эквивалентную массу металла, а затем и его молярную массу.
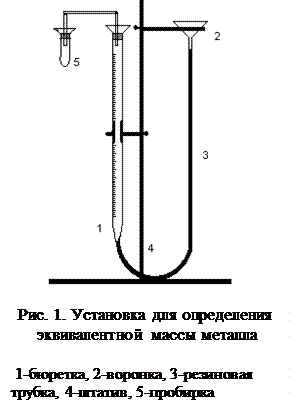
На рис. 1. изображена установка для выполнения эксперимента.
Установка состоит из бюретки 1 и воронки 2, соединенных резиновой трубкой 3, заполненных водой. Бюретка и воронка крепятся к штативу 4 и представляют собой сообщающиеся сосуды. К бюретке присоединена пробирка 5, в которой осуществляется реакция взаимодействия металла с кислотой.
Получите навеску металла у лаборанта. Перед началом работы убедитесь в герметичности установки. Для этого, проверив, плотно ли вставлены пробки в бюретку и пробирку, поднимите воронку на 10-15 см и зафиксируйте ее в этом положении. Если в течение 1-2 минут уровень воды в бюретке не изменяется, значит, установка герметична, и можно приступать к работе.
 Установив одинаковый уровень воды в бюретке и воронке, по нижнему краю мениска замерьте уровень воды (V1) в бюретке. В пробирку налейте 4-5 мл 10 % - ной соляной кислоты. Фильтровальной бумагой высушите верхнюю часть пробирки. Держа пробирку в наклонном положении, осторожно поместите на край пробирки навеску металла так, чтобы после присоединении пробирки к установке металл находился нижепробки, но не касался кислоты. Плотно закройте отверстие пробирки пробкой и приведите пробирку в вертикальное положение, чтобы весь металл опустился в кислоту; при этом начнется реакция.
Установив одинаковый уровень воды в бюретке и воронке, по нижнему краю мениска замерьте уровень воды (V1) в бюретке. В пробирку налейте 4-5 мл 10 % - ной соляной кислоты. Фильтровальной бумагой высушите верхнюю часть пробирки. Держа пробирку в наклонном положении, осторожно поместите на край пробирки навеску металла так, чтобы после присоединении пробирки к установке металл находился нижепробки, но не касался кислоты. Плотно закройте отверстие пробирки пробкой и приведите пробирку в вертикальное положение, чтобы весь металл опустился в кислоту; при этом начнется реакция.
После того как реакция закончится, дайте пробирке охладиться (3-4 мин.). Затем, опуская кольцо с воронкой, снова установите одинаковый уровень воды в бюретке и воронке, и вторично замерьте уровень воды в бюретке (V2).
Определите температуру опыта по термометру, а давление – по барометру.
Необходимо учесть, что водород, собранный над водой в бюретке, насыщен водяным паром. Поэтому общее давление в бюретке, равное атмосферному (Pатм) складывается из парциальных давлений водорода (PH2) и насыщенного водяного пара (PH2O): Pатм = PH2 + PH2O. Тогда PH2 = Pатм - PH2O. Давление водяного пара при температуре опыта определите, пользуясь таблицей 3.1.
Экспериментальные и расчетные данные внесите в таблицу 3.2.
Таблица 3.1.
ДАВЛЕНИЕНАСЫЩЕННОГО ВОДЯНОГО ПАРА ПРИ РАЗЛИЧНЫХ ТЕМПЕРАТУРАХ
| Температура, 0С | Давление, Па | Температура, 0С | Давление, Па | Температура, 0С | Давление, Па |
Таблица 3.2.
ЭКСПЕРИМЕНТАЛЬНЫЕ И РАСЧЕТНЫЕ ДАННЫЕ
| Масса навески металла, г | Условия опыта | Объем водорода в условиях опыта, м3 | Объем водорода, при н.у., м3 | Молярная масса металла, г/моль | Эквивалентная масса металла, г/моль | Ошибка опыта | ||||||||||
| Температура, К | Давление, Па | Уровень воды, м3 | ||||||||||||||
| опытная | теоретическая | опытная | теоретическая | абсолютная, г/моль | относительная, % | |||||||||||
| атмосферное | насыщенного водяного пара | до опыта | после опыта | |||||||||||||
| m (Me) | Т | Ратм | P(H2O) | V1 | V2 | VH2 | V0H2 | M оп. | М теор. | MЭ оп. | МЭ теор. | Δ абс. | Δ отн. | |||
РАСЧЕТНАЯ ЧАСТЬ
По разности между двумя объемами воды рассчитайте объем выделившегося водорода V(H2) = V2 – V1.
Расчет эквивалентной массы металла следует проводить двумя способами.
1. По массе выделившегося водорода (m(H2)).
Находят массу выделившегося водорода, используя уравнению Менделеева-Клайперона:
 ,
,
а затем, по выражению закона эквивалентов, определяют экспериментальное значение эквивалентной массы M¢Э(Ме):

2. По объему выделившегося водорода.
Пользуясь уравнением объединенного газового закона, приводят объем полученного в результате реакции водорода (VH2) к нормальным условиям (V0H2):
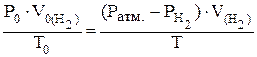
и также, по выражению закона эквивалентов, определяют экспериментальное значение эквивалентной массы M¢¢Э(Ме):

где Vэ(H2) = 11,2 л/моль;
V0(H 2) - объем водорода, приведенный к нормальным условиям;
P0 и T0 – значения давления и температуры при н.у.
Исходя из значения молярной массы металла M оп.(Ме) и учитывая его валентность, по периодической системе элементов Д.И.Менделеева определяют металл и теоретическое значение его молярной массы M теор.(Ме). Затем рассчитывают теоретическое значение эквивалентной массы MЭтеор.(Ме):

Абсолютную и относительную погрешности (ошибки) опыта определяют по формулам:
Dабс. = ½ M теор.(Ме) - M оп.(Ме) ½; 
Дата добавления: 2015-04-11; просмотров: 249; Мы поможем в написании вашей работы!; Нарушение авторских прав |