
КАТЕГОРИИ:
АстрономияБиологияГеографияДругие языкиДругоеИнформатикаИсторияКультураЛитератураЛогикаМатематикаМедицинаМеханикаОбразованиеОхрана трудаПедагогикаПолитикаПравоПсихологияРиторикаСоциологияСпортСтроительствоТехнологияФизикаФилософияФинансыХимияЧерчениеЭкологияЭкономикаЭлектроника
Задачи и упражнения для самостоятельного решения. 24.1. Составить уравнения реакций получения кислорода в лабораторных условиях
24.1. Составить уравнения реакций получения кислорода в лабораторных условиях. Как получают кислород в промышленности?
24.2. Какой объем кислорода (условия нормальные) можно получить при разложении 200 мл 15,5 %-го раствора пероксида водорода Н2О2, плотность раствора 1,1 г/мл? (Ответ: 11,2 л).
24.3. Закончить уравнения реакций:
а) P + O2 = …; б) Al + O2 = …; в) H2S + O2 = …; г) Na2O + CO2 = ….
24.4. Закончить уравнения реакций: а) Na2O + SO3 = …; б) Na2O + Al2O3 = …;
в) Al2O3 + SO3 = …; г) ВаО + H2O = …; д) Cl2O7 + H2O = ….
24.5. Какие свойства в окислительно-восстановительных реакциях проявляет пероксид водорода? Закончить уравнения реакций:
а) KI + H2O2 + H2SO4 = …; б) Hg(NO3)2 + H2O2 + NaOH = ….
24.6. Определить массовую долю (%) Н2О2 в растворе, если при разложении
500 г его выделилось 5,6 л кислорода (условия нормальные). (Ответ: 3,4 %).
24.7. Закончить уравнения реакций: а) Cr2(SO4)3 + H2O2 + KOH = …;
б) Ag2O + H2O2 = …; в) MnO2 + H2SO4 (конц.) = ….
24.8. При термическом разложении перманганата калия образовался объем кислорода (условия нормальные), равный объему О2, который получился в результате разложения водой 18,32 г Na2O2. Рассчитать массу разложившегося KMnO4. (Ответ: 37,1 г).
24.9. Закончить уравнения реакций: а) AgNO3 + H2O2 + KOH = …;
б) Cl2 + H2O2 = …; в) Co(OH)2 + H2O + O2 = ….
24.10. Написать уравнения реакций получения кислорода: а) из оксида марганца (IV); б) из оксида ртути (II); в) из нитрита калия.
24.11. Закончить уравнения реакций: а) HgCl2 + H2O2 + K2CO3 = …;
б) AuCl3 + H2O2 + NaOH = …; в) KClO3 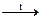 ….
….
24.12. Сколько миллилитров 3 %-го раствора пероксида водорода (плотность раствора 1,1 г/мл) и воды надо взять для получения 750 мл 0,1 М раствора Н2О2? (Ответ: 77,27 мл Н2О2; 672,73 мл Н2О).
24.13. Закончить уравнения реакций: а) HgCl2 + H2O2 = …;
б) Fe(OH)2 + O2 + H2O = …; в) KMnO4 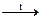 ….
….
24.14. Какой объем 3 %-ного раствора Н2О2 (ρ = 1,1 г/мл) и какая масса кристаллического KMnO4 прореагировали в кислой среде, если в результате реакции выделилось 1,12 л кислорода при нормальных условиях?
(Ответ: 51,52 мл Н2О2; 3,16 г KMnO4).
24.15. Закончить уравнения реакций получения пероксида водорода:
а) BaO2 + H2SO4 = …; б) Na2O2 + H2O = …; в) BaO2 + CO2 + H2O = ….
24.16. Написать уравнения реакций получения кислорода разложением:
а) KMnO4; б) K2Cr2O7; в) HgO.
24.17. При взаимодействии подкисленного раствора KI с раствором Н2О2 массой 0,8 г выделилось 0,3 г йода. Вычислить массовую долю (%) Н2О2 в растворе. (Ответ: 5 %).
24.18. Для полного обесцвечивания 20 мл 0,02 М раствора KMnO4 в сернокислой среде потребовался равный объем раствора Н2О2. Какова молярная концентрация Н2О2? Какой объем кислорода (условия нормальные) выделился при этом? (Ответ: 0,05 М; 22,4 мл).
24.19. Закончить уравнения реакций: а) K2Cr2O7 + H2O2 + H2SO4= …;
б) MnSO4 + H2O2 + KOH = …; в) HIO3 + H2O2 = ….
24.20. Какая масса 3,4 %-го раствора Н2О2 требуется для окисления 100 мл 1 М раствора FeSO4 в присутствии H2SO4? (Ответ: 50 г).
Дата добавления: 2014-11-13; просмотров: 313; Мы поможем в написании вашей работы!; Нарушение авторских прав |