
КАТЕГОРИИ:
АстрономияБиологияГеографияДругие языкиДругоеИнформатикаИсторияКультураЛитератураЛогикаМатематикаМедицинаМеханикаОбразованиеОхрана трудаПедагогикаПолитикаПравоПсихологияРиторикаСоциологияСпортСтроительствоТехнологияФизикаФилософияФинансыХимияЧерчениеЭкологияЭкономикаЭлектроника
Порядок расчета. Рассчитаем массу и объемный расход компонентов газа (кг и м3):
Рассчитаем массу и объемный расход компонентов газа (кг и м3):
m  = 2000 × 0,07 × 80 = 11 200 кг/ч = 3,11 кг/с;
= 2000 × 0,07 × 80 = 11 200 кг/ч = 3,11 кг/с;
V  =
= 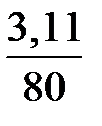 × 22,4 = 0,87 м3/с.
× 22,4 = 0,87 м3/с.
m  =
=  = 1,78 кг/с;
= 1,78 кг/с;
V  =
=  × 22,4 = 1,25 м3/с.
× 22,4 = 1,25 м3/с.
m  =
= 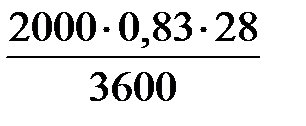 = 12,91 кг/с;
= 12,91 кг/с;
V  =
=  × 22,4 = 10,33 м3/с.
× 22,4 = 10,33 м3/с.
Количество тепла, поступающего с газом, равно:
Q  = 1,42 × 40 × 0,87 = 49,42 кДж/с;
= 1,42 × 40 × 0,87 = 49,42 кДж/с;
Q  = 1,42 × 40 × 1,25 = 71,0 кДж/с;
= 1,42 × 40 × 1,25 = 71,0 кДж/с;
Q  = 1,42 × 40 × 10,33 = 586,74 кДж/с.
= 1,42 × 40 × 10,33 = 586,74 кДж/с.
Количество тепла, поступающего с олеумом, составляет:
Qолеума = 1,34 × 40 × x = 53,76 × x кДж/с,
где x - масса олеума, кг.
Количество тепла, выделяющееся в результате конденсации SO3, рассчитывается по (51)
Qконд= 481,85 × 3,11 × 0,5 = 749,28 кДж/с.
Масса и химическое количество SO3, абсорбированного олеумом, составляют:
m  = 3,11 × 0,5 = 1,56 кг/с;
= 3,11 × 0,5 = 1,56 кг/с;
n  =
= 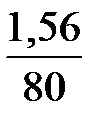 = 0,02 моль/с.
= 0,02 моль/с.
Количество тепла, выделяющееся при растворении жидкого SO3, равно
Qраств = 23,25 × 0,02 = 0,47 кДж/с.
Таким образом, приход тепла составит
Qприх = Q  + Q
+ Q  + Q
+ Q  + Qолеума + Qраств+ Qконд=
+ Qолеума + Qраств+ Qконд=
= 1456,91 + 53,6 × х кДж/с.
Определим расход тепла с уходящим газом.
Так как конденсируется 1,56 кг/с SO3, то на выходе его масса и объем составят
m  = 3,11 - 1,56 = 1,55 кг/с;
= 3,11 - 1,56 = 1,55 кг/с;
V  =
=  × 22,4 = 0,43 м3/с.
× 22,4 = 0,43 м3/с.
Количество тепла, выносимое с газом, равно
Q'  = 1,42 × 55 × 0,43 = 33,58 кДж/с;
= 1,42 × 55 × 0,43 = 33,58 кДж/с;
Q'  = 1,42 × 55 × 1,24 = 96,84 кДж/с;
= 1,42 × 55 × 1,24 = 96,84 кДж/с;
Q'  = 1,42 × 55 × 10,33 = 806,77 кДж/с.
= 1,42 × 55 × 10,33 = 806,77 кДж/с.
Количество тепла, выносимое с олеумом, равно
Q'олеума= (x + 1,56) × 1,34 × 55 = 114,5 + 73,7 × x кДж/с.
Расход тепла составит
Qрасх = Q'  + Q'
+ Q'  + Q'
+ Q'  + Q'олеума = 1051,69 + 73,7 × x кДж/с.
+ Q'олеума = 1051,69 + 73,7 × x кДж/с.
Так как Qприх = Qрасх, то получаем
1456,91 + 53,6 × х = 1051,69 + 73,7 × x;
х = 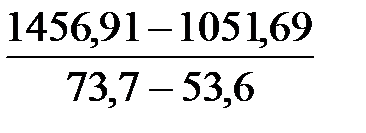 = 20,16 кг/с.
= 20,16 кг/с.
Таким образом, на орошение требуется 20,16 кг/с олеума.
Пример 11.Определить теоретическую температуру горения серы в воздухе по реакции
S + O2 = SO2 + Q (296 000 кДж).
Теплоемкости веществ, участвующих в процессе, кДж/(кмоль · град): SO2 – 50,6; N2 - 31,9.
Дата добавления: 2015-01-05; просмотров: 334; Мы поможем в написании вашей работы!; Нарушение авторских прав |