
КАТЕГОРИИ:
АстрономияБиологияГеографияДругие языкиДругоеИнформатикаИсторияКультураЛитератураЛогикаМатематикаМедицинаМеханикаОбразованиеОхрана трудаПедагогикаПолитикаПравоПсихологияРиторикаСоциологияСпортСтроительствоТехнологияФизикаФилософияФинансыХимияЧерчениеЭкологияЭкономикаЭлектроника
В условиях аптеки можно приготовить из листьев наперстянкт настой в соотношении 1:400.
Биотрансформация дигитоксина в дигоксин происходит в результате реакции 12-гидроксилирования, катализируемой ферментом клеток Digitalis lanata.
Вопрос 4.Рецепт выписан верно. Дигитоксин - Список А. В условиях аптеки хранят в металлическом, запирающемся на ключ шкафу в прохладном месте.
Срок действия рецепта - 1 мес. Рецепт хранится в аптеке 5 лет.
В своей деятельности аптечные работники руководствуются Перечнями и списками лекарственных средств, такими, как: Перечень ЖНВЛС;
Перечень наркотических средств, психотропных веществ и их прекурсоров, подлежащих 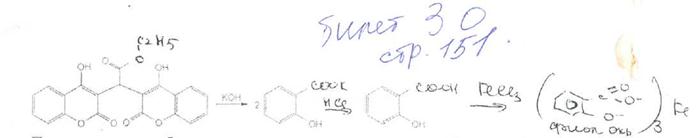
пидлинниихь лилииикумацсшш устанавливают с помощью реакции азосочетания. которую выполняют после предварительного нагревания на водяной бане (3-5 мин) с 0.1 М раствором гидроксида натрия. В этих менее жестких условиях происходит разрыв лактонного цикла:
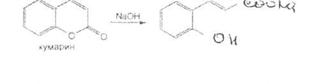
Образовавшийся фенол сочетают с диазотированной сульфаниловой кислотой или другим ароматическим амином. Появляется ярко-оранжевое или вишнево-красное окрашивание (азокраситель).
С концентрированной серной кислотой при слабом нагревании этилбискумацетат дает желтое, а затем оранжевое окрашивание. Разбавление окрашенного продукта водой приводит к образованию белого осадка, который представляет собой ди-(4-оксикумаринил-3)-уксусную кислоту (продукт гидролиза этилбискумацетата):

Полученная кислота ооразует растворимые соли. При добавлении раствора аммиака осадок растворяется, образуя бесцветный раствор, а после добавления гидроксида натрия получается раствор соломенно-желтого цвета.
Присутствие остатка этилового эфира в молекуле этилбискумацетата подтверждают реакцией с раствором иода и гидроксида натрия, в результате которой образуется йодоформ, имеющий характерный запах.

Для идентификации и количественного определения этилбискумацетата используют способность входящих в молекулу . фенольных гидроксилов к этерификации. Ацетилирование этилбискумацетата уксусным ангидридом (нагревание с обратным холодильником) проводят в течение 1 ч, затем реакционную смесь выливают в воду и оставляют на 30 мин. Образуется осадок диацетата этилбискумацетата: 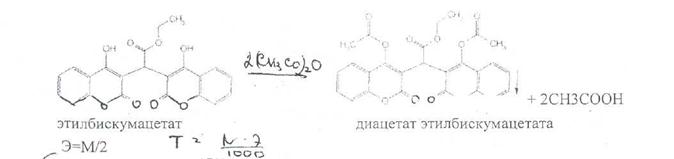
/ Подлинность этилбискумацетата подтверждают по температуре плавления / перекристаллизованного и высушенного диацетата. Количественное определение можно / выполнить гравиметрическим методом

При испытании на чистоту устанавливают наличие продуктов синтеза или гидролиза. В этилбискумацетате методом ТСХ определяют примесь ди-(4-оксикумаринил-3)-уксусной кислоты.
Количественное определение этилбискумацетата основано на кислотных свойствах его растворов в органических растворителях, обусловленных наличием в молекуле двух - гидроксильных групп. Определение проводят методом нейтрализации, титруя 0,1 М раствором гидроксида натрия. Растворителем служит ацетон. При титровании используют смешанный индикатор (смесь метилового красного и метиленового синего). Происходит образование монозамещенной соли (енолята):

Этилбискумацетат хранят по списку А в хорошо укупоренной таре, предохраняющей ОТ действия света и влаги. Применяют производные 4-оксикумарина в качестве антикоагулянтов непрямого действия (антивитаминов группы К). Назначают для профилактики и лечения тромбозов этилбискумацетат по 0,2 г в первый день, по 0,15 г 3 раза во второй день, затем по 0,2-0,1 г в сутки.
Вопрос 2. Fructus Ammi majoris — плоды амми большой (Ammi majoris fructus — аммибольшой плод)
Собранные в период массового созревания центральных зонтиков и высушенные плоды культивируемого однолетнего травянистого растения амми большой (Ammi majus L.) из сем. зонтичных — Apiaceae (Umbell-ferae); используют в качестве лекарственного сырья.
Амми большая — травянистый однолетник с прямым, бороздчатым, в верхней части ветвящимся стеблем высотой до 140 см. Листья дважды-трижды перисторассеченные на ланцетные, по краю зубчатые сегменты. Соцветие — сложный зонтик, состоящий из 50 лучей зонтичков, которые при созревании плодов сжимаются в «гнездышки». Листочки обертки и оберточек многочисленные, цельные. Плоды — вислоплодники, распадающиеся на два мерикарпия.
Химический состав. Плоды содержат до 2 % смеси фурокумаринов, состоящей в основном из изопимпинеллина, бергаптена и ксантотоксина в примерном соотношении 5 : 2 : 3, а также дигидрокумарин мармезин; флавоноиды, фитостерины, сапонины, полисахариды.

R1 = ОСНз, R2 = Н - бергаптен
R1 = Н, R2 = ОСНз - ксантотоксин
R1 = ОСНз, &2 = ОСНз - изопимпинеллин
Кумарины флуоресцируют в УФ-свете желтым, зеленоватым, голубым, фиолетовым светом. В щелочной среде флуоресценция усиливается.
Одним из самых характерных свойств кумаринов как лактонов является их специфическое отношение к щелочи. Для кумаринов характерна большая устойчивость лактонного кольца, которое под действием горячей разбавленной щелочи размыкается с образованием соли кислоты цис-орто-коричной (кумаринаты). При этом раствор желтеет. При подкислении раствора а-пироновое кольцо замыкается и кумарины регенерируются в неизменном виде. Это свойство кумаринов используется для их качественного определения (лактонная проба).

В основу количественного определения кумаринов положены их специфические физико-химические свойства. Методики количественного определения кумаринов можно подразделить на объемные, оптические, полярографические, комбинированные. В настоящее время для количественной оценки сырья и кумаринсодержащих препаратов используютподбирают с учетом избирательности (селективности), т. е. стремятся к тому, чтобы он максимально извлекал комплекс действующих вешеств и как можно меньше сопутствующих. При этом он должен не только хорошо растворять действующие вещества, но и легко десорбировать их с растительного материала. Последним обстоятельством объясняется использование смеси растворителей. При получении новогаленовых препаратов наряду с широко употребляемыми экстрагентами (этанол, вода) используют водные растворы кислот, солей, смеси этанола с хлороформом и др.
При выборе метода экстракции стремятся с наименьшей затратой времени и экстрагента получить концентрированное, т. е. обогащенное действующими веществами, извлечение. Наиболее широко при получении новогаленовых препаратов используют противоточную экстракцию, иногда мацерацию с циркуляцией экстрагента или с механическим перемешиванием (при работающей мешалке); при применении легко летучих экстрагентов — циркуляционную экстракцию.
На стадии очистки извлечения подвергают последовательной обработке, целью которой является выделение комплекса действующих веществ в нативном состоянии, свободного от балласта. Приемы и способы очистки первичных извлечений весьма разнообразны и индивидуальны.
Наиболее широко используют избирательное, фракционное осаждение действующих или балластных веществ, экстракцию в системах жидкость — жидкостью, адсорбцию и ионный обмен.
А в и с а н (Avisanum) — препарат, содержащий до 8 % суммы хромонов, а также небольшие количества фурокумаринов и флавонов.
Препарат получают из плодов амми зубной (Ammi visnaga L.). Плоды амми, высушенные на воздухе и содержащие не менее 0,8 % хромонов и не более 14% влаги (в пересчете на абсолютно сухое сырье экстрагируют 50 % этанолом.
Извлечение.
Противоточное экстрагирование
Метод заключается в многоступенчатом продвижении экстрагента с более истощенного на менее истощенное сырье до насыщения экстрактивными веществами. В промышленности противоточное экстрагирование проводится различными способами: в батарее экстракторов, когда сырье находится в неподвижном состоянии, а движется только экстрагент; в экстракторах непрерывного действия, диффузорах, где сырье и экстрагент движутся навстречу друг другу.
Экстрагирование в батарее экстракторов. Процесс происходит таким образом, что в каждом экстракторе сырье настаивается определенное время, в первом — с чистым экстрагентом, в последующих — с вытяжками, полученными из предыдущих экстракторов. Батарея экстракторов связана между собой с помощью штуцеров и трубопроводов, является коммуницированной. Получается замкнутая система, позволяющая подавать экстрагент и получать вытяжку из любого экстрактора. Этот метод используется на крупных заводах, которые выпускают продукцию одного наименования в больших количествах. Батарея монтируется из 4—5 и одного запасного экстрактора для обеспечения ее непрерывной работы, которая может продолжаться длительное время. Числоэкстракторов в батарее и скорость движения экстрагента должны обеспечить возможность его полного насыщения к моменту получения готовой вытяжки из последнего экстрактора и полного истощения сырья в первом. Принцип противоточного экстрагирования в батарее экстракторов можно проследить на рис. 2.
Чистый экстрагент непрерывно подается на сырье в первый экстрактор. В момент получения готового продукта из последнего экстрактора (V) первый отключают и загружают запасной (VI). Чистый экстрагент подается на сырье во втором экстракторе, который становится первым, а готовый продукт получают из запасного экстрактора, который становится последним. Таким образом, готовый продукт получают с менее истощенного сырья. Во всей батарее поддерживается значительная разность концентраций. Метод позволяет истощить сырье в каждом экстракторе максимально.
Из экстракта в вакууме отгоняют растворитель, а сиропообразный остаток высушивают в вакуум-сушильном шкафу при температуре 60—70 °С до влажности не более 8 %. Сухой остаток измельчают в шаровой мельнице, просеивают Из 12 кг амми зубной получают 1 кг ависана.
Ависан — аморфный порошок, желто-бурого цвета, горького вкуса, со слабым своеобразным запахом Гигроскопичен. Препарат выпускают в таблетках по 0,05 г, покрытых оболочкой. Хранят в сухом, защищенном от света месте. Применяют в качестве спазмолитического средства при почечной колике и спазмах мочеточников. Вопрос 4. Рецепт выписан верно. Неодикумарин хранят в металлическом шкафу (сейфе), привинченному к полу в плотно укупоренной таре , на внутренней стороне дверок должна быть надпись "A" Venena. На окнах материальных комнат должны быть решетки
Срок действия рецепта - 2 мес. Рецепт отдается больному с указание на обороте количества отпущенного препарата и даты отпуска и не хранится в аптеке. По истечении срока действия рецепт гасится штампом «Рецепт не действителен».
Способ применения ЛС обозначается на русском или русском и национальном языках с указанием дозы, частоты, времени приема и его длительности.
Неодикумарин рекламировать нельзя, реклама рецептурных препаратов разрешается только в изданиях для медицинских и фармацевтических работников и на мероприятиях, предназначенных для них.
ФЕДЕРАЛЬНЫЙ ЗАКОН ОТ 22.06.1998 N 86-ФЗ (РЕД. ОТ 30.06.2003) "О ЛЕКАРСТВЕННЫХ СРЕДСТВАХ" (ПРИНЯТ ГД ФС РФ 05.06.1998)
Глава XI. ИНФОРМАЦИЯ О ЛЕКАРСТВЕННЫХ СРЕДСТВАХ. РЕКЛАМА ЛЕКАРСТВЕННЫХ СРЕДСТВ
Статья 43. Информация о лекарственных средствах
1. Информация о лекарственных средствах осуществляется в соответствии с требованиями государственного информационного стандарта.
2. Информация о лекарственных средствах, отпускаемых без рецепта врача, может содержаться в публикациях и объявлениях средств массовой информации,специализированных и общих печатных изданиях, инструкциях по применению лекарственных средств, иных изданиях субъектов обращения лекарственных средств.
3. Информация о лекарственных средствах, отпускаемых по рецепту врача, допускается только в специализированных печатных изданиях, рассчитанных на медицинских и фармацевтических работников. Информация о лекарственных средствах для специалистов сферы обращения лекарственных средств может быть представлена в виде монографий, справочников, научных статей, докладов на конгрессах, конференциях, симпозиумах, научных советах, а также инструкций по применению лекарственных средств, предназначенных для врачей.
4. Допускается использование любых материальных носителей информации о лекарственных средствах, позволяющих хранить, передавать и использовать эту информацию без искажений.
Статья 44. Реклама лекарственных средств
1. В средствах массовой информации допускается реклама лекарственных средств, отпускаемых только без рецепта врача.
2. Независимо от формы реклама должна соответствовать фармакологическим данным о лекарственных средствах, полученным при клинических исследованиях лекарственных средств, и требованиям государственного информационного стандарта.
3. Реклама не должна представлять лекарственное средство как уникальное, наиболее эффективное, наиболее безопасное, исключительное по отсутствию побочных эффектов, не должна вводить в заблуждение относительно состава, происхождения, новизны или патентованности лекарственного средства.
4. Реклама не должна подрывать репутацию предприятий - производителей лекарственных средств, веру потребителей в действие лекарственных средств.
5. При рекламе лекарственного средства не допускается его сравнение с другими лекарственными средствами в целях усиления рекламного эффекта.
6. Реклама не должна создавать впечатление ненужности медицинских консультаций или хирургических операций.
7. Реклама не должна содержать утверждений о том, что действие лекарственного средства гарантировано.
8. При нарушении положений настоящего Федерального закона, касающихся рекламы лекарственных средств, федеральный орган исполнительной власти в сфере здравоохранения может запретить дальнейшую рекламу лекарственного средства или предупредить рекламодателя о необходимости изменения подхода к рекламе данного лекарственного средства.
Реклама — это распространяемая в любой форме с помощью любых средств информация о физическом или юридическом лице, товарах, идеях, начинаниях, которая предназначена для неопределенного круга лиц и призвана формировать или поддерживать интерес к этому физическому или юридическому лицу, товарам, идеям, начинаниям и способствовать реализации товаров, идей, начинаний.Под любыми понимаются средства:
массовой информации (радио, печать, телевидение, Интернет);
наружной рекламы (крупногабаритные плакаты, конструкции, электрифицированные панно);
реклама на транспорте;
реклама в местах продажи товара, так называемый мерчандайзинг.
Неопределенный круг лиц определяется нацеленностью рекламы не на конкретного человека, а на группы людей, в качестве которых могут выступать: подростки, пожилые люди, молодые родители, будущие родители, студенты и т.д.
Особая социальная значимость лекарственных средств, их роль в профилактике и лечении больного обуславливает строгие требования, предъявляемые к их рекламе.
Основными законодательными актами, регулирующими рекламу, являются Федеральные законы: «О рекламе» (1995), «О защите прав потребителей» (1995). «Об информации, информатизации и защите информации» (1995), «О лекарственных средствах» (1998), «О наркотических и психотропных веществах» (1998), Указ Президента РФ № 161 от 17.02.95. «О гарантиях права граждан на охрану здоровья при распространении рекламы».
Основное содержание всех этих законов можно представить следующими положениями:
рекламировать можно только лекарственные препараты, официально разрешенные к продаже, т.е. зарегистрированные в РФ;
реклама рецептурных препаратов разрешается только в изданиях для медицинских и фармацевтических работников и на мероприятиях, предназначенных для них.
Билет 31. Вопрос 1. Инсулин применяют при сахарном диабете I типа — инсулинзависимым диабетом (ИЗСД)
В 70-е гг. 20 в. шло прогрессирующее улучшение степени очистки инсулинов, что уменьшило проблемы, обусловленные инсулиновой аллергией, нарушениями работы почек, расстройством зрения и иммунной резистентностью к инсулину. Со времени открытия и до начала 80-х гг. использовали инсулин, получаемый из поджелудочной железы КРС и свиней. Инсулин КРС отличается тремя аминокислотами, свиной -одной аминокислотой от инсулина человека. Наиболее эффективный гормон для заместительной терапии при сахарном диабете - гомологичный инсулин, т.е. инсулин человека.
В 1980 г. датская фармацевтическая компания «Novo» разработала метод превращения инсулина свиньи в инсулин человека ферментативным замещением аланина, последний является 30-й аминокислотой в цепи В, на остаток треонина с последующей хроматографической очисткой продукта, в результате был получен однокомпонентный инсулин человека 99% чистоты.
В Великобритании с помощью Е. coli синтезированы обе цепи человеческого инсулина, которые затем были соединены в молекулу биологически активного гормона. Чтобы одноклеточный организм мог синтезировать на своих рибосомах молекулы инсулина, 
необходимо снабдить его нужной программой, т.е. ввести ему ген гормона. Химическим способом (операцию проводят специалисты биохимики) получают ген, программирующий биосинтез предшественника инсулина или два гена, программирующие в отдельности биосинтез цепей А и В. инсулина. Следующий этап — включение гена- предшественника инсулина (или гены цепей инсулина порознь) в геном Е. coli — особого штамма кишечной палочки, выращенного в лабораторных условиях; эту задачу выполняет генная инженерия. Из Е. coliвычленяют плазмиду соответствующей рестриктазой. Синтетический ген встраивается в плазмиду (клонированием с функционально активной С-концевой частью Р-галактозидазы Е. coli). В результате Е. coli приобретает способность синтезировать белковую цепь, состоящую из галактозидазы и инсулина. Синтезированные полипептиды отщепляют от фермента химическим путём, затем проводят их очистку. В бактериях синтезируется около 100000 молекул инсулина на бактериальную клетку.
Природа гормонального вещества, продуцируемого Е. coli, обусловлена тем, какой ген встраивается в геном одноклеточного организма. Если клонирован ген предшественника инсулина, бактерия синтезирует предшественник инсулина, который подвергается затем обработке рестриктазами для отщепления препептида с вычленением С-пептида, вследствие чего получается биологически активный инсулин. Для получения очищенного инсулина человека выделенный из биомассы гибридный белок подвергают химико-ферментативной трансформации и соответствующей хроматографической очистке (фронтальной, гель-проникающей, анионообменной).
В Институте биоорганической химии РАН получен рекомбинантный инсулин с использованием генно-инженерных штаммов Е. coli. Из выращенной биомассы выделяется предшественник, гибридный белок, экспрессируемый в количестве 40% от всего клеточного белка, содержащий препроинсулин. Превращение его в инсулин in vitro осуществляется в той же последовательности, что и in vivo - отщепляется лидирующий полипептид, препроинсулин превращается в инсулин через стадии окислительного сульфитолйза с последующим восстановительным замыканием трёх дисульфидных связей и ферментативным вычленением связывающего С~пептида. После ряда хроматографических очисток, включающих ионообменные, гелевыеи ВЭЖХ, получают человеческий инсулин высокой чистоты и природной активности.
Использование аффинной хроматографии значительно снизило содержание в препарате загрязняющих белков с более высокой м.м., чем у инсулина. К таким белкам относятся проинсулин и частично расщепленные проинсулины, которые способны индуцировать выработку антиинсулиновых антител. Стандартизация инсулина по загрязнению классифицирует препараты на обычные, содержащие проинсулина более 1 %, монопиковые — менее 0,3% п, улучшенные монопиковые — менее 0,005% и монокомпонентные, содержащие менее 0,001% проинсулина.
Использование человеческого инсулина с самого начала терапии сводит к минимуму возникновение аллергических реакций, Наиболее частые осложнения инсулиновой терапии -гипогликемические состояния, основными признаками избытка инсулина являютсянарушения функции ЦНС (спутанность сознания, странное поведение, кома).
Компания «Eli Lilly» в массовом производстве человеческого инсулина использует технологию рекомбинантных ДНК, помещая кДНК гена человеческого проинсулина в Е. coli или S. serevisae и гидролизуя наработанный проинсулин до молекулы инсулина. Человеческий инсулин быстрее абсорбируется и независимо от формы препарата имеет более короткую длительность действия, чем животные инсулины. Человеческие инсулины менее иммуногениы, чем свиные, особенно смешанные бычьи и свиные инсулины.
Контроль качества генноинженерного инсулина предполагает контроль дополнительных показателей, характеризующих стабильность рекомбинантного штамма и плазмиды, отсутствие постороннего генетического материала в препарате, идентичность экспрессируемого гена и др. (всего 22 показателя).
В настоящее время в медицинской практике используют инсулины трех типов:
короткодействующие с быстрым началом эффекта; средней продолжительности действия; длительного действия с медленным проявлением эффекта. Инсулин короткого действия — регулярный инсулин — представляет собой короткодействующий растворимый при нейтральном значении рН кристаллический цинк-инсулин, эффект которого развивается втечение 15 мин после подкожного введения и продолжается 5—7 ч.
С целью увеличения длительности действия все другие препараты инсулина модифицированы и при растворении в нейтральной среде образуют суспензию. Они содержат протамин в фосфатном буфере - протамин-цинк-инсулин и НПХ (нейтральный протамин Хагедорна) -НПХ-инсулин или различные концентрации цинка в ацетатном буфере -инсулины ультраленте,ленте, семженте. Изменяя порядок смешивания и длительность перемешивания, можно осадить две физические фракции цинк-инсулина: аморфную и кристаллическую.
Препараты инсулина средней длительности действия содержат протамин, представляющий белок средней м.м. 4400. богатый аргинином и получаемый из молок радужной форели. Для образования комплекса требуется соотношение протамина и инсулина 1:10. После подкожного введения протеолитические ферменты разрушают протамин. позволяя инсулину всасываться.
НПХ-инсулин не изменяет фармакокинетический профиль смешиваемого с ним регулярного инсулина. НПХ-инсулин предпочтительнее инсулина ленте в качестве компонента средней длительности действия в терапевтических смесях, содержащих регулярный инсулин.
В фосфатном буфере все инсулины (свиной, бычий, человеческий) легко образуют кристаллы с цинком.
Сырьем для получения инсулина из животного сырья является поджелудочная железа рогатого скота и свиней.
Основные стадии:
]. Очистка сырьяпри значении рН 6,5 перемешивают 2 ч; при значении рН 6.2 и 6.0 перемешивают 2 ч и отстаивают 18—20 ч и при значении рН 5,8 перемешивают 2 ч и отстаивают 48—96 ч при температуре 5 °С. Выпавшие кристаллы инсулина отделяют центрифугированием, промывают на воронке Бюхнера ледяной водой дистиллированной, ацетоном и эфиром. Досушивают инсулин на воздухе, в вытяжном шкафу и эксикаторе.
Активность инсулина определяют биологическим путем: по способности понижать содержание сахара в крови у здоровых кроликов. За единицу действия принимают активность 0,04082 мг кристаллического инсулина (стандарта), она должна быть 24—26 ЕД в 1 мг.
Ионно-обменная хроматография основана на различии в кислотно-основных свойствах белков
Адсорбционная хроматография основа на различии в сродстве белков к неполярному адсорбенту
Гель-хроматография основана на различии в молекулярной массе белков
Аффинная хроматография основана на специфичности связывания белков с лигандами
Электрофорез основан на различии в знаке и величине заряда белков.
Вопрос 2. Carbutamide — карбутамид (Букарбан)
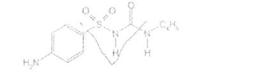
Ы-(п-аминобензолсульфонил)-Н-бутилмочевина
Белый кристаллический порошок, практически нерастворим в воде, растворим в этаноле. Ввиду наличия в молекулах сульфамидной группы, растворы в этаноле и диметилформамиде проявляют кислотные свойства. Растворим в растворах щелочей.
Подлинность производных сульфонилмочевины можно установить методом спектрофотометрии в УФ-области по расположению максимумов поглощения и по удельному показателю поглощения. Раствор карбутамида в этаноле имеет максимум при 269 нм, в 0,1 М растворе хлороводородной кислоты — при 266 и 272 нм, а в 0,1 М растворе гидроксида натрия — при 255 нм.
ПОДЛИННОСТЬ производных сульфонилмочевины устанавливают также с помощью химических реакций.
При нагревании карбутамида в растворе гидроксида калия происходит гидролиз с образованием аммиака, который можно обнаружить по запаху или по изменению окраски лакмусовой бумаги:

Реакция гидролиза происходит также при кипячении производных сульфонилмочевины с разбавленной серной кислотой. Последующее добавление 30%-пого раствора гидроксида2. Измельчение
3. Экстрагирование
4. Очистка вытяжки от белкрв
5. Очистка от жиров
6. Стандартизация
7. Получение лек.формы
Свежие или замороженные ткани железы измельчают на мясорубке-волчке и экстрагируют способом бисмацерации в эмалированном реакторе с мешалкой. В качестве экстрагента для первой мацерации используют 80—85 % этанол, для второй — 57 % этанол, подкисленный кислотой ортофосфорной (серной, хлороводородной) до значения рН 2,8— 3,0. Экстракцию проводят 1.5—4 ч при перемешивании. Экстракты отделяют фильтрованием или центрифугированием, объединяют и проводят очистку.
Предварительная, грубая очистка экстракта одинакова по всем технологиям, она сводится к удалению анионов кислот. Так, анион кислоты ортофосфорной (РОГ3) удаляют раствором кальция хлорида при значении рН 3,3—-3,8. Затем осуществляют депротеинизацию — последовательное отделение балластных белковых веществ при значении рН 4,5—5,1 и 3,5 при температуре 0 °С. Выпадающие осадки отделяют центрифугированием. Прозрачный экстракт концентрируют выпариванием на вакуум-дистилляционной установке пленочного типа при температуре не выше 30 °С до содержания этанола 10—25% в возможно более короткий срок, при строгом соблюдении температурного режима,так как длительное нагревание приводит к инактивации инсулина. Концентрированный остаток очищают от липидов и балластных белков отстаиванием на холоду (0—4 °С) при значении рН 3,0—3,3. От всплывшего слоя липидов и осадка балластных белков экстракт отделяют фильтрованием. Из сгущенного, очищенного экстракта инсулин-сырец выделяют двукратным высаливанием 25 % раствором натрия хлорида или 40 % раствором аммония сульфата. Этот способ используется на некоторых заводах с 1928 г. по настоящее время.
Наиболее прогрессивным является способ выделения инсулина ионообменной хроматографией. По этому способу операцию упаривания исключают, а осуществляют сорбцию Для удаления жира катионит промывают 65—67 % этанолом, а для отделения балластных белков —- 0,3 М раствором ацетатного буфера (рН 5,3). Десорбцию инсулина проводят 0.01—0,05 М раствором аммонийного буфера (рН 9,8—10,0).Инсулин неустойчив в щелочной среде, поэтому десорбируют его быстро, элюат немедленно подкисляют кислотой хлороводородной до значения рН 4,1—4Г5 и добавляют ацетон. Осадок балластных веществ удаляют. Инсулин осаждают в виде цинк-инсулина раствором цинка ацетата (рН 6,1—6,2), очищают кристаллизацией. Цинк-инсулин растворяют в воде, подкисленной кислотой лимонной до значения рН 2,6—2,8. Раствор отстаивают в течение 1 ч и выпавший осадок балластных белков удаляют фильтрованием через кизельгур. Фильтрат смешивают с ацетоном, добавляют цинк хлористый и фенол, охлаждают до температуры 0 °С, создавая условия для медленной кристаллизации инсулина. Раствор подщелачивают до значения рН 8,0—8,5; оставляют на 2—3 мин, затем создают значение рН 6,7—6,8 н перемешивают 1 ч;натрия приводит к выделению жирных капель аминов, имеющих характерный запах. После более продолжительного нагревания (10-30 мин) в присутствии 50%-ной серной кислоты (с обратным холодильником), последующего охлаждения и нейтрализации выделяется осадок сульфамида.

Наличие серы устанавливают после спекания со смесью карбоната и нитрата калия. Затем плав растворяют в хлороводородной кислоте и в фильтрате открывают сульфат-ион.

Сульфамидную группу в глибенкламиде обнаруживают по образованию комплексного соединения с ионом меди (II), выпадающего в виде осадка зеленовато-голубого цвета.

Карбутамид дает ряд других реакций, подтверждающих его подлинность. При пиролизе его кристаллов выделяется аммиак, а плав приобретает фиолетово-красный цвет. После обработки плава этанолом раствор окрашивается в красновато-фиолетовый цвет. При нагревании кристаллов карбутамида и резорцина с 1 мл серной кислоты смесь окрашивается в темно-красный цвет, после разбавления водой и добавления щелочи появляется желто-зеленая флуоресценция.
Карбутамид отличается от других производных сульфонилмочевины наличием первичной ароматической аминогруппы в молекуле.
Реакцию диазотирования и азосочетания с в-нафтолом в щелочной среде. Появляется красное окрашивание.

Реакция образования оснований Шиффа.
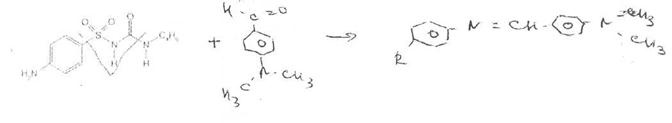
Количественное определение карбутамида выполняют по первичной ароматическойаминогруппе нитритометрическиы методом, устанавливая точку эквивалентности с помощью потенциометра, внешнего или внутренних индикаторов.

Хранят букарбан в сухом, защищенном от света месте, при температуре до 25 °С во избежании процессов гидролиза, окисления препарата. Список Б.
Производные сульфонилмочевины стимулируют образование инсулина в-клетками поджелудочной железы, понижая при этом содержание сахара в крови. Назначают при различных формах сахарного диабета в виде таблеток; карбутамид по 0,5 г, 43.13.
Вопрос 3. Rhizomata et radices Inulae (Rhizomata et radices Inulae
helenii) — корневища и корни девясила (Inulae rhizoma et radix — девясила корневище и корень)
Дикорастущего многолетнего травянистого растения девясила высокого (lnula helenium ' L.) из сем. сложноцветных —Asteraceae( Compoitae); используют в качестве лекарственного средства и лекарственного сырья.
Девясил высокий — крупное растение высотой 60-350 см. Корневище толстое, короткое, многоглавое, корни до 20 см длиной и 2-3 см толщиной. Листья продолговато-эллиптические, неравнозубчатые, снизу густоопушенные, бархатистые. Цветки желтые, краевые — ложноязычковые и срединные — трубчатые, собраны в крупные корзинки 6-7 см в диаметре. Плод — четырехгранная бурая семянка с хохолком. Цветет в июле — августе, плоды созревают в августе — сентябре.
Химический состав. Корневища и корни девясила содержат 1-3 % эфирного масла, основными компонентами которого являются сапонины и бициклические сесквитерпеновые лактоны с преобладанием алантолактона и изоалантолактона. Богаты инулином (до 40 %)г*

Химические методы определения подлинности. Качественные реакции. При нанесении на поперечный срез корневища 2—3 капель раствора йода не должно наблюдаться синего окрашивания (крахмал).
При нанесении на поперечный срез 2—3 капель 20 % спиртового раствора а-нафтола или тимола и 1 капли концентрированной серной кислоты должно наблюдаться красно-фиолетовое или оранжево-красное окрашивание соответственно (инулин).
Заготовка сырья, первичная обработка и сушка. Сырье от дикорастущих растений заготавливают вручную, выкапывая лопатами. Для возобновления зарослей оставляют один вполне развитый плодоносящий экземпляр на 10 м2. Повторные заготовки на этой же заросли возможны через 8 лет. Для восстановления зарослей несколько кусочков корневища, на верхушках которых имеются почки возобновления, закапывают в почву, не заглубляя их.
Выкопанное сырье отряхивают от почвы, быстро промывают в холодной воде, удаляют остатки стеблей (срезая их при основании), а также тонкие корешки и почерневшие или поврежденные корни. Корневища и толстые корни разрезают на куски длиной 3-20 см и расщепляют продольно с толщиной слоя 1-3 см.
Корневища и корни провяливают в течение 2-3 дней на открытом воздухе, а в сырую погоду — под навесом. Затем сушат в теплых, хорошо проветриваемых помещениях или в сушилках при температуре не выше 40 °С. В сухую погоду допускается сушка на солнце.
Хранение. На складах сырье хранят отдельно от других видов сырья. Срок годности сырья 3 года.
Использование. Корневища и корни девясила в аптеки поступают в измельченном виде и в форме брикета. Отвар из сырья девясила применяют как отхаркивающее средство при заболеваниях верхних дыхательных путей. Они также входят в состав противокашлевых сборов; используются для получения представляющего собой сумму сесквитерпеновых лактонов препарата «Алантон», который обладает противовоспалительным действием; применяют при язвенной болезни желудка и двенадцатиперстной кишки.
Используется в гомеопатии как маточное средство. Пряность.
Вопрос 4. Рецепт выписан верно. Срок действия рецепта - 2 мес. Рецепт отдается больному с указание на обороте количества отпущенного препарата и даты отпуска и не хранится в аптеке. По истечении срока действия рецепт гасится штампом «Рецепт не действителен».
Способ применения ЛС обозначается на русском или русском и национальном языках с указанием дозы, частоты, времени приема и его длительности, а для ЛС,
В защите от действия пониженной температуры нуждаются растворы инсулина. Препараты инсулина разрушаются при замерзании.
Хранят при Т от +2 до +8С
Сроки годности см билет №24Билет 32. Вопрос 1.
Пенициллины
Структурной основой лекарственных веществ полусинтетических пенициллинов является 6-аминопенициллановая кислота, которая включает конденсированные тиазолидиновый (А) и лактамный (В) циклы:

Лактамный цикл впервые обнаружен в природных пенициллинах и отличается большой лабильностью к воздействию различных факторов.
Пенициллин получают путем микробиологического синтеза. Процесс биосинтеза пенициллинов происходит в асептических условиях при непрерывной аэрации воздухом, температуре около 24°С, рН 6,0-6,5 и должен сопровождаться постоянным перемешиванием. Наличие жира в питательной среде оказывает пеногасящее действие и одновременно стимулирует процесс биосинтеза пенициллинов.
Выделение пенициллина из культуральной жидкости осуществляют фильтрованием или центрифугированием. Вначале мицелий и нерастворимые минеральные соли отделяют от культуральной жидкости. Очистку культуральной жидкости и выделение из нее пенициллина последовательно проводят способом замены растворителя
Отделяют пенициллины друг от друга различными способами: адсорбционной хроматографией (на активированном угле или оксиде алюминия); распределительной хроматографией (на. силикагеле) или противоточным распределением. Воду из растворов удаляют при температуре от -20 до -30°С и глубоком вакууме (лиофильная сушка) или пользуясь распылительной сушилкой, что позволяет предотвратить разложение. Кристаллические соли высокой степени чистоты получают перекристаллизацией из органических растворителей.
Ацилирование 6-АПК (6-аминопенициллановой кислоты) хлор ангидридам и кислот можно получить полусинтетические пенициллины (ампициллин)
Биологические свойства полусинтетических пенициллинов зависят от характера заместителя в положении 6. Устойчивость к b-лактамазам обеспечивают заместители, создающие стерические препятствия разрыву b-лактамного цикла. Поэтому синтетические пенициллины с аминогруппой и карбоксилом в боковой цепи (в положении 6), как правило, обладают более широким спектром антибактериального действия, чем природные пенициллины. В результате разработаны и внедрены в производство такие полусинтетические пенициллины, как ампициллин.
[ Лекарственное вещество Химическая структура Описание
1 СП 
----------.-----„—_------ I------——------.———------—-—— 1
Ampiciilin — ампициллин Белый
мелкокристаллический
^-' \ I ] V -> порошок без запаха.
' 6 Удельное вращение от
4 +280 до +305° (0,25%-
а-аминобензилпенициллин ный водный раствор)
Подлинность синтетических пенициллинов подтверждают с помощью УФ- и ИК-спектрофотометрии. Для растворов ампициллина устанавливают значения оптических плотностей в максимумах (256, 261, 267 нм) и минимумах (255, 260, 266 нм) поглощения.
ИК-спектры полусинтетических пенициллинов идентифицируют по совпадению с полосами поглощения соответствующих стандартных образцов в области 4000—400 см- .
Важная физическая константа пенициллинов — удельное вращение водных или спиртовых растворов. Все они вращают плоскость поляризованного света вправо.
Для установления подлинности ампициллина используют метод ВЭЖХ. Подлинность подтверждают, сравнивая время удерживания пика со стандартным образцом.
Химические реакции, используемые для испытаний подлинности пенициллинов, основаны на обнаружении в их молекулах различных функциональных групп, продуктов деструкции, атома серы, связанных аминов, катионов калия и натрия.
Для испытания подлинности используют цветную реакцию, основанную на разрыве в-лактамного цикла с образованием внутрикомплексной соли меди (II) с гидроксамовой кислотой (осадок зеленого цвета) или железа (III) — красное или фиолетовое окрашивание:


Образование этих солей происходит только в определенных интервалах значении рН.
Во всех пенициллинах можно обнаружить органически связанную серу после превращения ее в сульфид-ион сплавлением с едкими щелочами. Сульфид-ион затем открывают по образованию красно-фиолетового окрашивания после добавления раствора нитропруссида натрия.

А при взаимодействии с реактивом Фелинга приобретает фиолетовое окрашивание.
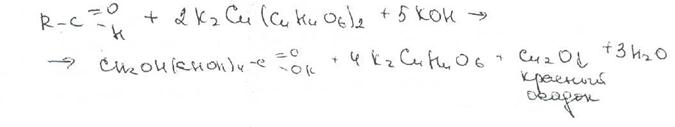
Затем за счет взаимодействия фенола с реактивом Марки происходит образование ауринового красителя, имеющего красное окрашивание. При нагревании на водяной бане наблюдается усиление интенсивности окраски.

Наблюдается оранжево-желтое (ампициллин)
Ряд испытаний выполняют для установления степени чистоты природных и синтетических пенициллинов. По величине оптической плотности растворов определяют светопоглощающие примеси. Выбор длины волны и допустимые значения оптической плотности зависят от химической структуры испытуемого пенициллина.
Синтетические пенициллины испытывают на наличие воды (по методу К. Фишера) и устанавливают рН растворов или водных суспензий (потенциометрически).
Испытание на токсичность
Испытание проводят на здоровых белых мышах обоего пола массой 19—21 г, на которых ранее не проводили никаких испытаний.
За 24 ч до испытания и во время его проведения животные должны находиться в помещении с постоянной температурой. За 2 ч до взвешивания и отбора животных для проведения испытаний у них отоирают корм и воду.
Каждую серию препарата испытывают на 5 мышах. Растворитель, концентрация раствора (тест-доза) и способ введения указаны в частных статьях.
Раствор препарата, подлежащего испытанию, подогревают до 37 °С и в объеме 0,5 мл вводят в хвостовую вену мыши со скоростью 0.1 мл/с, если в частной статье нет других указаний.Испытание проводят на здоровых кроликах обоего пола, не альбиносах, массой 2—3,5 кг, содержавшихся на полноценном рационе. Каждый кролик должен находиться в отдельной клетке в помещении с постоянной температурой. Колебания температуры не могут превышать ±3 °С. При уборке клеток и взвешивании животных их оберегают от возбуждения (избегать шума и резких движений).
ОПРЕДЕЛЕНИЕ АНТИМИКРОБНОЙ АКТИВНОСТИ АНТИБИОТИКОВ МЕТОДОМ
ДИФФУЗИИ В АГАР
Определение антимикробной активности антибиотиков основано на их способности угнетать рост микроорганизмов. Определение проводят методом диффузии в агар на плотной питательной среде путем сравнения размеров зон угнетения роста тест-микробов, образующихся при испытании растворов определенных концентраций Государственного стандартного образца и испытуемого препарата.
Антимикробная активность антибиотиков выражается в единицах действия — ЕД или «мгк». Для большинства антибиотиков 1 ЕД или «мкг» соответствуют 1 мкг активного вещества (кислоты или основания); для антибиотиков, имеющих иное количественное выражение единицы, соответствующие указания даются в частных статьях.
При определении антимикробной активности антибиотиков используют стандартные образцы, активность которых, как правило, устанавливают в соответствии с Международными биологическими стандартами. При отсутствии последних для указанных целей могут быть использованы международные химические стандарты, антимикробную активность которых рассчитывают на основании показателей качества, установленных физико-химическими методами. Антимикробную активность стандартных образцов антибиотиков, не имеющих аналогов в международной коллекции стандартов, рассчитывают также на основании показателей качества, установленных физико-химическими методами.
Методы количественного определения
Ампициллин количественно определяют методом формольного титрования, подобно аминокислотам. Навеску растворяют в воде, добавляют разбавленный нейтрализованный раствор формальдегида и через 2 мин титруют раствором гидроксида натрия (индикатор фенолфталеин).


Известен меркуриметрический метод определения ампициллина с использованием в качестве титранта нитрата ртути (II) или хлорида ртути (II).
Активность пенициллинов устанавливают микробиологическим методом по антибактериальному действию на определенный штамм золотистого стафилококка. Одна единица действия соответствует активности 0,5988 мкг химически чистой натриевой соли бензилпенициллина (1670 ЕД в 1 мг). Микробиологический метод определения пенициллинов дает воспроизводимость результатов 5-10%. Этот метод приведен в ряде ФС как альтернативный вместе с химическим или спектрофотометрическим методом. Алкалиметрический метод определения суммы пенициллинов имеет удовлетворительную воспроизводимость, но дает завышенные результаты, так как одновременно титруются все примеси, взаимодействующие со щелочью.
Наиболее точные, сопоставимые с микробиологическим методом результаты дает спектрофотометрическое определение пенициллинов, основанное на их гидролизе до пеницилленовых кислот. Они имеют максимум с вето поглощения при 320-324 или 335 нм. Присутствие ионов меди (И) повышает чувствительность реакции и воспроизводимость результатов определения. Общая схема гидролиза пенициллинов в кислой среде с образованием пеницилленовых кислот может быть представлена следующим образом:
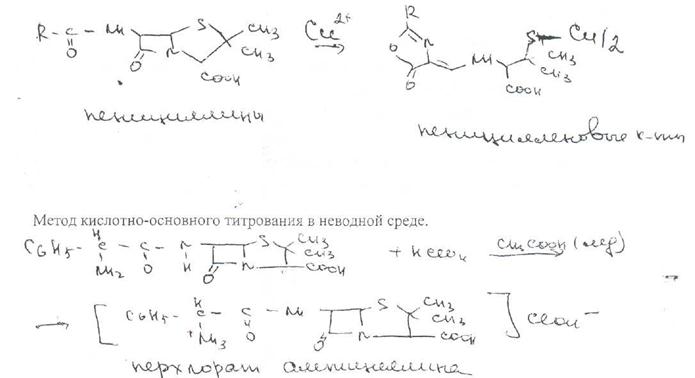
Пенициллины хранят по списку Ь, в сухом месте, при комнатной температуре. Упаковывают соли бензилпенициллина во флаконы, герметически закрытые резиновыми пробками,обжатыми алюминиевыми колпачками. На воздухе, при повышении температуры, в присутствии влаги, тяжелых металлов они быстро разлагаются. Ампициллин хранят в банках оранжевого стекла вместимостью по 0,5 кг,
УНАЗИН (Unasyn). Таблетки покрыты оболочкой.
Комбинироввнный препарат, содержащий в соотношении 2:1 ампициллин-натрий и сульбактам-натрий. Синоним: Sulacillm. Сульбактам-натрий - натриевая соль сульфонпенициллата - является производным основного ядра пенициллинов. Белый кристаллический порошок; легко растворим в воде. Сульбактам-натрий не обладает выраженной антибактериальной активностью, но необратимо ингибирует Ь-лактамазу (фермент, разрушающий b-лактамное ядро пенициллинов). При использовании вместе с пенициллинами, сульбактам защищает последние от гидролиза и инактивации. Уназин (комбинация сульбактама с ампициллином) является высокоэффективным препаратом, действующим на грамположительные и грамотрицательные аэробы и анаэробы, включая пенициллиноустойчивые штаммы.
Применение: Синусит, средний отит, фарингит, ларингит, инфекции мочевых путей, внутрибрюшинные, кожи и мягких тканей, костей и суставов; септицемия, пневмонии, пиелонефрит, гонококковые инфекции, профилактика хирургических инфекций.
Ампициллин влияет не только на Гр+, но и на Гр- бактерии, угнетая синтез клеточной стенки.
Вопрос 2. Radices Glycyrrhizae (Radices Liquiritiae) — корни солодки (лакричный корень) (Glycyrrhizae radix (Liquiritiae radix) — солодки корень)
Солодка голая (Glycyrrhiza glabra L.) и с. уральская (G. iiralensis Fisch.) из сем. бобовых — Fabaceae (Leguminosae
Химический состав. В подземных органах обнаружены: тритерпеновый сапонин — глицирризин (до 23 %), придающий корням сладкий вкус, — это кальциевая и калиевая соли кислоты глицирризиновой, агликоном которой является кислота глицирретиновая (глицирретовая), а углеводная часть глицирризина представлена двумя молекулами кислоты глюкуроновой, присоединяющимися к агликону у Сз; 27 флавоноидов, производные флаванона и халкона (ликвиритин, изоликвиритин и др.); полисахариды (крахмал, пектиновые вещества). Корневища содержат больше глицирризина, чем корни. 
R = Н - ликвиритигенин R = Gic - ликвиритин
Анализ сырья складывается из нескольких стадий: экстракция сапонинов из сырья, очистка полученного извлечения, разделение на индивидуальные компоненты.
Кислоту глицирризиновую определяют методом формольного титрования, используя кислотные свойства.

R = Н — изоликвиритигенин R = Glc - изоликвиритин
Сапонины, сапонизиды —- гликозиды (гетерозиды), производные стероидов и тритерпеноидов, обладающие гемолитической и поверхностной активностью и токсичностью для холоднокровных животных. В зависимости от химического строения агликона (сапогенина) их классифицируют на стероидные и тритерпеновые.
Для сапонинов характерен ряд биологических свойств, которые могут быть использованы в анализе. Они вызывают гемолиз эритроцитов за счет образования комплексов с холестерином мембран, вследствие чего оболочка эритроцита из полупроницаемой становится проницаемой и гемоглобин выходит в плазму крови, окрашивая ее в красный цвет («лаковая» кровь); нарушают функционирование жабр холоднокровных животных и ядовиты для них. Свойства сапонинов Характеристика свойств
1. Физические Сапонины — бесцветные, желтоватые кристаллические или аморфные свойства гигроскопические вещества с высокой температурой плавления (с
разложением). Водные растворы их при встряхивании образуют обильную устойчивую пену, вследствие способности понижать поверхностное натяжение. Растворимость в гидрофильных растворителях (вода, метанол и этанол различной концентрации) увеличивается с возрастанием количества моносахаридов в гликозильной части молекулы сапонина. Нерастворимы в бензоле, хлороформе, диэтиловом эфире. Оптически активны.
2. Химические Сапонины гидролизуются кислотами, олигозиды тритерпеновых кислот свойства щелочами. Многие из них образуют молекулярные комплексы со
стеринами, липидами, белками, фенольными соединениями, которые частоне проявляют гемолитических свойств и могут быть разрушен*
хлороформом.
Тритерпеновые сапонины (кислые) образуют комплексы с солями Pb, Ci
гидроксидами Ва, Mg; образуют окрашенные продукты (полиены)
кислотными реагентами (концентрированная кислота серная, уксусны:
ангидрид, сурьма треххлористая. кислота фосфорномолибденовая и др.).
Сапонины вызывают гемолиз эритроцитов за счет образования комплексов с холестерином мембран, вследствие чего оболочка эритроцита из полупроницаемой становится проницаемой и гемоглобин выходит в плазму крови, окрашивая ее в красный цвет.
Микроскопия. При микроскопическом исследовании поперечного среза диагностическое значение имеют широкие сердцевинные лучи, расширяющиеся во вторичной коре, и присутствие во вторичной коре деформированного луба, группы лубяных волокон с сильно утолщенными стенками, окруженных кристаллоносной обкладкой. Сосуды древесины разного диаметра окружены группами склеренхимных волокон с кристаллоносной обкладкой На продольно-радиальном срезе в коре и древесине видны длинные, сильно утолщенные склеренхимные волокна с кристаллоносной обкладкой; в древесине узкие сосуды — сетчатые, средние — со щелевидными порами, широкие — с бочковидными короткими члениками и ромбическими окаймленными порами, расположенными косыми рядами.
Хранение. Сырье хранят по общему списку в сухом, хорошо проветриваемом помещении. Срок годности 10 лет.
Использование. Препараты солодки издавна применяют как отхаркивающее, слабительное, диуретическое средство, а также как регулирующее водно-солевой обмен. Применяют в виде экстракта густого и сухого, сиропа солодкового корня, эликсира грудного, порошка. Солодковый корень служит основой для пилюль и улучшает вкус различных препаратов и микстур. Кислота глицирризиновая проявляет противовирусное действие. Инактивирует вирусы вне клеток, при этом вирусы опоясывающего лишая и простого герпеса необратимо; блокирует внедрение активных вирусных частиц внутрь клетки и нарушает способность вируса к синтезу новых структурных компонентов. Применяют при вирусных инфекциях половых органов, кожи, слизистых полостей рта. носа, а также при опоясывающем лишае. На основе кислот глицирризиновой и глицирретиновой созданы препараты, обладающие антиаллергическим, противовоспалительным действием и используемые для лечения бронхиальной астмы (препарат «Глицирам»), экзем и аллергических дерматитов (препарат «Глидеринин» — мазь, содержащая 1 %-ную или 2 %-ную кислоты 18-дигидроглицирретовой). На основе флавоноидов корней солодки созданы препараты — «Ликвиритон» и «Флакарбин», обладающие спазмолитическим, противоязвенным, противовоспалительным и антисекреторным действием. Применяют эти
175препараты при гиперацидном гастрите, язвенной болезни желудка и двенадцатиперстной кишки. Недавно обнаружены радиопротекторные свойства биологически активных веществ солодки. Корни входят в состав сбора М. Н. Здренко, их широко используют в пищевой промышленности для приготовления пива, халвы и др. Отпускается сырье в виде брикетов.
Применяется в медицине всех стран мира. Вопрос 3.
Экстракты (от лат. extractum — вытяжка, извлекать, вытягивать) — это концентрированные вытяжки из лекарственного растительного сырья, известны за несколько тысячелетий до нашей эры. В зависимости от применяемого экстрагента их делят на 4 группы: водные (extracta aquosa), спиртовые (extracta spirituosa), эфирные (extracta aetherea), масляные (extracta oleosa). Кроме того, применяют экстракты стандартизированные —- концентраты для приготовления настоев и отваров.
По консистенции различают экстракты: жидкие (extracta fluida),густые (extracta spissa), сухие (extracta sicca).
Густые — вязкие массы, содержащие не более 25 % влаги; сухие экстракты — сыпучие или пористые, губчатые массы, содержащие до 5 % влаги.
Технология экстрактов включает следующие стадии- экстрагирование лекарственного растительного сырья, очистка полученного извлечения, выпаривание, сушка, стандартизация.
Исходное сырье для получения экстрактов должно отвечать требованиям научно-технической документации (быть свежевысушенным, иметь определенную степень измельчения и т д.)
Процесс получения экстрактов связан с правильным выбором экстрагента, который в значительной степени определяет метод экстрагирования. В качестве экстрагентов используют воду, этанол различной концентрации, органические растворители, растительные и минеральные масла.
Экстракты получают методами дробной мацерации, в различных модификациях, перколяции, реперколяции, противоточного и циркуляционного экстрагирования и т. д. (методы описаны в разделах настойки-предыдущих билетах)
Водные экстракты. По консистенции водные экстракты могут быть густыми и сухими.. В настоящее время готовят экстракт корня солодкового густой — Extractum Glycyrrhizae spissum, экстракт корня солодкового сухой — Extractum Glycyrrhizae siccum, Экстракты солодки — бисмацерацией и противоточной экстракцией, При получении экстракта корней солодки методом бисмацерации используют 0,25 % водный раствор аммиака, что вызвано необходимостью перевода плохо растворимой в холодной воде кислоты глицирризиновои в хорошо растворимую аммониевую соль. Экстрагирование корня солодки методом противотока проводится в обогреваемой горячей водой батарее экстракторов, водные извлечения подвергают очистке от сопутствующих веществ, различных ВМС (слизей, пектинов, крахмала, Сахаров и др.), которые способствуют быстрому размножению микроорганизмов в извлечении.
Одним из способов очистки является термическая обработка вытяжки кипячением в течение определенного времени с последующим настаиванием с адсорбирующими веществами (экстракт корня солодки). Очищают вытяжки и настаиванием с адсорбирующими веществами при комнатной температуре в течение нескольких суток (экстракты одуванчика, трилистника водяного) В качестве
176адсорбентов используют тальк, каолин, бентонит и другие вещества. Применяется спирто о чистка, которая заключается в обработке упаренной до сиропообразной консистенции водной вытяжки этанолом в концентрации не ниже 60 % Под действием сильных дегидратирующих свойств этанола исчезает защитный гидратный слой полимеров, в результате чего происходит их коагуляция и выпадение в осадок.
После отстаивания в хорошо закрытой емкости в течение нескольких суток при температуре не выше 8 °С вытяжку сливают и фильтруют через нутч-фильтр (экстракт полыни горькой, получаемый перколяцией).
Очищенные водные вытяжки сгущают в вакуум-выпарной аппаратуре при температуре 50—60 °С. При получении экстракта полыни горькой методом дробной мацерации применяют особый технологический прием: первый слив сразу упаривают в вакуум-выпарном аппарате до консистенции густого экстракта, два последующих — до Уз первоначального объема и после центрифугирования снова упаривают. Все сгущенные вытяжки объединяют.
При производстве сухого экстракта корня солодки упаренные вытяжки подвергают сушке в вакуум-вальцовых сушилках и массу измельчают в шаровых мельницах.
Стандартизуют густые экстракты по содержанию влаги, тяжелых металлов (допустимое количество — не более 0,01 %) В экстракте корня солодки определяют количество кислоты глицерризиновой. В густом экс тракте должно быть не менее 14% , в сухом — не менее 17%.
Водные экстракты применяют в качестве наполнителей при изготовлении пилюль, экстракты корня солодки также для изготовления сиропа и эликсира лакричного. Экстракт травы полыни горькой используют как горечь для возбуждения аппетита и усиления деятельности пищеварительных органов.
Спиртовые экстракты. Спиртовые экстракты по консистенции могут быть жидкими, густыми и сухими Для получения спиртовых экстрактов используют методы перколяции, реперколяции, дробной мацерации по принципу противотока и противоточного экстраги рования. В качестве экстрагента при получении жид ких экстрактов применяют этанол в концентрации от 30 до 90 %, чаще 70 %, в производстве густых и сухих экстрактов — также спирты амиловый, пропиловый, иногда метиловый, которые в процессе производства готового продукта полностью удаляются. При получении густых экстрактов предпочитают использование этанола. Для полного истощения растительного материала при
перколировании требуется 7—9-кратное количество экстрагента.
Жидкий экстракт 1:1 означает, что в одной объемной части готового продукта содержится столько же действующих веществ, сколько в единице массы растительного сырья. На фармацевтических предприятиях экстракт готовят по массе, т е. из единицы массы сырья получают единицу массы готового продукта. Наиболее предпочтительным методом получения жидкихэкстрактов является противоточный, исключающий стадию упаривания извлечения.
Очистка жидких экстрактов как аналогов настоек осуществляется длительным отстаиванием при температуре не выше 8 °С в хорошо закрытых емкостях, с последующим фильтрованием осветленной жидкости через пресс-фильтр.
Очистка вытяжек для густых и сухих экстрактов проводится различными способами:
177аналогично водным извлечениям — кипячением с добавлением адсорбирующих веществ или без них, если экстрагирование проводилось слабым этанолом (20—40 %) и в вытяжках много ВМС (водорастворимых белков, Сахаров, ферментов); обработкой крепким этанолом, путем замены растворителя — к упаренной вытяжке добавляют воду Растворимые в этаноле побочные продукты (хлорофилл, смолистые вещества и некоторые другие) выпадают в осадок. Вытяжку отстаивают, фильтруют или центрифугируют и затем упаривают до нужной концентрации
Густые и сухие экстракты стандартизуют по содержанию влаги и действующих веществ. Экстракты, не соответствующие требованиям НТД по содержанию действующих веществ доводят до стандарта смешиванием с одноименным экстрактом или (при необходимости) разбавляют каким-либо индифферентным веществом густые экстракты - декстрином, сахаром свекловичным, патокой; сухие — сахаром молочным, глюкозой и т. д.
Густые экстракты быстро подвергаются разложению под действием микроорганизмов, их трудно дозировать (отвешивать)
Сухие экстракты большей частью гигроскопичны Многие из них отсыревают в процессе производства и во время хранения Достаточно 1—2 раза открыть банку с сухим экстрактом, как он набирает влагу, сбивается в комки прилипает к стенкам, дозировать его невозможно
В связи с этим проводится поиск методов устранения их гигроскопичности. Установлено что этанол разной концентрации существенно влияет на гигроскопичность экстрактов, следовательно, необходимо подбирать такой экстрагент который не извлекал бы гигроскопичные побочные вещества. По этой же причине обращается внимание на подбор наполнителей при разбавлении экстрактов.
Основные факторы технологии, влияющие на процесс экстрагирования
Полнота и скорость экстрагирования действующих веществ из растительного лекарственного сырья зависит от технологических свойств материала: содержания влаги, действующих и экстрактивных веществ, пористости и порозности, величины поверхности частиц, способности набухать и удерживать определенное количество экстрагента, коэффициентов диффузии, вымывания и др. Их необходимо учитывать в процессе экстрагирования. Пористость сырья — это величина пустот внутри растительной ткани. Чем она выше, тем больше образуется внутреннего сока при набухании. Порозность — это величина пустот между кусками измельченного материала. Она связана с количеством внешнего сока. При набухании порозность возрастает при малом объеме сырья и уменьшается, если его объем большой и он плотно уложен в экстракторе. От величины пористости и порозности зависит скорость смачивания и набухания материала. Скорость набухания возрастает при предварительном вакуумировании сырья, а также при повышении давления и температуры.
Содержание влаги действующих и экстрактивных веществ в сырье дает возможность определить его исходное количество для получения заданного объема препарата. Процентное содержание влаги в сырье строго регламентируется, его повышение может привести к потере действующих веществ.
Высококачественное сырье дает возможность получить препарат, в котором содержание действующих веществ будет выше сопутствующих. Степень и характер измельчения, поверхностьчастиц и число разрушенных клеток оказывают существенное влияние на процесс экстрагирования. Чем мельче размер частиц материала, тем больше поверхность его соприкосновения с экстрагентом, тем быстрее происходит из влечение. Для каждого вида сырья в зависимости от анатомического строения, состава и локализации действующих веществ степень и характер измельчения подбираются индивидуально. Оптимальным считается размер частиц от 0,5 до 2,0 мм, он определяется просеиванием через сито. При использовании слишком измельченного сырья, вследствие сильного набухания резко возрастает гидравлическое сопротивление и процесс экстрагирования затрудняется. Полученная вытяжка будет содержать много мельчайших частичек растительного материала, от которых ее трудно очистить. Из сырья с разрушенной клеточной структурой (раздавленное, истертое, размолотое) процесс извлечения, как указано выше, сводится к вымыванию. В распиленном и изрезанном материале, где сохраняется клеточная структура, преобладают диффузионные процессы, экстрагирование замедляется, но полученная вытяжка содержит меньше механических включений и легче очищается.
Пористость и порозность сырья обусловливают его поглощающую способность.
Коэффициент поглощения сырья определяется по формуле: К=Р2/Р1,
где Р1 и Р2 — соответственно масса сырья до и после набухания.
Различают «внутреннюю» и «полную» поглощаемость сырья. «Внутренняя» — это количество внутреннего сока, удерживаемое сырьем, «полная» — количество экстрагента, поглощенное сырьем и находящееся на его поверхности. Для проведения процесса определяющим является «полная» поглощаемость сырья, которая находится в прямой зависимости от степени его измельчения.
В настоящее время нет единого мнения о необходимости стадии намачивания материала. В ряде случаев она может быть опущена, так как не будет оказывать существенного влияния на процесс экстрагирования. Для некоторых видов сырья она необходима, так как предотвращает запрессовывание материала в экстракторах в результате увеличения его объема при смачивании и способствует эффективности извлечения.
Одним из параметров, характеризующих протекание процесса экстрагирования, является коэффициент вымывания. Если он низкий, это значит, что в сырье мало разрушенных клеток, экстрагирование идет медленно и определяется в основном скоростью молекулярной диффузии, есди достаточно велик, то процесс протекает быстро. В этом случае он зависит главным образом от гидродинамических условий системы. За величину коэффициента вымывания принимают количество вещест
Дата добавления: 2015-01-13; просмотров: 595; Мы поможем в написании вашей работы!; Нарушение авторских прав |