
КАТЕГОРИИ:
АстрономияБиологияГеографияДругие языкиДругоеИнформатикаИсторияКультураЛитератураЛогикаМатематикаМедицинаМеханикаОбразованиеОхрана трудаПедагогикаПолитикаПравоПсихологияРиторикаСоциологияСпортСтроительствоТехнологияФизикаФилософияФинансыХимияЧерчениеЭкологияЭкономикаЭлектроника
Ионная связь
Для тома существует две основные возможности подчиниться правилу октета. Первая из них — образование ионной связи. (Вторая — образование ковалентной связи, о ней речь пойдет ниже). При образовании ионной связи атом металла теряет электроны, а атом неметалла приобретает. Для примера рассмотрим электронное строение атомов натрия и хлора:
Na 1s2 2s2 2p6 3s1 - один электрон на внешнем уровне
Cl 1s2 2s2 2p6 3s2 3p5 – семь электронов на внешнем уровне
Если атом натрия передаст свой единственный Зs-электрон атому хлора, правило октета будет выполнено для обоих атомов. У атома хлора окажется восемь электронов на внешнем третьем слое, а у атома натрия — тоже восемь электронов на втором слое, который теперь стал внешним:
Na+ 1s2 2s2 2p6 - восемь электронов на внешнем уровне
Cl- 1s2 2s2 2p6 3s2 3p6 - восемь электронов на внешнем уровне

Образование ионной связи
При этом ядро атома натрия по-прежнему содержит 11 протонов, но общее число электронов уменьшилось до 10. Это означает, что число положительно заряженных частиц на одну превышает число отрицательно заряженных, поэтому общий заряд „атома” натрия равен +1.
„Атом” хлора теперь содержит 17 протонов и 18 электронов и его заряд равен -1.
Заряженные атомы, образовавшиеся в результате потери или приобретения одно или нескольких электронов, называются ионами. Положительно заряженные ионы получили название катионов, а отрицательно заряженные называются анионами.
Катионы и анионы, имея противоположные заряды, притягиваются друг к другу электростатическими силами. Это притяжение противоположно заряженных ионов и называется ионной связью. Она возникает в соединениях, образованных металлом и одним или более неметаллами. Нижеперечисленные соединения удовлетворяют этому критерию и имеют ионную природу: MgCl2, Fel2, CuF, Na20, Na2S04, Zn(C2H302)2.
Есть и другой способ изображения ионных соединений:

Образование ионной связи
В этих формулах точками показывают только электроны, находящиеся на внешних оболочках (валентные электроны). Такие формулы называют формулами Льюиса в честь американского химика Г. Н. Льюиса, одного из основоположников (наряду с Л. Полингом) теории химической связи.
Перенос электронов от атома металла к атому неметалла и образование ионов возможны благодаря тому, что неметаллы имеют высокую электроотрицательность, а металлы — низкую.
Из-за сильного притяжения ионов друг к другу ионные соединения в большинстве своем твердые и имеют довольно высокую температуру плавления.
Ионная связь образуется при переносе электронов от атома металла к атому неметалла. Образовавшиеся при этом ионы притягиваются друг к другу электростатическими силами.
6. Важнейшие классы неорганических веществ. Оксиды. Получение и свойство..
Первоначально все химические вещества делятся на простые и сложные.
Простые вещества подразделяются на металлы и неметаллы.
Помимо типичных металлов и неметаллов есть большая группа веществ, обладающая промежуточными свойствами, их называют металлоидами.
Сложные вещества подразделяются на четыре класса химических соединений: оксиды, основания, кислоты и соли..
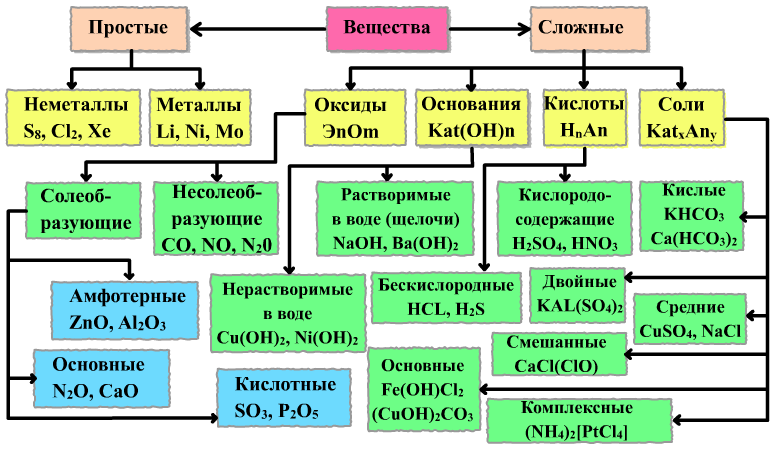 Оксидаминазываются сложные вещества, в состав молекул которых входят атомы кислорода в степни окисления – 2 и какого-нибудь другого элемента.
Оксидаминазываются сложные вещества, в состав молекул которых входят атомы кислорода в степни окисления – 2 и какого-нибудь другого элемента.
Оксидымогут быть получены при непосредственном взаимодействии кислорода с другим элементом, так и косвенным путём (например, при разложении солей, оснований, кислот). В обычных условиях оксиды бывают в твёрдом, жидком и газообразном состоянии, этот тип соединений весьма распространён в природе. Оксиды содержатся в Земной коре. Ржавчина, песок, вода, углекислый газ – это оксиды.
Дата добавления: 2015-01-19; просмотров: 431; Мы поможем в написании вашей работы!; Нарушение авторских прав |