
КАТЕГОРИИ:
АстрономияБиологияГеографияДругие языкиДругоеИнформатикаИсторияКультураЛитератураЛогикаМатематикаМедицинаМеханикаОбразованиеОхрана трудаПедагогикаПолитикаПравоПсихологияРиторикаСоциологияСпортСтроительствоТехнологияФизикаФилософияФинансыХимияЧерчениеЭкологияЭкономикаЭлектроника
Реальный газ, уравнение Ван-дер-Ваальса; первое начало термодинамики; работа при изменении объема; теплоемкость; внутренняя энергия газа.
 1. Реальный газ. Уравнение Ван-дер-Ваал ьса
1. Реальный газ. Уравнение Ван-дер-Ваал ьса
Полученное в предыдущей лекции уравнение состояния идеального газа не является универсальным. Оно оказывается справедливым при достаточно малых давлениях (и плотностях) и выполняется тем точнее, чем меньше давление. По мере же увеличения давления газа его свойства все более отклоняются от свойств идеального газа и, в конце концов, наступает его конденсация в жидкость.
В этом нет ничего удивительного, если
вспомнить те допущения, которые были сделаны
при выводе уравнения состояния идеального газа.
В самом деле, идеальный газ мы определили как
газ, состоящий из молекул, не
взаимодействующих между собой, а сами молекулы при этом считали материальными точками, т.е. мы пренебрегали их размерами и объемом. Однако оба эти допущения являются приближенными.
Так, например, если при атмосферном давлении среднее расстояние между молекулами в 10 раз превосходит их собственные размеры, то при давлении в 100 атм молекулы газа в среднем удалены друг от друга на расстояние, которое только вдвое больше их размеров. В этих условиях объемом молекул нельзя пренебречь, а силы взаимодействия должны уже сказываться не только в моменты столкновений.
Начнем с того, что учтем в уравнении состояния (которое мы будем писать для одного моля газа) ограниченную сжимаемость газа. Для этого надо в уравнении идеального газа Р = RT/V
заменить объем V разностью (V-b), где b -
некоторая положительная постоянная,
учитывающая размеры молекул. Уравнение

показывает, что объем не может быть сделан меньшим, чем Ь, поскольку при V -» b давление Р обращается в бесконечность.
Учтем теперь притяжение молекул. Это притяжение должно приводить к уменьшению давления газа, поскольку на каждую молекулу, находящуюся вблизи стенки сосуда, будет действовать со стороны остальных молекул сила, направленная внутрь сосуда. В грубом приближении эта сила будет пропорциональна числу молекул в единице объема, то есть концентрации газа.
С другой стороны, давление само пропорционально этому же числу. Поэтому общее уменьшение давления, связанное с взаимным

|
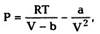
|
| или, иначе, |

|
| Это — так называемое уравнение Ван-дер-Ваальса,или уравнение состояния реального газа, записанное для одного моля. Для произвольного |

|

|
притяжением молекул, будет обратно пропорционально квадрату его объема. В соответствии с этим вычтем из (11.1) выражение
При большом разрежении газа (большие объемы V) величинами а и b можно пренебречь, и мы возвращаемся к уравнению Менделеева — Клапейрона. Ниже мы увидим, что уравнение (11.3) правильно описывает характер явлений и в обратном предельном случае больших сжатий.
Для исследования поведения реального газа, описываемого уравнением Ван-дер-Ваальса, рассмотрим определяемые этим уравнением изотермы - кривые зависимости Р от V при заданных значениях Т. С этой целью перепишем лтавнение М1.2) (лля олного моля) в виде

При заданных значениях Р и Т - это уравнение третьей степени относительно неизвестного V.
Как известно, уравнение третьей степени имеет три корня, из которых вещественными могут быть либо все три, либо один (в последнем случае уравнение имеет также два комплексно сопряженных корня). Физическим смыслом объема могут обладать, разумеется, лишь вещественные (причем положительные) корни. Поэтому заданным значениям Р и Т по уравнению Ван-дер-Ваальса соответствуют либо три различных, либо одно значение объема.
Второй случай всегда имеет место при
достаточно высоких температурах.
Соответствующие изотермы мало отличаются от

|

изотерм идеального газа и являются монотонно спадающими кривыми (кривая 1 на рис.11.1; увеличение номера кривых соответствует убыванию температуры). При более же низких температурах изотермы имеют максимум и минимум (кривые 3, 4Г), так что для каждой из них существуют такие интервалы давлений, в которых кривая определяет три различных значения V (три точки пересечения изотермы с горизонтальной прямой).
Рассмотрим изотерму 3 и выясним, какой смысл имеют различные ее участки. На участках де и са зависимость давления от объема имеет нормальный характер - давление уменьшается при увеличении объема.
Участок же ее соответствовал бы неестественному положению, когда сжатие вещества приводило бы к уменьшению давления. Наличие заведомо неосуществимого участка ее изотермы означает, что при постепенном изменении объема вещество не может оставаться все время в виде однородной среды; в некоторый момент должно наступить скачкообразное изменение состояния и распадение вещества на две фазы.
Другими словами, истинная изотерма будет иметь вид ломаной линии abfg.Часть ее ab отвечает газообразному состоянию вещества, а часть fg— жидкому состоянию. Горизонтальный же прямолинейный отрезок bf соответствует двухфазным состояниям — переходу газа в жидкость, происходящему (при заданной температуре) при определенном постоянном давлении. Можно показать, что отрезок bf должен быть расположен так, чтобы были одинаковы площади bedи def.
При повышении температуры прямолинейный участок изотермы уменьшается и обращается в нуль (на изотерме 2) при температуре, которая называется критической.Проходящая через эту точку изотерма 2 разделяет изотермы двух типов: монотонные изотермы вида 1 и изотермы 3, 4 с минимумами и максимумами, на которых неизбежно распадение вещества на две фазы (жидкость и газ). При критической температуре плотность пара (газа) становится равной плотности жидкости, и пар становится неотличим от жидкости.
Используя уравнение (11.4), нетрудно доказать, что

2. Первое начало термодинамики
Обратимся теперь к энергетической стороне процесса изменения состояния какого-либо тела.
Любое тело (твердое, жидкое, газообразное),
находящееся в определенном состоянии, которое
характеризуется его макроскопическими
параметрами Р, V и Т, обладает определенным запасом внутренней энергииU. Внутренняя энергия тела складывается из кинетической энергии поступательного движения молекул, кинетической энергии вращения молекул, кинетической энергии движения атомов внутри молекулы (если молекула не одноатомная), потенциальной энергии взаимодействия между атомами и потенциальной энергии взаимодействия молекул между собой. В нее, однако, не входит кинетическая энергия движения тела как целого и потенциальная энергия внешних сил, действующих на тело.

|
| помощью какого процесса произошел этот переход, и |

|

|
Внутренняя энергия тела является функцией его состояния.Это означает, что при переходе
начальном и конечном состояниях. Если над телом совершается циклический процесс, в результате которого тело возвращается в исходное состояние, то изменение внутренней энергии за цикл

означает, что бесконечно малое изменение внутренней энергии dU при любом процессе является полным дифференциалом.
Внутреннюю энергию тела можно изменить двумя способами:
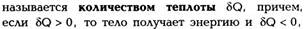
|
| если оно ее отдает. В этом случае изменение внутренней энергии |

|
| 2) Наше тело можно теплоизолировать и |

|
| предоставить телу возможность совершить работу 6А над окружающими телами. В первом случае б А |

|

|
| — положительной |
| случае изменение внутренней энергии |

|
| Если же тело может получать (или отдавать) |
1) Привести тело в контакт с более нагретым или менее нагретым телом. При этом наше тело может получать или отдавать энергию, которая

|

|
Это важное соотношение выражает закон сохранения энергии при тепловых процессах. Его называют первым началом термодинамики.

|

|
Для конечного процесса

Наконец, при изотермическом процессе (Т = const)

Нетрудно доказать, что при циклическом процессе работа А числено равна площади петли цикла на диаграмме Р —V и положительна, если процесс происходит по часовой стрелке (рис.11.3).

|

процесса, с помощью которого тело переводится из состояния 1 в состояние 2. Поэтому говорят,

|

|
процесса(а не состояния, как внутренняя энергия U). Из (11.10) следует, что при циклическом

|
3. Работа при изменении объема
Рассмотрим теперь каждое из слагаемых, вхоляших в пепвое начало тепмолинамики (11.9).
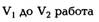
|
| При изменении объема от |

|
производит над окружающими его телами механическую работу. Если объем тела увеличивается на dV, то тело совершает бесконечно малую или элементарнуюработу
4. Теплоемкость
Определим теперь количество теплоты, которое необходимо сообщить телу для его нагревания или отнять от тела для его охлаждения. Конечно, это количество теплоты зависит от массы тела и от того, на сколько градусов должна быть изменена его температура. Поэтому для характеристики тепловых свойств тела пользуются особой величиной — теплоемкостью.
По определению теплоемкостью тела С называется количество тепла, которое нужно подвести или отнять у тела для изменения его температуры на 1 К.
Теплоемкость, отнесенная к единице массы
тела М называется удельной теплоемкостью

|

|
и численно равна площади (см. рис.11.2) под кривой процесса на диаграмме зависимости
Следует отметить, что формулы (11.12) и (11.13) верны для любых тел. Найдем работу, которую совершает идеальный газ при различных процессах.


Теплоемкость, отнесенная к одному молю вещества, называется молярной теплоемкостью
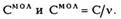

|

|
Обе эти теплоемкости уже характеризуют не само тело, а вещество, из которого тело состоит. Из определения теплоемкости тела следует, что
Пусть нагревание происходит при постоянном объеме (V = const). Соответствующая теплоемкость называется теплоемкостью при постоянном


|

|
Следовательно, подводимое к телу тепло SQ расходуется на изменение температуры dT (изменение внутренней энергии) и изменение объема dV (с этим связана механическая работа).

|
| или на основании (11.19): |
Если при нагревании постоянным остается давление, то теплоемкость называется теплоемкостью при постоянном давленииСР:
и показатель адиабаты

что хорошо согласуется с экспериментом.
Нетрудно показать, что выражение (11.22) можно записать через у:


|

|

|
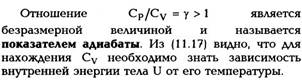
|
| Для идеального газа |
| следовательно, |
5. Внутренняя энергия газа
Начнем с нахождения внутренней энергии идеального газа, которая, как мы знаем, состоит из кинетической энергии поступательного движения молекул газа, кинетической энергии вращения молекул и из энергии колеблющихся внутри молекулы атомов. Каждый из этих трех видов движения вносит определенный вклад и в теплоемкость газа.
Легче всего определить внутреннюю энергию одноатомного идеального газа (таковы благородные газы Не, Ne, Аг), которая представляет собой просто сумму кинетических энергий поступательного движения его частиц. Поскольку по определению температуры средняя
Попытаемся теперь найти внутреннюю энергию идеального газа, состоящего из многоатомных молекул. Как мы знаем из предыдущей лекции, на каждую из трех поступательных степеней свободы приходится кТ/2 кинетической энергии. Согласно классической механике такой результат получился бы для всех вообще степеней свободы молекулы, связанных как с поступательным движением, так и с ее вращением и с колебаниями атомов в ней.
Действительно, в классической (в отличие от квантовой) физике доказывается так называемая теорема о равномерном распределении кинетической энергиипо всем степеням свободы молекул. Эту теорему можно сформулировать так: если система молекул находится в состоянии теплового равновесия при температуре Т, то средняя кинетическая энергия равномерно распределена между всеми степенями свободы молекулы и для каждой степени свободы молекулы она равна кТ/2.
Мы знаем также, что при колебательном движении (см. лекцию 5) среднее значение потенциальной энергии равно среднему значению кинетической энергии, поэтому можно сделать вывод, что на одну колебательную степень свободы приходится энергия кТ (кТ/2
кинетической и кТ/2 потенциальной). В дальнейшем мы будем считать, что на колебательную (как на поступательную и вращательную) степень свободы приходится энергия кТ/2, но число колебательных степеней
будем удваивать.
Если обозначить полное число степеней свободы молекулы буквой i (с удвоенным количеством колебательных степеней), то внутренняя энергия газа из N таких молекул


|

|
то внутренняя энергия газа, состоящего из N одноатомных молекул

Поэтому его теплоемкости (на основании (11.17)и (11.21))
Его теплоемкости
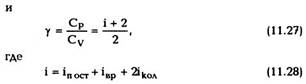
Дата добавления: 2014-10-31; просмотров: 501; Мы поможем в написании вашей работы!; Нарушение авторских прав |