
КАТЕГОРИИ:
АстрономияБиологияГеографияДругие языкиДругоеИнформатикаИсторияКультураЛитератураЛогикаМатематикаМедицинаМеханикаОбразованиеОхрана трудаПедагогикаПолитикаПравоПсихологияРиторикаСоциологияСпортСтроительствоТехнологияФизикаФилософияФинансыХимияЧерчениеЭкологияЭкономикаЭлектроника
Вещество CN

Химические названия: ω-хлорацетофенон; α-хлорацетофенон; хлорметилфенилкетон; хлористый фенацил; фенацил хлорид; хлорацетилбензол; 2-хлор-1-фенил-1-этанон.
Условные названия и шифры: CN (США); САР (Великобритания); O-Salz (Германия); Grandite (Франция).
Хлорацетофенон впервые был получен и исследован в 1871 г. Г. Гребе (Франция). В первую мировую войну он был предложен в США для применения в качестве ОВ, но боевой проверки не прошел. Тем не менее, в межвоенный период и в годы второй мировой войны в США были созданы производственные мощности по производству CN и накоплены его запасы. В Германии хлорацетофенон производился тремя заводами (в Ханенберге, Зеельце и Людвигсхафене) с суммарной годовой производительностью 7,2 тыс. т. Запас вещества уже к маю 1943 г. составил 7114 т.
В послевоенное время хлорацетофенон не потерял своего значения. В 60-е годы американская армия применяла его против национальных сил освобождения Южного Вьетнама.
В армии США разработаны рецептуры на основе CN, позволяющие применять его в любое время года с помощью дисперсионных боевых приборов. Рецептуры имеют шифры CNB (смесь 10% CN, 45% СС14 и 45% бензола), CNC (смесь 30% CN и 70% СНС13), CNS (смесь 24% CN, 38% PS и 38% CHCl3). На вооружении состоят ранцевые и съемные механические генераторы аэрозолей. Резервуар ранцевого генератора вмещает 9 кг CN или рецептуры на его основе, а съемного — 40 кг. Съемные генераторы могут устанавливаться на вертолетах или автомобилях. Существуют химические гранаты, снаряженные порошкообразным CN, из которых ОВ переводится в аэрозоль методом взрыва. Боеприпасы в снаряжении CN и его рецептурами относятся по табельности группе В. Они кодируются одним красным кольцом. Генераторы маркируютс надписью «CN ТАС», а гранаты — «CN RIOT». Хлорацетофенон входит в соста жидких и твердых учебных рецептур многих армий.
Вещество CN — типичный лакриматор. Слезотечение возникает при Снач 0,0005 мг/л, Снеп 0,002 мг/л. При такой концентрации помимо обильного слезотеченш возможно раздражение кожи лица и шеи. IСτ50 0,08 мг·мин/л, LCτ50— 10—11 мг·мин/л.
В чистом виде CN представляет собой бесцветное кристаллическое вещество c приятным запахом цветущей черемухи. Технический продукт может иметь окраску от соломенно-желтой до серой. Плотность 1,321 г/см3 при температуре 20 °С, плотность пара по воздуху 5,3. Растворимость в воде при температуре 20 °С около 0,1%. Оно ограниченно растворяется в неполярных и хорошо — во многих полярных растворителях. Температура кипения CN 245 °С, давление насыщенного пара при температуре 20 °С 0,013 мм рт. ст., летучесть — 0,11 мг/л, температура плавления 59 °С.
Вещество CN относится к классу замещенных жирноароматических кетонов, которые в целом химически устойчивы. Хотя CN вступает в реакции, обусловленные наличием в его молекуле атома хлора, полярной карбонильной группы и ароматического ядра, для осуществления этих реакций требуются определенные условия.
Хлорацетофенон практически не реагирует с водой и может даже перегоняться с водяным паром без заметного разложения. Очень медленно взаимодействуют с ним и щелочи в водных растворах. Только при кипячении в спиртовых или водно-спиртовых растворах щелочей он почти количественно гидролизуется до твердого нетоксичного фенацилового спирта:

Водно-спиртовые растворы сернистого натрия лучше при нагревании превращают CN в нетоксичный дифенацилсульфид и хлористый натрий:

Реакция используется для дегазации CN и для его определения по хлору.
Для CN известны и другие реакции замещения атома хлора, например йаимодействие с йодидами, роданидами, тиосульфатами, алкоголятами, фенолятами, солями карбоновых кислот и т. п., которые описывают общей схемой:

Под действием сильных окислителей (гипохлоритов, окислов хрома, перманганата калия и т.д.) в органических растворителях CN окисляется главным образом до бензойной кислоты:
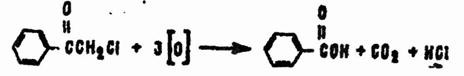
Азотная кислота одновременно окисляет и нитрует CN.
В определенных условиях CN хлорируется в боковую цепь или ароматическое ядро. Такие хлорпроизводные обладают меньшим слезоточивым действием, чем CN, но приобретают кожно-нарывное действие, поэтому реакции имеют ограниченное значение для целей дегазации.
Хлорацетофенон термически стабилен, плавится и перегоняется при атмосферном давлении без разложения. Нагревание его в течение 15 мин при температуре 300 °С вызывает пиролиз 1,5% вещества, при температуре 600 °С — 9% и даже при температуре 750 °С — не более 32%. Он устойчив к детонации и в расплаве смешивается со взрывчатыми веществами. Эти свойства CN позволяют переводить его в аэрозольное состояние термической возгонкой из пиротехнических смесей и даже из сплавов со взрывчатыми веществами.
Для защиты от аэрозоля CN достаточно надеть противогаз. Для дегазации CN применяют подогретые водно-спиртовые растворы сернистого натрия.
Дата добавления: 2015-04-15; просмотров: 310; Мы поможем в написании вашей работы!; Нарушение авторских прав |