
КАТЕГОРИИ:
АстрономияБиологияГеографияДругие языкиДругоеИнформатикаИсторияКультураЛитератураЛогикаМатематикаМедицинаМеханикаОбразованиеОхрана трудаПедагогикаПолитикаПравоПсихологияРиторикаСоциологияСпортСтроительствоТехнологияФизикаФилософияФинансыХимияЧерчениеЭкологияЭкономикаЭлектроника
Теоретическое введение. Железо, кобальт, никель составляют первую триаду элементов VIII группы побочной подгруппы (семейство железа)
Железо, кобальт, никель составляют первую триаду элементов VIII группы побочной подгруппы (семейство железа), расположены в 4 периоде, относятся к d-элементам. Электронное строение 3dn4s2 (n = 6, 7, 8). Степени окисления +2, +3 и +6 (для Fe).
В ряду напряжений Fe, Co, Ni располагаются перед водородом в той же последовательности, в какой они стоят в периодической системе элементов.
В соляной и разбавленной серной кислоте железо, кобальт, никель растворяются при комнатной температуре с выделением водорода и образованием солей М (II).
Под действием концентрированной H2SO4 и дымящей HNO3 при обычной температуре эти металлы пассивируются. Разбавленная азотная кислота растворяет железо с образованием соли Fe (II); продуктами восстановления HNO3 могут быть (в зависимости от концентрации) NH4NO3, N2, N2O: Только концентрированная HNO3 при нагревании растворяет железо с образованием солей
Fe (III).
4Fe + 10HNO3 = 4Fe(NO3)2 + NH4NO3 + 3H2O;
5Fe + 12HNO3 = 5Fe(NO3)2 + N2 + 6H2O;
Fe + 6HNO3 = Fe(NO3)3 + 3NO2 + 6H2O.
Кобальт и никель растворяются в HNO3 с образованием солей М (II) и выделением NO2 в случае концентрированной кислоты и NO в случае разбавленного раствора.
Fe, Co, Ni образуют оксиды MО, M2O3 и М3О4 (МО . М2О3).
Оксид железа Fe+6O3, в свободном состоянии не получен, известны соответствующие соли − ферраты Na2FeO4, K2FeO4.
Оксиды МО и соответствующие им гидроксиды М(ОН)2 обладают основными свойствами, практически не растворимы в воде и растворяются только в кислотах. М(ОН)2 получаются при взаимодействии солей М (II) со щелочами. Гидроксид Fe(OH)2 легко окисляется и частично переходит в Fe(OH)3:
4Fe(OH)2 + 2H2O + O2 = 4Fe(OH)3.
Гидроксид Со(ОН)2 существует в виде двух модификаций − синей и розовой, окисляется в Со(ОН)3 под воздействием кислорода воздуха, но медленнее, чем Fe(OH)2. Под действием окислителей Н2О2, Br2 окисление идет гораздо быстрее. В отличие от Fe(OH)2 и Со(ОН)2 гидроксид Ni(OH)2 устойчив на воздухе и устойчив к действию Н2О2. Окисляется только более энергичными окислителями (Cl2, Br2):
2Ni(OH)2 + Br2 + 2NaOH = 2Ni(OH)3 + 2NaBr.
Оксид Fe2O3 и соответствующий гидроксид проявляют основные свойства, легко растворяются в кислотах, но могут проявлять и слабые амфотерные свойства. При сплавлении со щелочами или содой образуют ферриты:
Fe2O3 + Na2CО3 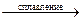 2NaFeO2 + CО2.
2NaFeO2 + CО2.
Оксиды Co2O3 и Ni2O3 и соответствующие им гидроксиды Со(ОН)3 и Ni(OH)3 плохо растворимы в воде, проявляют только основные свойства, являются сильными окислителями. При действии на них кислот образуют соли
М (II) и продкуты окисления, например:
Cо2O3 + 6HCl = 2CoCl2 + Cl2 + 3H2O;
Для железа более устойчивыми являются соединения со степенью окисления +3, для никеля и кобальта +2. Поэтому Fe2+ является довольно сильным восстановителем, тогда как Со2+ и Ni2+ этими свойствами в заметной степени не обладают. В степени окисления +3 железо, кобальт и никель проявляют окислительные свойства; окислительная способность увеличивается в ряду
Fe −Co − Ni .
Соли сильных кислот, как правило, все хорошо растворимы, растворы их вследствие гидролиза имеют кислую среду.
Элементы триады железа легко образуют комплексные соединения, в которых железо может иметь степень окисления +2, +3, кобальт, главным образом, +3, а никель +2. Наиболее характерное координационное число 6, редко 4.
Дата добавления: 2014-11-13; просмотров: 287; Мы поможем в написании вашей работы!; Нарушение авторских прав |