
КАТЕГОРИИ:
АстрономияБиологияГеографияДругие языкиДругоеИнформатикаИсторияКультураЛитератураЛогикаМатематикаМедицинаМеханикаОбразованиеОхрана трудаПедагогикаПолитикаПравоПсихологияРиторикаСоциологияСпортСтроительствоТехнологияФизикаФилософияФинансыХимияЧерчениеЭкологияЭкономикаЭлектроника
Метод травления
Применение определенных способов травления и исследование результатов этих процедур варьируют в широких пределах и зависят от поставленной цели. Главная область применения травления – изучение дефектов строения природных или синтетических кристаллов. Рассмотрим самые популярные методы травления кристаллов.
Газовое травление. В данном методе ионы газа хемосорбируются на полированной поверхности образца, включенного в противоположность ионному травлению анодно, с образованием тонких поверхностных пленок. Смонтированная на столике микроскопа эвакуированная камера травления из кварцевого стекла наполняется корродирующим газом, который ионизируется исходящим с катода электронным пучком посредством захвата электронов нейтральными молекулами газа. Отрицательные ионы газа захватываются положительно заряженной поверхностью образца и ведут в зависимости от реакционной способности отдельных минеральных фаз к образованию различных по толщине и, следовательно, различно окрашенных реакционных слоев.
Термическое травление. Под термическим травлением понимают изменение профиля поверхности с образованием ямок травления, ступеней или фасеток при температурах, которые в общем случае близки к точке плавления, с тем, чтобы в приемлемое время реакции достичь оптимального эффекта испарения. Испарение может происходить в вакууме, где кристалл окружен только своим собственным паром, а также в присутствии постороннего газа.
Травление посредством ионной бомбардировки (ионное травление). Если поверхность металлов бомбардировать при низком давлении ионами, которые ускоряются электрическим полем, то наступает спонтанное распыление обрабатываемого вещества. Благодаря этому становятся видимыми границы зерен, включения и нарушения решетки.
Для различных материалов известны полирующие растворы, которые обладают свойством не разъедать кристалл избирательно, из таких растворов изготавливаются смеси, которые могут подавить шероховатости поверхности выше 1 мкм.
Чтобы полировать металлические поверхности, в первую очередь пользуются способом электролитического полирования, причем образец металла включается как анод.
5) Рентгеновская дифракционная топография
Под рентгеновской дифракционной топографией понимают совокупность методов изучения реальной структуры кристаллов с помощью дифракции рентгеновских лучей. Рентгеновская топография позволяет выявлять различные нарушения периодичности кристаллической структуры: границы субзерен и двойников, выделения примесей, дефекты упаковки, линии скольжения и единичные дислокации. Формирование изображения дефектов на топограммах обусловлено различной интенсивностью рентгеновских лучей, дифрагированных несовершенными и совершенными областями кристаллов. Разрешающая способность рентгеновской топографии около 5·10-3 мкм и выше. Помимо линейного отмечается и угловое разрешение, представляющее собой видимый минимальный угол разориентации блоков. Угловая разрешающая способность рентгеновской топографии составляет от нескольких минут до десятых долей секунды. Большое преимущество метода – возможность изучения объектов без их разрушения.
Рентгеновские топографические методы в зависимости от тех возможностей, которыми они располагают, подразделяются на три группы. Первые из них составляют методы, с помощью которых характеризуют блочную структуру: определяют размер блоков, угол разворота соседних блоков друг относительно друга, расположение малоугловой границы.
Съемка топограмм для исследования блочной структуры кристаллов производится либо на просвет, либо на отражение. Методы различаются спектральным составом используемого излучения (белое или характеристическое) и геометрией съемки. Угловое разрешение зависит, в частности, от расстояния образец – пленка.
При анализе дифракционных пятен на топограммах обычно рассматриваются два взаимно перпендикулярных направления: направление в плоскости рассеяния – радиальное направление, и направление, перпендикулярное плоскости рассеяния – азимутальное направление. По радиальному сдвигу характеристических линий или пятен, получаемых в белом излучении, определяется угол разворота блоков вокруг нормали к плоскости рассеяния, а по азимутальному сдвигу – линии пересечения отражающей плоскости и плоскости рассеяния.
Наиболее распространенным методом, в котором используется съемка на просвет, является метод Фудживара. Съемка осуществляется в смешанном белом и характеристическом рентгеновском излучении от точечного источника. Образец устанавливается перпендикулярно центральному лучу падающего пучка, пленка помещается за образцом параллельно его поверхности, либо перед точкой фокусировки отраженных лучей, либо за ней. Размеры блоков определяются по рентгенограмме путем измерения размера соответствующих рефлексов на поверхность образца. По пятнам, расположенным на двух взаимно перпендикулярных диаметрах пленки, можно определить составляющей разворота блоков относительно трех координатных осей.
Метод Фудживара дает также направление линии пересечения малоугловой границы с поверхностью кристалла. По рентгенограммам, полученным от двух непараллельных срезов, можно определить расположение границы в кристалле. Разрешение метода Фудживара составляет 1 – 2 мин.
К методам, использующим съемку на отражение, относятся методы Шульца, Берга – Барретта и метод с применением проволочной сетки при исследовании блочной структуры. Метод Берга – Барретта использует схему съемки на отражение в монохроматическом излучении. Условия дифракции выбираются так, чтобы угол рассеяния был близок к π / 2, а падающий пучок почти параллелен поверхности образца. Метод находит применение для изучения тонких порядка (1 – 50)·10-3 мкм поверхностных слоев монокристаллов.
С помощью проволочной сетки достигается увеличение разрешения при съемке. Сетка помещается на пути отраженного или падающего пучка. На изображениях соседних блоков наблюдается смещение теней от сетки, по величине которого подсчитывается угол разворота блоков. В местах изгиба кристаллической сетки или на неровностях поверхности наблюдается изгиб теней от сетки.
Когда блочная структура отсутствует или блоки велики (каждый составляет несколько миллиметров), а плотность дислокаций внутри блоков не превышает 105 – 106 см-2, возможно прямое наблюдение дефектов в кристалле методами рентгеновской трансмиссионной топографии, наиболее универсальным среди которых является метод Ланга и его разновидности.
Методом Ланга исследуются нарушения в «тонких» кристаллах, t – толщина их обычно составляет от 0,1 до 2 – 3 мм, а μt < 1, где μ – линейный коэффициент поглощения в кристалле. Принципиально важным представляется коллимированный пучок рентгеновских лучей от микрофокусной трубки для получения дифракции только одной Кα1 составляющей дублета. Прямой пучок отсекается специальной диафрагмой, а дифрагированный регистрируется на фотоматериале с высокой разрешающей способностью. Для получения изображения от большой области кристалла применяют сканирование (возвратно-поступательное движение жестко скрепленных образца и пленки). «Проекционная» топограмма, получаемая при синхронном перемещении кристалла и пластинки, составляет 30х30 мм2 участка кристалла.
На топограммах, полученных методами Берга – Барретта и Ланга, деформированные области кристалла дают изображения повышенной интенсивности за счет уменьшения влияния первичной экстинции. Первичная экстинции – ослабление интенсивности рентгеновских лучей, происходящее в пределах одного блока.
Метод Ланга позволяет получать также стереопары топограмм, выявляющие объемное расположение дефектов.
К этой же группе методов относится метод аномального прохождения (Боррмана), применяемый для изучения дефектов в «толстых» кристаллах (μt > 1). Геометрия метода аналогична схеме Ланга, однако используется широкий падающий пучок без разделения Кα1- α2 дублета от трубки с линейчатым фокусом.
Сущность аномального прохождения в аномально малом коэффициенте поглощения рентгеновских лучей в совершенных кристаллах, находящихся в отражающем положении. Явление лучше всего иллюстрируется моделью волнового поля. Если плоская монохроматическая волна входит в пластинку совершенного кристалла, образуются две стоячие волны. Узловые плоскости одной из волн (А) совпадают с положением семейства плоскостей решетки (hkl), в то время как для другой (В) они находятся на половине расстояния между ними. Полагая атомы точечными центрами поглощения, а кристалл достаточно толстым, можно считать, что волна В вскоре совершенно поглотится благодаря ее сильному взаимодействию с атомами, тогда как волна А пройдет через кристалл, сохраняя полную интенсивность независимо от ее толщины. Однако интенсивность очень сильно зависит от степени совершенства кристалла. Нарушения периодичности уменьшают интенсивность волны А, на чем и основана регистрация их отображения на топограммах в виде светлых полос.
Идентификация дефектов и, в частности, определение вектора Бюргерса производится, как и в методе Ланга, по правилу фазового контраста.
Максимальная эффективность методов рентгеновской топографии достигается путем визуализации рентгеновской увеличенной картины на телеэкране.
К третьей группе методов относятся наиболее чувствительные методы двухкристальной и муаровой топографии. Картину полос интерференции двух рентгеновских полей, полученных в результате дифракции одновременно от пары кристаллов, называют рентгеновским муаром.
В методе двухкристальной топографии отражение плоскости обоих кристаллов параллельны или антипараллельны.
В методе муаровой топографии муаровая картина возникает при прохождении поля через исследуемый кристалл, установленный непосредственно за первым. При этом параметры двух решеток либо различны, либо имеют относительный разворот. В другом варианте метода муаровой топографии из исследуемого кристалла изготавливается рентгеновский интерферометр, представляющий собой монолитный блок с тремя отражающими частями.
Тема 4:Рост кристаллов
В основе современной классификации методов выращивания монокристаллов лежит способ создания оптимальных условий кристаллизации. Условия – это прежде всего, движущая сила кристаллизации и поведение ее во времени, которое определяет скорость выращивания кристалла и степень ее стабилизации, форму фронта кристаллизации; это исходная шихта, величина и время перегрева расплава (раствора), характер и скорость его перемешивания, природа атмосферы кристаллизации, ориентировка затравочного кристалла.
Под методом понимают ряд отличительных признаков техники выращивания кристаллов: необходимость использования контейнера для удержания расплава (раствора), его конфигурация, тип источника нагрева, положение и направление фронта кристаллизации относительно зеркала расплава и т.п.
Лекция 1.Основные принципы технического выращивания монокристаллов
1) Введение
Процессу выращивания монокристаллов предшествует большая подготовительная работа: 1) очистка исходного сырья; 2) подбор легирующей примеси; 3) приготовление расплава, раствора и т.п., фиксирование рН среды; 4) подбор состава среды, в которой происходит кристаллизация (вакуумированной, инертной, водородной и т.п.); 5) выращивание или приготовление затравочных кристаллов необходимой формы и достаточной степени совершенства; 6) выбор материала сосуда (в частности, тигля), в котором происходит кристаллизация; 7) монтаж затравочных кристаллов; 8) подготовки и перемешивание раствора или расплава; 9) выбор нагревательного устройства (печи); 10) обеспечение правильного отвода тепла; 11) выбор устройства для равномерного относительного перемещения кристалла в печи; 12) стабилизация и управление температурой кристаллизации; 13) учет и использование закона геометрического отбора; 14) борьба с посторонними кристаллами («паразитами»); 15) обеспечение стерильности на всех этапах подготовки и проведение процесса кристаллизации; 16) извлечение выращенных монокристаллов.
Вышеперечисленные пункты должны быть умело учтены для успешного решения задачи получения кристаллов, отвечающих определенным требованиям.
К настоящему времени разработано много различных методов выращивания кристаллов из расплавов в условиях изменения температуры при неподвижном тигле (метод Киропулоса, метод Штебера и Стронга и др.); перемещения кристалла в температурном градиенте (метод Чохральского); перемещения тигля или печи в температурном градиенте (метод Обреимова – Шубникова – Бриджмена – Стокбаргера – Степанова); бестигельные методы (метод Вернейля) и, наконец, методы зонной кристаллизации как тигельные, так и бестигельные.
В основе классификации методов выращивания кристаллов из растворов лежит способ задания пересыщения, в связи с чем различают метод кристаллизации путем изменения температуры раствора в динамическом и статическом режимах, метод испарения растворителя, кристаллизацию при тепловой конвекции раствора, в частности гидротермальный метод, электрокристаллизацию и др.
Кристаллизация из парообразного состояния получают сравнительно совершенные кристаллы, но чаще эпитаксиальные пленки. Известно несколько приемов получения кристаллов из газовой фазы: путем сублимации данного вещества, метод химических реакций в газе и химических транспортных реакций.
Кристаллизацией вещества из твердого состояния пользуются значительно реже, чем кристаллизацией из жидкого состояния; отчасти поэтому методы перекристаллизации вещества менее разработаны. Выгодное исключение составляет метод собирательной рекристаллизации и метод рекристаллизации обработки, т.е. рекристаллизации предварительно деформированного поликристаллического образца.
В последнее время особым вниманием пользуются способы получения кристаллов из паров, жидкостей и твердого вещества путем химических реакций. Обыкновенно кристаллический осадок выпадает в виде порошка из очень мелких кристаллов. Однако если замедлить реакцию, то последующие порции выделяющегося вещества осаждаются на уже готовые кристаллики, и последние будут расти.
Различные процессы кристаллизации имеют больше общего, чем это может показаться на первый взгляд. Благодаря общим чертам процессов кристаллизации современным методам придается характер большой универсальности, которая достигается путем комбинации различных методик выращивания.
2) Методы очистки исходного материала и легирование
1. Методы очистки вещества
Разработано большое число методовочистки вещества. Одни из них не сопряжены с изменением химического состояния вещества. Сюда обычно относятся: процессы перегонки, возгонки (сублимации), испарения и фильтрации. К этой группе методов очистки относится и метод зонной плавки. Все они используются для очистки как простых веществ, так и неорганических и органических соединений.
Вторая группа включает методы очистки растворов. Хорошо растворимые в жидкостях твердые тела очищают путем многократного растворения с последующей кристаллизацией. К этой группе относятся: метод адсорбционного соосаждения из раствора, хроматографические методы, метод экстракции несмешивающимся растворителем.
Третью группу составляют «химические» методы, основанные на различной химической активности примесей.
Часто элементы или соединения, которые нельзя очистить непосредственно, переводят в какое-нибудь промежуточное состояние. Последнее подвергают очистке и в дальнейшем восстанавливают до исходного элемента. Промежуточное состояние может оказаться менее тугоплавким, химически не столь активным, как исходные элементы. Очень часто в качестве промежуточных состояний используются галогениды.
Перегонка и возгонка. В методах перегонки и возгонки используются разности давления паров примеси и основного вещества. Для практического осуществления их («фракционной перегонки») служат фракционные колонки. Пары кипящей жидкости поступают в колонку, где происходит их конденсацияс последующим многократным испарением. В результате чистое вещество с наивысшим давлением пара доходит до вершины колонки, где оно конденсируется и отбирается.
Эффективность перегонной колонки высока, в ней можно разделять жидкости с разностью температур кипения менее 1 оС.
Более тугоплавкие вещества очищают путем многократной возгонки или испарения в специальном устройстве. При выборе надлежащего положения и температуры нагревателя возгоняемое или испаряемое вещество перемещается вдоль трубки. Процесс ведут в токе инертного газа при атмосферном давлении, иногда в вакууме.
Фильтрация. Вещество плавится в воронкообразном тигле с очень маленьким донным отверстием. Шлак собирается на поверхности, а расплав вытекает через спускное отверстие. Фильтрацию лучше проводить в атмосфере водорода или инертного газа, повторяя ее несколько раз. Такой процесс фильтрации предшествует введению вещества в трубки для зонной плавки.
Очистка растворением. Элемент или соединение растворяют в подходящем растворителе, после чего раствор очищают от примесей. Простейший способ очистки – перекристаллизация. Образующиеся кристаллы исходного вещества отделяют от раствора фильтрованием.
Часто перед кристаллизацией элементы переводят в растворимое соединение. Из раствора их можно извлечь электроосаждением или с помощью химической реакции.
Перекристаллизация. Широко используется для очистки как неорганических, так и органических веществ. В основе перекристаллизации лежит способность растущего кристалла вытеснять примеси. Путем многократной перекристаллизации можно довести вещество до высокой степени чистоты. Наибольшее значение приобрел разработанный Пфанном метод зонной плавки.
Хроматография. Применяются несколько видов хроматографии: адсорбционная, распределительная, ионообменная, газовая и др.
Адсорбционная хроматография основана на использовании селективного взаимодействия основного вещества с какими-либо другими веществами. Это взаимодействие позволяет проводить разделение с использованием подобранных растворителей. Растворитель должен обеспечивать «распределение» или относительную адсорбцию растворенного вещества между неподвижной твердой фазой и самим растворителем.
В распределительной хроматографии распределение растворенного вещества происходит между двумя жидкостями, а не между твердой и жидкой фазами, как в адсорбционной хроматографии.
В ионообменной хроматографии в качестве неподвижной фазы применяются ионообменные смолы, которые составлены из крупных полимерных молекул, синтезируемых из органических молекул с кислотными и основными боковыми группами. Простой пример использования ионообменных смол – получение дистиллированной воды.
В методе газовой или парофазной хроматографии основную роль играет распределение между подвижной газовой или паровой фазой и неподвижной жидкостью. Последняя удерживается в колонке на подходящем адсорбенте, а исходное вещество поступает в колонку в виде пара и обычно в смеси с инертным газом.
Адсорбционное осаждение. В методе используется большая адсорбционная способность поверхности свежеобразованного осадка. Осадок адсорбирует ионы на своей поверхности и тем самым выделяет их из раствора. Природа адсорбированных ионов определяется природой осадка и состоянием раствора.
Жидкостная экстракция. Смесь двух веществ, находящихся в одном растворителе, часто можно разделить, экстрагируя одно из них другим растворителем, не смешивающимся с первым.
Электролитические методы. Принцип этих методов разделения или очистки главным образом металлов хорошо известен. В электролит опускаются два электрода: катод-пластинка чистого металла и анод-неочищенный металл. Электролитом служит раствор с ионами того же металла. При пропускании тока происходит растворение анода и эквивалентное осаждение металла на катоде. Вещества с более высоким потенциалом выделения остаются в растворе.
Электролитические методы пригодны и для очистки растворов от следов примесей. Примеси собирают либо на платиновой фольге, либо на поверхности жидкой ртути, используемых в качестве катода.
Химические методы –выщелачивание химическими реагентами, реакции замещения. В последнем случае происходит вытеснение одного элемента другим, регулируемое электроотрицательностью и другими показателями.
Химическими можно назвать диффузионные методы, в которых удаление примесей осуществляется нанесением на поверхность твердого тела или приведением в тесный контакт с ним такого вещества, которое при нагревании взаимодействуют с диффундирующими на поверхность примесями, образуя с ними химические соединения.
Специальные методы. Один из наиболее сложных процессов – разделение изотопов. Чаще всего для этого используются масс-сепаратором. Заряженные частицы разделяются в электрическом и магнитном полях путем отклонения – разветвления их путей, которое строго следует отношению е / m.
Разделение изотопов осуществляется также с помощью термодиффузии и центрифугирования.
Очистка обычных газов. По возможности очистку потока газа лучше вести с помощью не химических, а физических процессов во избежание его загрязнения.
Следует иметь в виду, что методы очистки становятся «уверенными», когда их эффективность надежно контролируется аналитическими методами. Определение примесей, концентрация которых требует порядка 10-10 атомных долей, производится специальными методами: методом меченых атомов, чувствительность которого достигает 10-11 %, масс-спектрометрическим (10-8 %). Для этой цели улучшены давно существующие методы определения концентрации примесных атомов.
2. Легирование
После того как получен чистый материал, если это необходимо, его подвергают легированию, которое осуществляется двумя способами. Первый – это легирование заранее приготовленного монокристалла, т.е. сначала из чистого материала выращивают монокристалл, а затем вводят примесные элементы. Второй способ заключается в выращивании кристаллов непосредственно из среды, содержащей необходимое количество нужных примесных элементов. При легировании кристаллов в процессе их выращивания важно получить кристаллы с однородным распределением примесей, т.е. предотвратить сегрегацию. Способы решения такой проблемы зависят от методов выращивания кристаллов.
Введение примесных атомов в готовый кристалл осуществляется тремя способами. Наиболее часто кристалл приводят в контакт с другой фазой (твердой, жидкой или газообразной), содержащей необходимые примеси, которые затем проникают в кристалл благодаря диффузии. Этот метод применяется для тонких кристаллов. Так, медь в монокристаллы германия вводится нагреванием их в контакте с жидким сплавом, содержащим медь.
Второй способ введения примесных атомов в тонкий поверхностный слой готового кристалла состоит в том, что последний подвергают бомбардировке соответствующими ионами.
Третий способ легирования готового кристалла – ядерные реакции. Кристалл облучается α – частицами или нейтронами.
3) Аппаратура для нагрева, измерения и поддержания температуры
1. Источниками нагрева в аппаратуре для выращивания монокристаллов служат разнообразные печи сопротивления. Наиболее широкое распространение получили трубчатые печи.
Огнеупорную трубу с намотанным на нее нагревательным элементом в виде проволоки или ленты засыпают слоем теплоизолирующего материала соответствующей толщины. Т.о., печь представляет собой многослойный цилиндр (рис. 4.1).
При расчете простой печи ее тепло Q суммируется из полезного тепла и вспомогательного за вычетом потерь тепла за время t:
QПЕЧИ = QПОЛ + QВСПОМ – QПОТЕРЬt (4.1)
где QПОЛ = ∑g С (Т2 – Т1);
QВСПОМ = ∑gi Сi (Т2 – Т1);
g – вес нагревателя; С – теплоемкость материала нагревателя; gi – вес футеровки (металлического вкладыша); Сi – теплоемкость материала; Т – температура.
 (4.2)
(4.2)
где L – длина печи (трубы); D1, D2, D3, D4 – соответственно диаметры печи, обмотки, слоя тепловой изоляции, рубашки; λ1, λ2, λ3 – коэффициенты теплопроводности материала футеровки, обмотки и изолятора.
 По достижении необходимой температуры Т2 подвод мощности Р к печи должен быть отрегулирован так, чтобы потери тепла в точности возмещались подводимой мощностью. Практическая мощность, потребляемая печью, определяется именно через QПОТЕРЬ:
По достижении необходимой температуры Т2 подвод мощности Р к печи должен быть отрегулирован так, чтобы потери тепла в точности возмещались подводимой мощностью. Практическая мощность, потребляемая печью, определяется именно через QПОТЕРЬ:
 (4.3)
(4.3)
где К – переводной коэффициент.
Потребляемая мощность тем меньше, чем медленнее разогрев и чем лучше термоизоляция. Тепловой поток, идущий от нагревателя внутрь печи, меньше обратного. Величина Q* равна:
 .
.
Удельная поверхностная мощность нагревателя W (мощность рассчитанная на 1 см 2) определяется формулой:
 (4.4).
(4.4).
Для проволочного нагревателя:
 , (4.5)
, (4.5)
где d – диаметр проволоки; h – шаг намотки. Имеются таблицы рассчитанных поправок  .
.
Чем больше W, тем в более жестких условиях способна работать печь.
Далее можно преступить к расчету всех других параметров:
 кВт , (4.6)
кВт , (4.6)
где U – напряжение, поступающее из трансформатора; R – сопротивление;
 мм, (4.7)
мм, (4.7)
где d – диаметр обмотки; ρ – удельное сопротивление;
 м, (4.8)
м, (4.8)
где l – длина проволоки.
Обычно, определив мощность печи, выбирают материал для нагревательного элемента. Этот выбор определяется температурой, необходимой для эксперимента. Для температур до 1250 оС можно пользоваться нихромом, до 1500 оС – платиной, а до 2500 оС – молибденом или вольфрамом. Однако работать на максимальных режимах не рекомендуется. Поскольку молибден и вольфрам при нагреве легко окисляются, то их можно использовать только в инертной атмосфере или в вакууме. Питание для них подается через мощный понижающий трансформатор.
Трубы, приготовленные из кварца, годятся для нагрева до 1100 оС; до 1500 оС можно применять алюмосиликатные трубы; до 1900 оС служат трубы из чистого глинозема, а до 2200 оС - из двуокиси циркония и двуокиси тория.
Наматывается лента на трубу либо вручную, либо на токарно-винторезном станке. После укрепления обмотки ее обмазывают огнеупорной смесью, предохраняющей витки от наползания друг на друга в процессе нагрева.
Чтобы избежать неравномерный нагрев печи, шаг обмотки должен быть небольшим, а обмотка – равномерной.
Существуют трубчатые печи сопротивления других типов: силитовые, графитовые. В них нагревательным элементом служит сама труба. Силитовые печи могут работать на воздухе до температуры 1350 оС. Графитовые печи в бескислородной среде выдерживают нагрев до 2600 оС. Питание к таким печам подводят через водоохлаждаемые латунные или стальные наконечники.
В другом типе печей нагревательный элемент представляет собой огнеупорный стержень с намотанной проволокой или лентой. Такими элементами, собранными в обоймы, обкладывают разогреваемый объем. В качестве объема для стержней наиболее пригоден пирофиллит. В зависимости от обстоятельств нагревательные элементы можно располагать внутри или вне печной камеры.
Теплоизоляция печей обеспечивается материалами с ячеистой структурой (здесь используется низкая теплопроводность неподвижного воздуха); огнеупорные кирпичи, брикеты и гранулы из асбестовой ваты или мелкой огнеупорной щебенки.
Роль теплоизоляторов играют также отражатели тепла в виде металлических поверхностей, полированных или покрытых алюминиевой фольгой.
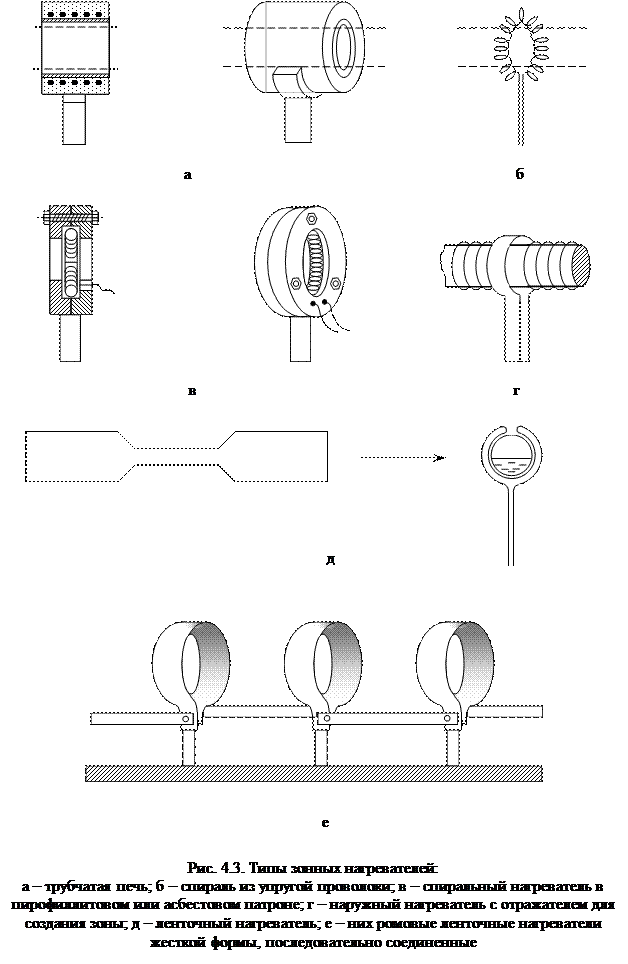
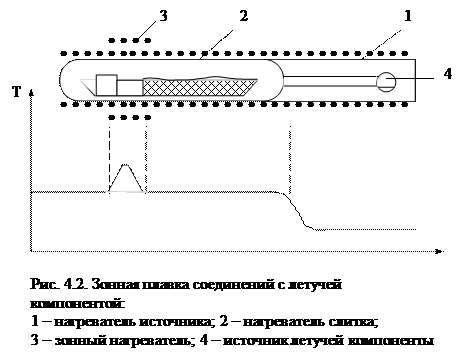 В ряде случаев используют вакуумные рубашки, особенно полезные там, где требуется обеспечить быстрый нагрев и устойчивое поддержание высоких температур. Естественное распределение температуры в трубчатых печах таково, что в центральной части она наибольшая, на концах – наименьшая. Чтобы подравнять температуру, вводят дополнительный нагрев на концах печи или делают неравномерный шаг намотки вдоль длины печи, иногда вводят местную дополнительную экранировку. В этих целях готовятсекционированные печи. На рис. 4.2 дана схема секционированной трубчатой печи с дополнительным зонным нагревателем, а также ее температурный профиль. На рис. 4.3 показаны типы дополнительных (зонных) нагревателей. Иногда в целях выравнивания температуры используют металлический вкладыш с высокой теплопроводностью (см. рис. 4.1).
В ряде случаев используют вакуумные рубашки, особенно полезные там, где требуется обеспечить быстрый нагрев и устойчивое поддержание высоких температур. Естественное распределение температуры в трубчатых печах таково, что в центральной части она наибольшая, на концах – наименьшая. Чтобы подравнять температуру, вводят дополнительный нагрев на концах печи или делают неравномерный шаг намотки вдоль длины печи, иногда вводят местную дополнительную экранировку. В этих целях готовятсекционированные печи. На рис. 4.2 дана схема секционированной трубчатой печи с дополнительным зонным нагревателем, а также ее температурный профиль. На рис. 4.3 показаны типы дополнительных (зонных) нагревателей. Иногда в целях выравнивания температуры используют металлический вкладыш с высокой теплопроводностью (см. рис. 4.1).
Печи сопротивления получили широкое распространение из-за их надежности, простоты оформления и широкого диапазона температур от комнатной до 3000 оС. Недостатком печей
накала является большая инерционность (для их охлаждения требуется около двух часов), опасность загрязнения кристалла со стенок печей и их плохая воспроизводимость.
Для долее высокого нагрева пользуются радиационной печью. Ее можно сделать в виде цилиндра (в идеальном случае в виде сферы), полированные стенки которого хорошо отражают падающее на них излучение. Разогрев обеспечивают нагревательным элементом в виде кольцеобразной обоймы из кварцевых или пирофиллитовых стержней, на которые натянута проволока. Образец и термопару размещают вблизи центра цилиндра. Для такой печи характерна низкая теплоемкость и высокая чувствительность к изменению мощности.
В последние годы все чаще используется аппаратура с индукционным, или высокочастотным, нагревом. При быстром изменении магнитного поля, пронизывающего нагреваемый объект, на поверхности последнего наводятся индукционные токи. Индукционные токи протекают преимущественно вдоль поверхности объекта и выделяемое тепло передается вглубь лишь за счет теплопроводности материала.
Индукционный, или высокочастотный, нагрев в аппаратурном оформлении не сложнее печей сопротивления. Преимущество такого нагрева и в том, что опасность загрязнения материала сводится к минимуму.
В ряде случав используются такие способы нагрева, как электрической дугой, создание сверхвысоких температур (более 15 000 оС) плазменным шнуром, нагрев катодными лучами и нагрев до 3500 оС фокусированным тепловым излучением (солнечные печи).
2. Во всех системах необходимо надежное измерение температуры, которое давало бы гарантию успеха в выращивании монокристаллов.
Для этой цели разработан ряд приборов: жидкостные термометры, пирометры.
Действие жидкостных термометров основано на свойстве жидкости расширяться при нагреве. В интервале измеряемых температур от –30 оС до + 600 оС используется ртуть,
от –300 оС до + 100 оС – толуол, от –80 оС до + 80 оС – этиловый спирт и др.
Общеизвестны ртутные контактные термометры, в которых нагревающаяся ртуть, расширяясь, поднимается по трубке, касается подвижного контакта и замыкает цепь реле, отключающего нагреватель. При остывании опускающаяся ртуть размыкает реле и электронагревательвключается. Для изменения контролируемой температуры достаточно поднять или опустить подвижный контакт в капиллярной трубке терморегулятора.
Действие термометров сопротивления основано на зависимости электросопротивления от температуры. Эти термометры определяют температуру с большой точностью. Используемые металлы должны иметь высокий температурный коэффициент удельного сопротивления  . Для большинства металлов α = 4·10-3 1/град, но на величину α влияют примеси. Желательно, чтобы зависимость сопротивления от температуры выражалась монотонной кривой (лучше - линейной). Металл должен быть химически стойким и сохранять свои характеристики неизменными.
. Для большинства металлов α = 4·10-3 1/град, но на величину α влияют примеси. Желательно, чтобы зависимость сопротивления от температуры выражалась монотонной кривой (лучше - линейной). Металл должен быть химически стойким и сохранять свои характеристики неизменными.
Наиболее широкое применение получили термопары. Они механически прочнее и просты в работе. Действие их основано на возникновении э.д.с. в местах контакта (спая) двух проводников различного состава и э.д.с. в проводнике, концы которого поддерживаются при разных температурах. Величина э.д.с. определяется природой металла и разностью температур между холодным и горячим спаями и не зависит от длины проводов. Для отсчета температуры существуют градуированные таблицы или кривые. Необходимо, чтобы температура свободных концов была равна той, при которой производится градуировка термопар. При градуировке холодный спай должен поддерживаться при температуре 0 оС.
Вообще говоря, для измерения температуры можно воспользоваться любой парой металлов, однако практически важным условиям – неизменности показаний во времени и воспроизводимости – удовлетворяют лишь немногие из них. Желательно также, чтобы величина возбуждаемой э.д.с. зависела от температуры линейно.
Широко используются термопары хромель-алюмелевые (ХА), хромель-капелевые, платино-платино-родиевые (ПП) и др.
Для высокотемпературных измерений можно воспользоваться оптическим пирометром. Действие его основано на изменении цвета излучения в зависимости от температуры. Ниже температуры 500 оС излучение находится за пределами видимости; тусклый красный цвет соответствует 600 оС; красный – 700 оС; светло-красный – 800 оС; вишнево-красный – 900 оС; оранжево-красный – 1000 оС; оранжевый – 1100 оС; белое свечение – выше 1600 оС. В большинстве случаев цвет исследуемого тела сравнивают с эталоном. Для этой цели изготавливаются специальные пирометры с исчезающей нитью.
3. В практике выращивания кристаллов особое значение придается поддержанию постоянства температуры печи. Стабильность температуры (максимальная ± 0,5 оС) наряду с другими условиями обеспечивает монокристальный рост, совершенство кристалла и его стехиометрический состав.
Колебания температуры печи могут вызываться непостоянством питающего напряжения, изменениями температуры окружающей среды, повреждениями обмотки или теплоизоляции печи. Если источник питания стабилизирован, то тем самым колебания температуры в печи в зависимости от типа стабилизатора не выходят за пределы ± 0,5 - ± 1 оС. В лучших стабилизаторах выходное напряжение второго трансформатора непрерывно и автоматически корректируется посредством специальной схемы.
Для обеспечения высокой точности поддержания температуры применяют следящие системы – устройства, в которых данные о температуре печи передаются питающему элементу. Если температура печи ниже заданной, то автомат усиливает подачу энергии; в обратном случае вся энергия или часть ее снимается. В качестве контролирующего элемента могут быть использованы термометры сопротивления или термопары. Эффективность регулирования температуры зависит от теплоемкости печи. Печь с очень большой теплоемкостью в малой степени реагирует на изменение температуры окружающей среды и более заметно, но медленно реагирует на изменения силового питания. Лучше всего такая печь работает при относительно низких температурах. Печь с очень малой теплоемкостью подвержена воздействию окружающей среды, но зато обладает быстрой реакцией и более пригодна для высокотемпературных процессов.
4) Материалы сосудов и тиглей
Сосуды, заключающие расплав, называют тиглями, лодочками. В ряде случае выращиваемый из расплава монокристалл принимает форму заключающего его сосуда.
К материалу тигля предъявляется ряд требований: 1) кристаллизуемое вещество не должно при соприкосновении с материалом тигля вступать с ним в химическую реакцию; 2) не должно прилипать к стенкам сосуда; 3) материал тигля не должен размягчаться при температуре, превышающей примерно на 100 оС температуру плавления кристаллизуемого вещества; 4) теплопроводность тигля желательна по возможности большая, но не должна превышать теплопроводность кристаллизуемого вещества; 5) упругость паров материала тигля должна быть в условиях кристаллизации не очень высокой, в противном случае срок службы тигля будет исчисляться немногими часами; 6) чистота тигля не должна уступать чистоте кристаллизуемого вещества.
Для изготовления тиглей чаще всего используют плавленый кварц, стекло, платину, графит, окись алюминия, тугоплавкие окислы (окись бериллия, окись магния, двуокись циркония, двуокись тория), сталь, молибден и другие тугоплавкие металлы, огнеупорные материалы.
Весьма распространен в качестве тигельного материала плавленый кварц. Он инертен к большей части элементов и соединений. Исключение составляют основные окислы и фториды. Кварц выдерживает нагрев до 1200 оС. Чрезвычайно малый коэффициент расширения обеспечивает его хорошую термическую стойкость. Толстостенные кварцевые тигли выдерживают давление до 10 атм. Кварц вообще очень чистый материал: лучшие сорта содержат лишь десятитысячные доли процента натрия, кальция, алюминия, фосфора, мышьяка, бора и иногда железа, меди и кобальта. Поверхность кварца легко сделать чистой и гладкой. Важнейшее преимущество плавленого кварца в том, что ему можно придать самую разнообразную форму, обеспечивающую при необходимости полную герметизацию всей системы.
Кварц не взаимодействует со всеми обычными кислотами, за исключением плавиковой, но энергично реагирует с концентрированными щелочами, поэтому в контакте со щелочными веществами его применять не следует. Некоторые расплавленные металлы сильно прилипают к кварцу, однако смачивание металлов можно ослабить, если кварц покрыть слоем сажи. Так, кварцевую лодочку часто покрывают сажей, выдерживая ее в коптящем пламени бензола или парафинового воска. Аналогичные результаты можно получить споласкиванием трубки в ацетоне или спирте с последующим нагреванием до 600 – 700 оС. Органическое вещество, сгорающее при ограниченном доступе воздуха, образует тонкий, но очень стойкий и прочно удерживаемый слой углерода. Для футеровки кварцевых тиглей также применяют графитовый порошок. Любое расширение передается слою графита, легко деформирующемуся вследствие своей мягкости.
Стекло – тоже широко распространенный тигельный материал. Ему легко придать нужную форму, из него изготовляют полностью закрытые сосуды. Стекло прочнее кварца, но размягчается при более низкой температуре. Боросиликатные стекла, например пирекс, из которых обычно изготовляют жароустойчивую лабораторную аппаратуру, размягчается уже при температуре 600 оС. Большой недостаток стекла в его значительной загрязненности, некоторые из его примесей переходят в обрабатываемые вещества. Кроме того, при нагревании стекла из него выделяется вода. Боросиликатное стекло, содержащее 96 % двуокиси кремния и почти 4 % окиси бора, называется викором. По своей прочности и теплостойкости оно родственно кварцу, но имеет более низкую температуру размягчения.
Из благородных металлов чаще других применяется платина. Ее преимущество в стойкости и механической прочности. Платину можно нагреть на воздухе до 1500 оС без какого-либо разрушения. Она инертна к галогенидам и окислам, но не в восстановительной атмосфере. Платина взаимодействует с большей частью расплавленных металлов, а также с серой, селеном, теллуром, фосфором, мышьяком и сурьмой в расплавленном состоянии.
В качестве тигельного материала очень удобен графит. Он инертен ко всем расплавленным металлом, за исключением алюминия, бора, кремния и германия. В отсутствие кислорода он применим вплоть до 2500 оС. Графит очень удобно нагревать индукционно или непосредственно током. Он обладает высокой термостойкостью. Пористость графита зависит от способа производства, однако выпускаемый в настоящее время графит вакуум не удерживает.
Окись алюминия (глинозем) используется для нагрева до 1850 оС. Из нее изготавливают вполне вакуумноплотную посуду с очень гладкой поверхностью. По механическим свойствам глинозем уступает кварцу, в частности у него более высокий коэффициент теплового расширения. Чистота сортовой технической окиси алюминия обычно около 99,8 %. Глинозем стоек в отношении металлов и может быть использован в контакте со щелочными металлами. Будучи устойчив по отношению ко всем кислотам, окись алюминия легче взаимодействует с едкими щелочами. С окислами металлов она взаимодействует при температурах выше 800 оС. Глинозем более порист, чем кварц.
В настоящее время широко применяются в качестве тигельного материала тугоплавкие окислы: окись бериллия, окись магния, двуокись циркония и двуокись тория. Они выдерживают более высокий нагрев, чем окись алюминия (некоторые из них до 2400 оС). По сравнению с окисью алюминия они обычно более пористы, особенно окись бериллия. По способу приготовления изделий, механических и термических свойств и чистоте все они близки к окиси алюминия. Окись бериллия («сладкозем») чрезвычайно ядовита, поэтому с ней следует обращаться осторожно.
Лекция 2.Выращивание монокристаллов из растворов
1) Введение
Формы роста кристаллов из растворов усложняются ввиду присутствия растворителя, играющего роль примеси.
Все методы выращивания монокристаллов из растворов основаны на использовании зависимости концентрации с вещества в растворе от термодинамических параметров, определяющих состояние системы:
с = f (p, T, c`) (4.9)
где с` - концентрация «вспомогательных» веществ, которые в случае многокомпонентной системы могут находиться в растворе. Величиной пересыщения можно управлять, изменяя по уравнению (4.9) концентрацию с.
Способы задания пересыщения (движущей силы кристаллизации) различны. Если пересыщение создается изменением температуры или испарением растворителя, то такие условия кристаллизации называют нестационарными. Кривые растворимости позволяют сделать выбор целесообразного метода выращивания монокристаллов данного вещества. Поэтому, приступая к выращиванию кристаллов какого-либо вещества, необходимо иметь кривую его растворимости и на ней основывать технические расчеты кристаллизации.
Если пересыщение создается тепловой или концентрационной конвекцией раствора, а также вынужденной конвекцией или путем химической реакции в условиях встречной диффузии вещества, то такие условия кристаллизации называются стационарными. Гидротермальный метод представляет собой пример кристаллизации в стационарных условиях.
У растворов метастабильная область значительно уже, чем у расплавов; она еще более сужается при хорошем перемешивании растворов. Вероятность возникновения зародышей возрастает, эта возможность зависит и от количества пересыщенного раствора за счет спонтанного образования флуктуациями энтропии. Поэтому большое количество раствора в метастабильном состоянии для выращивания больших монокристаллов можно сохранить при малом пересыщении, которое восполняется по мере надобности непрерывной подачей небольших количеств пересыщенного раствора (подпиткой).
Типичными дефектами для кристаллов, полученных из растворов, всегда будут включения маточной среды, но в них ниже плотность дислокаций, угол разориентации блоков не превышает первые единицы минут.
2) Построение кривой растворимости
Под растворимостью принято понимать максимальное количество вещества (предельная концентрация), способное раствориться при данных условиях в определенном количестве растворителя. Растворимость зависит от природы растворителя и растворенного вещества и от термодинамических условий растворения.
Способы выражения концентрации – величины, характеризующей количество данного вещества в растворе, - различны. Наиболее распространено и принято в большинстве справочников по растворимости солей выражение в весовых процентах (вес.%), т.е. число граммов растворимого вещества в 100 г раствора.
Концентрацию раствора обычно определяют косвенными методами, например измерением удельного веса или показателя преломления раствора. Пересчитав результаты по соответствующим таблицам, далее, по графику или по таблице растворимости находят, при комнатной температуре раствор данной концентрации становится насыщенным. Но такое определение неточно. Для прямого установления температуры насыщения используется явление концентрационных потоков, которое позволяет определить температуру насыщения раствора с точностью иногда до 0,1 оС.
Сущность метода концентрационных потоков, предложенного А.Н. Ковалевским, заключается в том, что о состоянии раствора судят по направлению концентрационных потоков, возникающих благодаря изменению плотности среды вокруг кристалла, который помещен в собственный раствор. Нисходящие от кристалла концентрационные потоки указывают на его растворение. Восходящие от кристалла потоки характерны для пересыщенного раствора (метастабильная область), когда кристалл растет. В насыщенном растворе, отвечающем, например, точке Д на кривой растворимости (см. рис. 1.1), устанавливается динамическое равновесие, исключающее концентрационные потоки.
Для определения tН раствора данной концентрации нагревают (охлаждают) раствор до ненасыщенного состояния и, далее, поместив в него кристаллик соли, растворимость которой исследуется, медленно охлаждают (нагревают), отмечая температуру t1, при которой исчезают нисходящие потоки растворения кристалла. Продолжая постепенно охлаждать раствор, находят температуру появления потоков роста t2. Среднее арифметическое 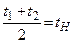 представляет собой температуру, в значительной мере приближающуюся к истинной температуре насыщения раствора.
представляет собой температуру, в значительной мере приближающуюся к истинной температуре насыщения раствора.
Для построения кривой растворимости с = f (t) необходимо около десятка точек. Фиксация каждой требует приготовления раствора соответствующей концентрации и, следовательно, для снятия всей кривой растворимости необходимо около десятка порций растворов, которые проще всего получить разбавлением исходного концентрированного раствора. Если m вес.% - отношение веса твердого вещества к весу всего раствора, а – вес всего раствора, b – вес твердого вещества, то х – количество растворителя, нужное для получения разбавленного раствора n вес.%, будет:
 .
.
3) Технический расчет кристаллизации
Кривая растворимости с = f (t) выбранного вещества и уравнение баланса массы:
 (4.10)
(4.10)
лежат в основе технического расчета кристаллизации, предшествующего процессу кристаллизации. В форму (4.10)  - масса вещества, отложившаяся на кристалле; dc – убыль пересыщения раствора. Первая равна:
- масса вещества, отложившаяся на кристалле; dc – убыль пересыщения раствора. Первая равна:
 ,
,
где ρ – плотность вещества; λi – нормальная скорость роста i-той грани; Si – ее поверхность; t – время. Вторая равна:
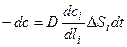 ,
,
где  - градиент концентраций у i-той грани; D – коэффициент диффузии; li – расстояние, на которое переместилась грань по нормали.
- градиент концентраций у i-той грани; D – коэффициент диффузии; li – расстояние, на которое переместилась грань по нормали.
Имея кривую растворимости, можно рассчитать: 1) необходимое количество растворителя и соли для получения кристалла желаемого веса, если кристаллизация происходит в интервале изменения температур (t2 – t1); 2) вес кристалла, который можно получить из данного объема раствора при изменении температуры от t2 до t1; 3) количество растворенного вещества, переходящего в кристаллическую фазу из данного объема раствора при изменении температуры на доли градуса от заданной.
4) Кристаллизация путем изменения температуры в водных растворах
В этом методе пересыщение достигается путем непрерывного изменения температуры во всем объеме кристаллизатора.
Подавляющее большинство веществ характеризуется прямой зависимостью растворимости от температуры. Для них пересыщение создается снижением температуры.
Любая кристаллизационная установка, используемая для выращивания кристаллов из водных растворов в динамическом режиме, состоит из следующих основных узлов (рис. 4.4): кристаллизатора с платформой для крепления кристалла – кристаллоносцем, блока питания всей установки и регулирования температуры, мешалки с электрическим приводом.
В изображенной установке нагревателем служит безынерционная печь с нихромовой обмоткой, холодильником-помещением, в котором производится кристаллизация. Блок терморегулировки состоит из реле, на которое поступают сигналы от контролирующей температуру контактного термометра. При замыкании и размыкании цепи контактного термометра реле соответственно включает или выключает нагреватель, поддерживая тем самым температуру кристаллизации вблизи заданного уровня. Изменение температуры в процессе роста кристалла производится подвижным контактом терморегулятора. Моторчик с мешалкой обеспечивает необходимое перемешивание раствора. Температура раствора измеряется
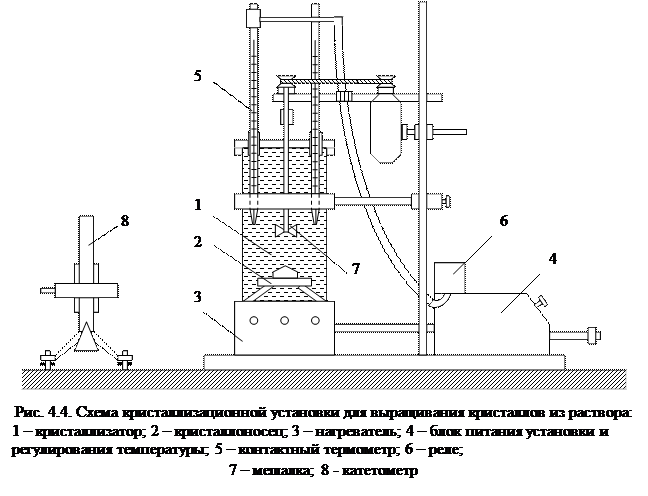 |
обычным термометром.
В учебных лабораторных условиях полезно использовать катетометр с вертикальной и горизонтальной шкалами и точностью отсчета по обеим нониусам 0,02 мм. Катетометр позволяет измерять линейные скорости роста кристалла без нарушения режима кристаллизации.
Затравкой может служить маленький (3 – 5 мм) ограненный кристаллик того вещества, раствор которого заполняет кристаллизатор. До начала кристаллизации производят микрометрический замер линейных размеров кристаллической затравки и рассчитывают ее активную поверхность и массу. Контролем правильности проведенного расчета служит взвешивание затравки. Затравка приклеивается парафином к платформе и помещается в пустой кристаллизатор. Приготовление насыщенного при задаваемой температуре раствора и определение его точки насыщения производятся в отдельной посуде по правилам, изложенным выше. Для расчета необходимого количества соли, насыщающего раствор, используется кривая растворимости данного вещества. Приготовленный раствор перегревается на несколько градусов выше точки насыщения и после получасовой выдержки осторожно, без разбрызгивания переливается в кристаллизатор, крышка которого, мешалка, контактный и ртутный термометры перед этим пропариваются для устранения возможных случайных центров кристаллизации. На герметической крышке затем устанавливаются термометры. Перемешивание раствора до полной регенерации затравочного кристалла не допускается.
Так как кристаллизатор, заполненный раствором, имеет цилиндрическую форму, то следует определить коэффициент искажения линейных размеров растущего кристалла, измеряя катетометром кажущийся диаметр стержня мешалки и относя полученную величину к известному размеру диаметра стержня.
За температурой раствора непрерывно ведется наблюдение.
Отмечают начало роста кристалла, наблюдая первые признаки регенерации кристаллической затравки (появление «шероховатостей», острых углов и плоских граней не ее поверхности.). Установив начало роста, прекращают понижение температуры, включая терморегулятор. После полной регенерации затравки (восстановление ее первоначальных размеров) соответствующим понижением температуры создают необходимое пересыщение раствора, допускаемое размерами поверхности кристалла и включают мотор перемешивающего механизма со скоростью 60 об / мин. Далее, через каждые 15 – 20 мин измеряют температуру и размеры кристалла. Очередное понижение температуры производят с учетом количества вещества, перешедшего в кристаллическую фазу, когда пересыщение раствора достигает половины от первоначальной величины.
Во время работы необходимо вести журнал наблюдений, в котором записываются все данные, относящиеся к подготовке и проведению кристаллизации.
Закончив кристаллизацию, вынимают платформу-кристаллоносец из раствора. Неиспользованный раствор переливают в чистый сосуд и герметически закрывают. Кристаллизатор и все детали установки, соприкасающейся с раствором, тщательно промывают теплой водой.
Пересыщенный раствор, из которого ведется выращивание, представляет собой неустойчивую систему, в которой велики шансы возникновения добавочных кристаллов-паразитов. Процесс образования их носит иногда лавинообразный характер: при трении их о дно и стенки сосуда и столкновении между собой возникают новые центры кристаллизации.
Вредность «паразитов» в том, что, питаясь за счет основного кристалла, они нарушают режим снижения температуры и образуют с основным кристаллом всевозможные сростки.
На практике все же можно создать условия, исключающие источники «паразитов». Прежде всего следует предохранить раствор от попадания зародыша извне, для чего на всех стадиях процесса подготовки к кристаллизации и ее проведения необходима полная чистота, а также герметичность загруженного кристаллизатора. Источником «паразитов» может стать сама затравка, вводимая в раствор. Чтобы избежать этого, затравочный кристалл предварительно обрабатывают, обтачивают мокрой тряпочкой неровные участки граней, его углы и ребра. Возникшая в результате такой обработки на поверхности кристалла тонкая кристаллическая пыль удаляется путем кратковременного опускания кристалла в теплую воду.
Облегчает образование «паразитов» наличие острых краев и выступов во всех предметах, соприкасающихся с раствором. Во избежание «паразитов» не следует допускать соприкосновения кристалла с предметами, имеющими весьма отличающиеся коэффициенты температурного расширения. Слишком быстрое движение кристалла при высоком пересыщении также приводит к возникновению «паразитов». Этому же всегда способствуют сильная вибрация и местные переохлаждения. В целях исключения источников «паразитов» следует пользоваться чистой солью и дистиллированной водой.
Особое внимание уделяется движению раствора и кристалла, необходимому для выравнивания разности пересыщения во весь период роста кристалла. Недаром динамические приемы выращивания кристаллов из растворов получили название скоростных методов выращивания сравнительно однородных кристаллов.
Известно, что монокристаллы растут по-разному при разных движениях кристалла или раствора. Поэтому для выращивания многих монокристаллов применяется реверсивное вращательное движение.
Впервые Г.В. Вульф пользовался вращающимися кристаллизаторами и приспособлениями с часовым механизмом, которые все время поворачивали кристалл и ставили тем самым различные его грани в одинаковые условия. В.Б. Татарским был впервые предложен способ планетарного движения самого кристалла.
На успешный рост кристаллов оказывает влияние также и скорость вращения. Последняя, в свою очередь, определяется формой кристаллоносца, вязкостью и количеством раствора, а также формой и размером вращаемых кристаллов. Очень важна правильно выбранная продолжительность перерыва между сменами направлений вращения оси, во время которой движущийся раствор медленно останавливается. Необходимо, чтобы при повторном разбеге мотора не происходило резких движений.
 Важнейшее значение в практике выращивания совершенных монокристаллов придается поддержанию и программному понижению температуры. При выращивании высококачественных кристаллов колебания температуры раствора должны быть минимальны. Такое сохранение температуры в данных пределах зависит от чувствительности применяемых регулировочных элементов, количества раствора и общего устройства кристаллизатора. Задача поддержания и программного понижения температуры успешно решается путем использования термостатов, куда помещаются кристаллизаторы с раствором и контактные термометры. Устройство и размер термостатов бывают самые разнообразные. Для заводского выращивания кристаллов сегнетовой соли применяется большой воздушный термостат – комната, вмещающая до нескольких десятков кристаллизаторов. Нагрев осуществляется сопротивлениями, расположенными в полу термостата. Температура регулируется автоматически системой контактных магнитных термометров. Движения руководящих магнитов контактных термометров управляются электронным импульсным датчиком при помощи шагового механизма. Этим путем достигается равномерное падение температуры на десятые доли градуса в сутки.
Важнейшее значение в практике выращивания совершенных монокристаллов придается поддержанию и программному понижению температуры. При выращивании высококачественных кристаллов колебания температуры раствора должны быть минимальны. Такое сохранение температуры в данных пределах зависит от чувствительности применяемых регулировочных элементов, количества раствора и общего устройства кристаллизатора. Задача поддержания и программного понижения температуры успешно решается путем использования термостатов, куда помещаются кристаллизаторы с раствором и контактные термометры. Устройство и размер термостатов бывают самые разнообразные. Для заводского выращивания кристаллов сегнетовой соли применяется большой воздушный термостат – комната, вмещающая до нескольких десятков кристаллизаторов. Нагрев осуществляется сопротивлениями, расположенными в полу термостата. Температура регулируется автоматически системой контактных магнитных термометров. Движения руководящих магнитов контактных термометров управляются электронным импульсным датчиком при помощи шагового механизма. Этим путем достигается равномерное падение температуры на десятые доли градуса в сутки.
Хорошие результаты дает способ достаточно быстрого выращивания, главным образом, затравочных кристаллов в статическом режиме. При нагревании приготавливается насыщенный раствор соли, который переливается в предварительно прогретый горячей водой цилиндрический сосуд Дьюара. В горячем растворе подвешивается кристалл. Сосуд плотно закрывают картонной крышкой с глубокими краями и помещают в бочонок или деревянный ящик, наполненный ватой или сухими древесными опилками (рис. 4.5). Чем лучше изолирован сосуд, тем медленнее охлаждение и тем более совершенным вырастает кристалл. Вскрывают ящик через несколько суток, кода температура раствора снизилась до температуры помещения.
5) Кристаллизация посредством испарения растворителя
Если вещество обладает малым к.т.р., то пересыщенные его растворы целесообразно получать путем испарения растворителя при постоянной температуре раствора. Испарение растворителя можно регулировать током сухого воздуха, который проходит над поверхностью раствора, увлажняется и удаляется через отверстие в крышке кристаллизатора. Выращивание кристаллов сернокислого лития Li2SO4 · H2 производится при высокой температуре (95 – 100 оС) из слабокислых растворов (рН 4,5 – 5). При этом используются термостатированные стеклянные кристаллизаторы емкостью около 9 л, схематически изображенные на рис. 4.6. Отвод конденсата осуществляется сифоном. Кристаллы выращивают с подпиткой – по мере слива конденсата добавляется свежий раствор. Для этого кристаллизатор соединяют с сосудом, из которого по принципу сообщающихся сосудов раствор непрерывно поступает в кристаллизатор. Подачу раствора необходимо вести плавно и в количествах, равных количеству сливаемого конденсата. Кристаллоносцем служит вертикальная ось из титана с ввинчивающимися в нее горизонтальными отростками, которая заканчивается цанговыми зажимами для укрепления стержневых затравок. Ось кристаллоносца проходит через укрепленный на крышке кристаллизатора стеклянный шариковый холодильник, служащий для возврата конденсата.
В кристаллизаторе на высоте 2 – 3 см укреплено ложное дно, в центре которого имеется отверстие диаметром около 5 см. Паразитические кристаллы отбрасываются движением раствора под ложное дно, где возможность их роста ограничена и они не мешают развитию основных кристаллов.
Удлинение затравки (4 – 5 см) совпадает с осью Z кристалла (рис. 4.6), а ее сечение для облегчения регенерации берется минимальным, обычно 3 мм.
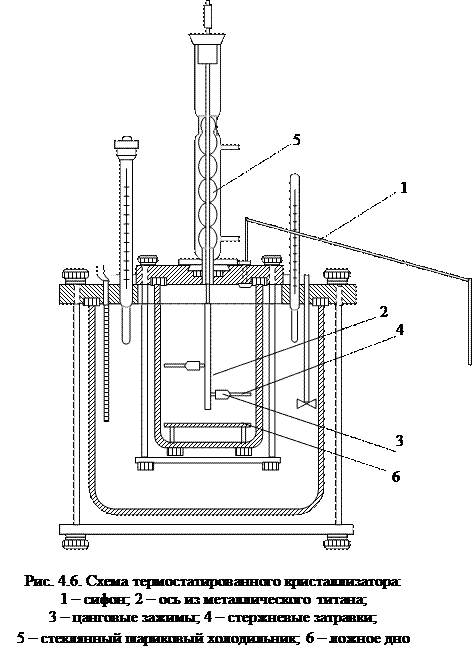 |
В собранный и нагретый примерно до 70 оС кристаллизатор заливают подогретый раствор сульфата лития в дистиллированной воде, подкисленной 0,5 – 1,5 г серной кислоты на 1 л раствора. Температура насыщения раствора (97 – 100 оС) определяется по плотности (1,213 – 1,214 г / см 3 ). Температура начала роста уточняется визуальным наблюдением за регенерацией затравок и поддерживается постоянной (± 0,2 оС) в течение всего цикла выращивания.
Исходя из размеров установленных затравок, габитуса кристаллов и заданной скорости их роста рассчитывается суточный график слива конденсата на весь цикл выращивания.
Выращивание производится со скоростью 3 мин / сут по оси y в обоих направлениях. По окончании выращивания раствор сливается и кристаллизатор медленно охлаждается до комнатной температуры, после чего снимают кристаллы. Т.о., за 40 – 60 сут получают кристаллы до 400 г. Выращиваемые динамическим методом ограненные кристаллы сульфата лития редко свободны от трещин, что нужно отчасти отнести за счет анизотропии скоростей роста различных граней.
Крупные, визуально однородные кристаллы сульфата лития без трещин возможно выращивать в форме ориентированных блоков. Получение таких кристаллов в вынужденной форме производится уже в статическом режиме. В качестве затравки используется пластинка, вырезанная параллельно одной из медленно растущих граней (100) кристалла. Она укладывается строго горизонтально на дно круглого стеклянного стакана и целиком его покрывает. В неподвижном растворе конвекционные потоки устремляются вверх от любой точки горизонтальной поверхности кристалла, непрерывно перемешиваясь на ней. В случае возникновения микровозвышений рост их тормозится восходящими потоками, который задерживается там до тех пор, пока соседние участки грани не догонят их в росте. Такой механизм роста позволяет получить визуально однородные кристаллы достаточно большого сечения и нужной формы из неперемешиваемых сильно пересыщенных растворов.
В практике выращивание совершенных монокристаллов исключительно важно качество затравочных кристаллов, с уменьшением размера которых ослабевает их влияние на качество выращиваемых кристаллов.
6) Кристаллизация при тепловой конвекции раствора. Гидротермальный метод.
Пересыщение раствора задается разностью температур между зонами растворения исходной шихты и роста кристалла. Вещество, помещенное в более нагретую зону, растворяется и конвекционными потоками переносится в менее нагретую область раствора. Здесь раствор, становясь п
Дата добавления: 2014-12-03; просмотров: 389; Мы поможем в написании вашей работы!; Нарушение авторских прав |