
КАТЕГОРИИ:
АстрономияБиологияГеографияДругие языкиДругоеИнформатикаИсторияКультураЛитератураЛогикаМатематикаМедицинаМеханикаОбразованиеОхрана трудаПедагогикаПолитикаПравоПсихологияРиторикаСоциологияСпортСтроительствоТехнологияФизикаФилософияФинансыХимияЧерчениеЭкологияЭкономикаЭлектроника
ПРИМЕРЫ ТИПОВЫХ ЗАДАЧ И ИХ РЕШЕНИЕ.
Задача 1. Определить степени окисления атомов всех элементов в соединениях: Cr2O3, K2Cr2O7, Ca3(PO4)2, NH4NO3.
При определении степеней окисления атомов следует руководствоваться следующим правилом: алгебраическая сумма степеней окисления всех атомов в молекуле вещества равна нулю, а в ионе – заряду иона. Для успешного решения подобных задач надо хорошо выучить элементы, у которых степень окисления атомов постоянна.
Решение.
Молекула Cr2O3 состоит из 3 атомов кислорода (степень окисления равна –2) и 2 атомов хрома (степень окисления неизвестна, х). Составляем уравнение: 2х+3(-2)=0, отсюда х=+3, получаем  .
.
В молекуле K2Cr2O7 известны степени окисления калия (+1) и кислорода (-2). Составляем уравнение: 2(+1)+2х+7(-2)=0, получаем х=+6,  .
.
В соединении Ca3(PO4)2 неизвестна только степень окисления фосфора. Однако в данном случае составлять уравнение, подобное предыдущему, не стоит. Ca3(PO4)2 – фосфат кальция, соль фосфорной кислоты, H3PO4, а в кислотах и их солях степень окисления основного элемента (в данном случае фосфора) одинакова. Поэтому для определения степени окисления фосфора составим более простое уравнение для кислоты, от которой образована соль (Н3РО4): 3(+1)+х+4(-2)=0, отсюда х=+5, получаем  .
.
В молекуле NH4NO3 (нитрата аммония, соли азотной кислоты) неизвестна степень окисления двух разных атомов азота, х и у (  ). Степень окисления азота “у” определяем так же, как в предыдущем примере, т.е. по формуле азотной кислоты, HNO3: 1(+1)+у+3(-2)=0; у=5.
). Степень окисления азота “у” определяем так же, как в предыдущем примере, т.е. по формуле азотной кислоты, HNO3: 1(+1)+у+3(-2)=0; у=5.
Степень окисления азота «х» определяем, зная, что ион аммония (NH4+) имеет заряд 1+: х+4(+1)=+1, отсюда х=-3. Получаем  .
.
Задача 2. Чему равен объем (н.у) сероводорода массой 8,5 г? Сколько молей и молекул H2S содержится в этой массе?
Известно, что 1 моль любого вещества имеет массу, называемую молярной массой, и содержит число Авогадро (NА=6,02·1023) молекул. Известно также, что если вещество является газом или паром, то при нормальных условиях (н.у.) объем его 1 моль равен 22,4 л.
Решение.
В данном случае имеем соотношение (А):
(А) 1 моль H2S – 34 г HzS – 22,4 л (н.у.) – 6,02 w23 молекул H2S. ¥ Введем обозначения:  - массаH2S,
- массаH2S,
 - объем H2S,
- объем H2S,
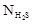 - число молекул H2S,
- число молекул H2S,
 - количество (число молей) H2S.
- количество (число молей) H2S.
Задачу можно решить двумя способами.
Дата добавления: 2015-04-11; просмотров: 229; Мы поможем в написании вашей работы!; Нарушение авторских прав |