
КАТЕГОРИИ:
АстрономияБиологияГеографияДругие языкиДругоеИнформатикаИсторияКультураЛитератураЛогикаМатематикаМедицинаМеханикаОбразованиеОхрана трудаПедагогикаПолитикаПравоПсихологияРиторикаСоциологияСпортСтроительствоТехнологияФизикаФилософияФинансыХимияЧерчениеЭкологияЭкономикаЭлектроника
Кондуктометрическое титрование
Кулонометрические методы основаны на измерении электрической проводимости веществ. Единицей электрической проводимости является проводимость проводника сопротивлением 1 Ом (в системе Си – сименс (См)). Электрическая проводимость раствора выражается в единицах или удельной, или эквивалентной электрической проводимости. Удельная электрическая проводимость χ измеряется в См/м и представляет собой электрическую проводимость 1 м3 раствора, находящегося между параллельными электродами площадью 1 м2 каждый при расстоянии между ними 1м.
В разбавленных растворах удельная электрическая проводимость с увеличением концентрации растет, при некоторой достаточно высокой концентрации достигает максимума и затем уменьшается. Это объясняется увеличением числа ионов с возрастанием концентрации, однако в концентрированных ионах возрастают силы межионного взаимодействия, увеличивается вязкость раствора, снижается скорость движения ионов, следовательно, уменьшается электрическая проводимость.
Для аналитических измерений обычно используется участок кривой с возрастающей удельной электрической проводимостью, т.е. область разбавленных и умеренно концентрированных растворов.
Эквивалентной электрической проводимостью называют проводимость раствора, содержащего 1моль эквивалента вещества и находящегося между двумя параллельными электродами, расстояние между которыми 1см. Её единицей измерения является См·см2/моль экв.
Удельная и эквивалентная проводимость взаимосвязаны соотношением:
 (27)
(27)
где с – молярная концентрация эквивалента, моль/л.
У сильных электролитов в области разбавленных растворов (0,001М и меньше) концентрационная зависимость проводимости выражается уравнением:
 (28)
(28)
где λ0 – предельная эквивалентная электрическая проводимость сильного электролита при бесконечном разведении; а – константа.
Константа а уравнения (28) объясняется теорией Дебая-Хюккеля, развитой Онзагером и связана с эффектами электрофоретического и релаксационного торможения.
Предельная эквивалентная электрическая проводимость λ0 может быть представлена суммой предельных электрических проводимостей или предельных подвижностей ионов:
 (29)
(29)
где λ0(+) и λ0(-) - предельная эквивалентная электрическая проводимость или предельная подвижность соответственно катиона и аниона.
Концентрационная зависимость электрической проводимости слабых электролитов имеет более сложный характер, чем у сильных электролитов.
Электрическая проводимость растворов с ростом температуры повышается. В водных растворах повышение составляет 2-2,5% на градус.
Токи, имеющие частоту порядка мегагерц и десятков мегагерц, называются токами высокой частоты. При таких частотах в растворе начинают играть роль эффекты молекулярной или деформационной и ориентационной поляризации. Поляризация молекул приводит к существенному изменению диэлектрической и магнитной проницаемости раствора, что открывает новую возможность исследования свойств раствора при титровании.
Промышленность выпускает комплектные приборы для определения электрической проводимость растворов – мосты переменного тока и кондуктометры.
Кондуктометрическое титрование. Экспериментально измеряемая величина сопротивления раствора зависит от размера электродов и расстояния между ними, а также от их формы и взаимного расположения, объема раствора и других факторов, не всегда поддающихся точному учету, так как токопроводящим является не только тот объем раствора, который заключен между электродами. Действительная электрическая проводимость раствора, не зависит от формы или взаимного расположения электродов или каких-либо других факторов, а определяется лишь концентрацией раствора, природой компонентов и температурой. Истинная электрическая проводимость раствора χ пропорциональна экспериментально измеренной величине χ, :
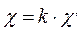 (30)
(30)
где k – константа сосуда.
Это очень важная характеристика ячейки. Она зависит от площади электродов, расстояния между ними, от формы сосуда и объема раствора, проводящего ток.
Измерение электрической проводимости растворов широко применяется в титриметрическом анализе для определения точки эквивалентности. В методах кондуктометрического титрования измеряют электрическую проводимость раствора после добавления небольших определенных порций титранта и находят точку эквивалентности графическим методом с помощью кривой в координатах χ – V (титранта). Практически в этом методе могут быть использованы такие химические реакции, в ходе которых достаточно заметно изменяется электрическая проводимость раствора или происходит резкое изменение электрической проводимости после точки эквивалентности.
Дата добавления: 2014-11-13; просмотров: 339; Мы поможем в написании вашей работы!; Нарушение авторских прав |