
КАТЕГОРИИ:
АстрономияБиологияГеографияДругие языкиДругоеИнформатикаИсторияКультураЛитератураЛогикаМатематикаМедицинаМеханикаОбразованиеОхрана трудаПедагогикаПолитикаПравоПсихологияРиторикаСоциологияСпортСтроительствоТехнологияФизикаФилософияФинансыХимияЧерчениеЭкологияЭкономикаЭлектроника
Структура периодической системы химических элементов.
Периодическая система химических элементов в короткой форме состоит из семи периодов – горизонтальных последовательностей химических элементов, расположенных по возрастанию заряда ядер, их атомов.
Атомы элементов одного периода имеют одинаковое число энергетических уровней (электронных слоёв), равное номеру периода и максимальному значению главного квантового числа n. Исключение составляет элемент 46Pd (палладий), атомы которого имеют четыре энергетических уровня, хотя расположен он в пятом периоде.

Каждый период (кроме первого) начинается элементом– щелочным металлом, атомы которого на внешнем энергетическом уровне имеют 1 электрон на ns-подуровне. Заканчиваются периоды элементам–благородными газами, атомы которых на внешнем уровне имеют энергетически выгодную, и поэтому устойчивую, электронную конфигурацию ns2np6.
Первый период начинается с элемента водорода, который в силу специфики свойств его атомов, помещают в первую и в седьмую группу. Этот период заканчивается элементом гелием, электронная конфигурация которого 1s2.
Закономерностью заполнения электронами энергетических уровней атомов объясняется различное число химических элементов в периодах, равное максимальному числу электронов на заполняемых подуровнях.
У атомов элементов первого периода заполняется единственный s-подуровень первого энергетического уровня, который имеет только одну орбиталь, и, следовательно, на нём может находиться всего 2 электрона. Поэтому первый период состоит только из двух s-элементов (H и He).
У атомов элементов второго и третьего периодов электроны могут занимать четыре орбитали: одну – s-подуровня и три – р-подуровня внешнего (соответственно второго и третьего) энергетического уровня. Поэтому второй и третий периоды состоят из двух s- и шести p-элементов.
В четвёртом и пятом периодах содержится по 18 химических элементов, так как заполняются, кроме четырёх орбиталей s- и p-подуровней внешнего (соответственно четвёртого и пятого) энергетического уровня, ещё пять орбиталей d-подуровня предвнешнего уровня, то есть (n – 1) d-подуровня. Поэтому эти периоды между s- и p-элементами содержат вставные декады 3d-и 4d элементов.
Следующие – шестой и седьмой – периоды ещё длиннее, так как в атомах их элементов, кроме девяти орбиталей ns-, nр- и (n – 1) d-подуровней, происходит заполнение электронами семи f-орбиталей предпредвнешнего уровня, то есть (n – 2) f-подуровня.
Шестой период имеет две вставки химических элементов: вслед за 6s-элементами расположена декада 5d-элементов, в которой после первого элемента – лантана, находятся 14 4f-элементов (лантаниды*). В итоге шестой период состоит из 32 химических элементов.
Аналогично построен и пока незавершённый седьмой период (25** химических элементов), в котором за первым 6d-элементом вставной декады – актинием, следуют 14 5f-элементов (актиниды***).
Свойства химических элементов закономерно изменяются в периодах при переходе от щелочных металлов к благородным газам. При переходе от одного периода к последующему число внешних электронов меняется скачкообразно.
По вертикали периодическая система подразделяется на восемь групп (I–VIII), объединяющих элементы, атомы которых имеют одинаковое число валентных электронов, равное номеру группы. И поэтому эти химические элементы характеризуются повторяемостью химических, физических и некоторых других свойств их атомов, а также образуемых или простых и сложных веществ.
Каждая группа делится на две подгруппы.
В главных подгруппах (А-группы) находятся элементы малых и больших периодов, в атомах которых происходит заполнение электронами внешнего энергетического уровня. Причём так, что число электронов на этом уровне равно номеру группы.
В побочных подгруппах (Б-группы) расположены элементы только больших периодов, в атомах которых электронами заполняется предвнешний энергетический уровень, а на внешнем уровне содержатся 1 или 2 электрона (у Pd – 0). Группа VIIIБ особая, она содержит триады химических элементов, составляющих семейства железа (Fe, Co, Ni) и платиновых металлов (Ru, Rh, Pd и Os, Ir, Pt).
Атомы элементов одной группы, но разных периодов отличаются друг от друга числом энергетических уровней (электронных слоёв). Сходство же их заключается в том, что вобразовании химических связей максимально может участвовать число электронов, равное номеру группы. В этом – физический смысл номера группы Периодической системы химических элементов Д.И. Менделеева.

Сходство химических элементов в подгруппах – наиболее заметная и важная закономерность в периодической системе. В атомах элементов побочных подгрупп (Б-групп) валентными являются электроны не только внешних, но и предвнешних электронных слоёв. И в этом заключаются основные различия в свойствах атомов элементов групп А и Б.
Пример. На каком основании элементы хлор и марганец помещены в одной группе, но в разных подгруппах Периодической системы химических элементов Д.И. Менделеева ?
Решение. Электронные формулы атомов хлора и марганца в основном состояниях таковы:
Cl – 1s22s22p63s23p5, Mn 1s22s22p63s23p63d54s2.
Валентные электроны атома хлора – 3s23р5, марганца – 3d54s2. Таким образом, эти элементы не являются электронными аналогами и не должны размещаться в одной подгруппе. Однако на валентных орбиталях их атомов в возбуждённом состоянии максимально может находиться одинаковое число электронов – 7.
Сl 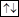
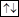


 Сl*
Сl* 







 3s 3p 3s 3p 3d
3s 3p 3s 3p 3d
Mn 




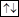
 Mn*
Mn* 








3d 4s 3d 4s 4p
На этом основании элементы хлор и марганец помещены в седьмую группу Периодической системы, но в разные подгруппы.
В зависимости от того, какой энергетический подуровень (s, p, d или f) в атоме заполняется электронами последним, различают s-, p-, d- и f-элементы.
s-Элементы – элементы главных подгрупп I и II групп (IA- и IIА-групп), а также элементы 1-го периода Н и He. Валентными электронами в атомах этих элементов являются электроны ns-орбиталей.
p-Элементы – элементы шести главных подгрупп III–VIII-групп (групп IIIA–VIIIA). Валентными электронами в атомах этих элементов являются электроны ns- и nр-орбиталей.
d-Элементы – элементы побочных подгрупп расположены в десяти столбцах восьми групп: IIIБ–VIIIБ, а также IБ и IIБ. В атомах этих элементов происходит заполнение электронами пяти орбиталей (n – 1) d-подуровня, то есть d-орбиталей предвнешнего энергетического уровня. Валентными электронами атомов этих элементов являются s-электроны внешнего энергетического уровня и, в большинстве случаев, d-электроны предвнешнего уровня. Поэтому атомы d-элементов в химических соединениях обычно проявляют переменную валентность. Например, атомы марганца проявляет валентности II, IV, VI, VII.
f-Элементы – это лантаниды и актиниды, в атомах которых идёт заполнение семи орбиталей (n – 2) f-подуровня, то есть f-орбиталей предпредвнешнего энергетического уровня. Валентными электронами в них являются ns-, а также (n – 1) d- и (n – 2) f-электроны.
После рассмотрения электронного строения атома становятся очевидными принципы построения Периодической системы элеменотов Д. И. Менделеева.
1. Элементы в периодической системе образуют последовательность, соответствующую возрастанию заряда ядер их атомных.
2. Каждый период начинается элементом, в атомах которого происходит заполнение электронами нового энергетического уровня.
3. Число электронов на внешнем энергетическом уровне равно номеру группы (это относится к А-группам). Так, атомы Li, Na, К и других элементов, расположенных в IA-группе, имеют по одному электрону на внешнем уровне. Атомы Be, Mg, Ca и других элементов IIА-группы имеют по два внешних электрона; а атомы F, C1, Вr и других элементов VIIA-группы содержат по семь электронов на внешнем уровне.
Таким образом, внешний энергетический уровень (электронный слой) атомов элементов одной подгруппы имеет равное число электронов. И он периодически повторяется с ростом заряда ядра атомов,элементов. А поскольку химические реакции осуществляются за счёт внешних электронов атомов элементов, то периодически повторяются и их химические свойства элементов. В этом заключается суть Периодического закона.
Итак, периодическая система Д. И. Менделеева является естественной классификацией элементов по электронной структуре их атомов, о которой судят по положению элемента в соответствующих периоде и подгруппе этой системы.
Для определения электронной конфигурации данного элемента атома используют:
· порядковый номер элемента, определяющий число протонов в его ядре, а также число электронов в его нейтральном атоме;
· номер периода, указывающий на число энергетических уровней и номер внешнего уровня в его атоме;
· номер и тип группы (А или Б), которые указывают, к какому типу (s, p, d или f) относится данный элемент и сколько электронов в его нейтральном атоме содержится на заполняемом энергетическом подуровне, а также на внешнем и предвнешнем энергетических уровнях.
Число электронов на внешнем энергетическом уровне нетрального атома равно: номеру группы – для атомов s- и р-элементов, или двум – для атомов d- и f-элементов с электронной конфигурацией ns2 (исключение составляют атомы d-элементов: Cr, Cu, Nb, Mo, Ru, Rh, Ag, Pt, Au, имеющие один ns-электрон, а Pd – ноль).
Число электронов на заполняемом энергетическом подуровне нейтральных атомов s-элементов равно номеру группы, р-элементов – номеру группы минус 2, а d- и f-элементов, соответственно на (n – 1) d- или (n – 2) f-подуровне, – обычно разности между порядковыми номерами данного элемента и s-элемента IIА-группы того же периода.
Таким образом, на основе Периодической системы элементов Д.И. Менделеева можно определить электронную конфигурацию атомов любого элемента (как нейтральных, так и положительно и отрицательно заряженных – катионов и анионов).
Определим, например, электронную конфигурацию нейтрального атома элемента железа, находящегося в основном (невозбуждённом) состоянии.
1. Порядковый номер элемента железа 26, заряд атомного ядра +26, число электронов в атоме – 26.
2. Период – 4-й, следовательно, в атоме железа электроны занимают четыре энергетических уровня с подуровнями 1s2s2p3s3p3d4s.
3. Железо находится в VIIIБ-группе, то есть принадлежит к d-элементам, и в его атоме заполняется 3d-подуровень.
4. На s-подуровне внешнего энергетического уровня имеется 2 электрона: 4s2.
5. На заполняемом 3d-подуровне имеется 26 – 20 = 6 электронов: 3d6 (20 – порядковый номер кальция, элемента IIА-группы 4-го периода).
6. Остальные энергетические подуровни атома железа заполняются максимально возможным для них числом электронов.
Полная электронная формула нетрального атома железа:
26Fe 1s22s22p63s23p64s23d6.
7. Общее число электронов в атоме равно: 2 + 2 + 6 + 2 + 6 + 2 + 6 = 26, что соответствует порядковому номеру элемента железа.
Последовательность составления электронных формул атомов элементов на основе их местоположения элементов в Периодической системе элементов Д.И. Менделеева позволяет прежде всего определить электронное строение внешних энергетических уровней их атомов и тем самым выявить особенности, определяющие их химические свойства, то есть способность отдавать или присоединять электроны.
Атомы элементов, не имеющие на внешнем энергетическом уровне устойчивой электронной конфигурации ns2np6, при химическом взаимодействии с атомами других элементов перестраивают свой внешний энергетический уровень для достижения устойчивой конфигурации. В зависимости от природы атомов элементов это достигается тремя путями: отдачей, присоединением или обобществлением электронов с образованием химической связи. При этом атомы элементов с числом электронов на внешнем энергетическом уровне меньше четырёх обычно отдают электроны (являются восстановителями), а с числом больше четырёх – принимают электроны (являются окислителями).
Способность атома элемента отдавать или присоединять электроны зависит от его радиуса и характеризуется величинами энергии ионизации и сродства к электрону, а в составе молекулы – его относительной электроотрицательностью (разделы 2.1-2.4)
Периодичность повторения внешних электронных конфигураций атомов элементов приводит к периодическому изменению их свойств. В этом – физический смысл периодического закона.
Дата добавления: 2014-12-30; просмотров: 584; Мы поможем в написании вашей работы!; Нарушение авторских прав |