
КАТЕГОРИИ:
АстрономияБиологияГеографияДругие языкиДругоеИнформатикаИсторияКультураЛитератураЛогикаМатематикаМедицинаМеханикаОбразованиеОхрана трудаПедагогикаПолитикаПравоПсихологияРиторикаСоциологияСпортСтроительствоТехнологияФизикаФилософияФинансыХимияЧерчениеЭкологияЭкономикаЭлектроника
Биологическая роль катионов второй аналитической группы. Применение соединений катионов второй аналитической группы в медицине
Свинец.Биологическая роль свинца не установлена. Его соединения токсичны. У рабочих различных производств, связанных с получением и применением свинца, могут встречаться явления острого и хронического отравления (сатурнизм). При сатурнизме наблюдается ряд симптомов поражения ЦНС (головная боль, бессонница, судороги, галлюцинации, атрофия зрительного нерва), а также нарушения функции почек (альбуминурия) и желудочно-кишечного тракта («свинцовые колики»).
В медицине соединения свинца применяются только наружно как антисептические и вяжущие средства. Оксид свинца РbО входит в состав свинцового пластыря, используемого при воспалительных заболеваниях кожи, фурункулезе. Добавки свинца используют при изготовлении одежды для медперсонала рентгеновских кабинетов (фартуки, рукавицы, шлемы), так как свинец поглощает рентгеновские и γ-лучи.
Серебро.Физиологическая роль серебра в живом организме изучена недостаточно. Серебро относится к ультрамикроэлементам. Это означает, что оно находится в организме в концентрации менее 10-12 %.
В медицине применяются:
1. Нитрат серебра AgNO3 (ляпис) - вяжущее и прижигающее средство, используется наружно. Применяется в стоматологии для серебрения корневых каналов и кариозных полостей зубов перед их пломбированием. Сначала из нитрата серебра получают аммиачный раствор оксида серебра, затем добавляют водный раствор формальдегида с его массовой долей 10 %. Химизм этого процесса может быть выражен следующим образом:
2AgNO3 + 2NH4OH → Ag2O + 2NH4NO3 + H2O
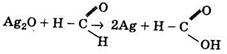
Образующаяся серебряная пленка посылает в окружающее пространство ионы серебра, которые обладают бактерицидным действием.
2. Нитрат и хлорид серебра применяются для пропитки перевязочного материала - бумаги, ваты, марли.
Ртуть. Ртутное заражение почвы, природных вод, растений и животных в настоящее время характерно для многих регионов планеты. Оно связано с поступлением в биосферу большого количества ртути в виде продуктов промышленного производства, выхлопов транспорта, ядохимикатов. Ртуть накапливается главным образом в печени и почках. При хроническом отравлении ртутью и ее соединениями («меркуризм») появляются металлический привкус во рту, сильное слюнотечение, слуховые и обонятельные галлюцинации, головные боли, наблюдается ослабление памяти.
Хотя все соли ртути ядовиты, многие из них применяются в медицине.
1. Желтая ртутная мазь — оксид ртути (II). Используется для лечения кожных заболеваний.
2. Хлорид ртути (II) HgCl2 (сулема). Обладает высокой токсичностью, при работе с ней необходимо соблюдать большую осторожность; растворы в разведении 1:1000 применяются для дезинфекции белья, предметов ухода за больными, помещений, медицинского инструментария.
В медицине используют не только соединения, но и саму ртуть и ее пары (ртутные термометры, ртутные манометры в аппаратах для измерения кровяного давления). Ультрафиолетовые лучи, полученные от ртутнокварцевых ламп, глубоко прогревают ткани, губительно действуют на многие микроорганизмы.
Дата добавления: 2014-11-13; просмотров: 749; Мы поможем в написании вашей работы!; Нарушение авторских прав |