
КАТЕГОРИИ:
АстрономияБиологияГеографияДругие языкиДругоеИнформатикаИсторияКультураЛитератураЛогикаМатематикаМедицинаМеханикаОбразованиеОхрана трудаПедагогикаПолитикаПравоПсихологияРиторикаСоциологияСпортСтроительствоТехнологияФизикаФилософияФинансыХимияЧерчениеЭкологияЭкономикаЭлектроника
ИЗМЕЛЬЧЕНИЕ
Вопросам измельчения в фармацевтической технологии придается особое значение. Известно, что с уменьшением размера частиц резко увеличивается поверхностная энергия измельчаемого лекарственного вещества. При тонком измельчении
лекарственные вещества лучше растворяются, быстрее и полнее участвуют в химических реакциях и т. д. Измельчение может существенным образом влиять на терапевтическую активность лекарственных веществ вследствие изменения процессов их всасывания. Это происходит при изменении растворимости лекарственных веществ, скорость которой прямо пропорциональна площади поверхности и обратно пропорциональна величине частиц вещества. Например,при назначении одинаковых доз сульфадимезина микронизированного и полученного в заводском производстве без дополнительного измельчения выявлено, что в первом случае в плазме крови людей содержание вещества на 40 % выше, максимальная концентрация достигается на 2 ч раньше, а общее количество всосавшегося вещества на 20 % больше, чем во втором случае. При уменьшении размера частиц кислоты ацетилсалициловой до микронизированных увеличивалось приблизительно в 2 раза ее анальгетическое, жаропонижающее и противовоспалительное действие.
Убедительные результаты о влиянии размера частиц лекарственных веществ на высвобождение и всасывание получены при изучении суспензий и мазей. Например, сульфадиметоксин микронизированный (3— 12мкм). введенный животным в виде 2% водной суспензии из расчета 500 мг/кг. всасывался в кровь значительно быстрее по сравнению с лекарственным веществом, отвечающим требованиям нормативно-технической документации. Его максимальная концентрация через 1—2 ч составляла от 18,5 до 21,9мг/мл. в то время как в контрольной группе максимальный уровень вещества в крови достигался через 4 ч и составлял лишь 5 мг/мл.Аналогичные результаты получены при использовании суспензии сульфамонометоксина.
В аптечной практике необходимый размер частиц порошка получают при соблюдении следующих условий измельчения: выбор ступки, время измельчения, применение аппаратов, порядок смешивания, особые правила и приемы технологии . Технология других лекарственных форм, например суспензий, мазей, где возможно растворение или измельчение лекарственных веществ, также имеет свои особенности.
Полиморфизм. Это явление свойственно веществам, которые могут существовать в двух и более кристаллических модификациях. Полиморфизм особенно распространен среди салицилатов, барбитуратов, сульфамидов, гормональных препаратов. Так, например, ацетилсалициловая кислота известна в шести кристаллических формах (сферические, игольчатые и другой формы кристаллы), кортизона ацетат — в пяти и т. д. Получение той или иной кристаллической модификации обусловливается комплексом условий, при которых протекает синтез (или выделение из природного сырья), и в большей степени от условий, в которых протекает кристаллизация субстанции (температурный фактор, природа растворителя, давление и т. д.).
Различные полиморфные модификации одного и того же препарата обладают различной способностью к растворению, плавлению, стойкостью к окислению, различаются по своим поверхностным свойствам, от которых зависит как скорость всасывания лекарственных веществ, так и их стабильность в лекарственных формах.
Типичным примером, показывающим терапевтическое значение факта полиморфизма лекарственных веществ, может служить суспензия цинк-инсулина (Suspensio Zinc-insulini). После реакции с хлоридом цинка осажденный инсулин представляет собой нерастворимый комплекс, который в зависимости от значения рН среды может быть аморфным или кристаллическим. При необходимости получения быстрого и непродолжительного действия используют легко всасывающийся аморфный цинк-инсулин. Кристаллический цинк-инсулин всасывается медленно и обеспечивает пролонгированное действие гормона.
форм вспомогательных веществ.
Химическая модификация. Одно и то же вещество может быть использовано в качестве лекарственного средства в разных химических состояниях. В простейших случаях это может касаться солеобразования того или иного активного вещества. Например, алкалоид хинин из основания может быть переведен в разные соли: сульфат, хлорид, бромид. Их растворимость будет равна соответственно 1:800, 1:34, 1:16, При сохранении фармакологического действия хинина его соли, как обладающие различной растворимостью, будут иметь разную кинетику всасывания.
Дисперсность. Размер частиц лекарственного вещества имеет не только технологическое значение, т. е. существенно влияет на сыпучесть порошкообразных материалов, однородность смешения, точность дозирования и т. д., но, что является особенно важным, оказывает большое влияние на скорость и полноту всасывания лекарственного вещества при любых способах его назначения, исключая, конечно, внутрисосудистый.
Солюбилизация.Многие лекарственные вещества обладают плохой растворимостью в воде. Повысить их растворимость можно, использовав эффект солюбилизации. В присутствии поверхностно-активных веществ (ПАВ) плохо растворимые и даже практически нерастворимые в воде органические лекарственные вещества приобретают способность коллоидно растворяться, или солюбилизироваться.
Например, с помощью твина-80 можно существенно повысить растворимость синэстрола и метилтестостерона.
ГФХ1 ст. «Суспензии»
Суспензии — жидкая лекарственная форма, содержащая в качестве дисперсной фазы одно или несколько измельченных порошкообразных лекарственных веществ, распределенных в жидкой дисперсионной среде.Различают суспензии для внутреннего, наружного и парентерального применения. Суспензии для парантерального применения вводят только внутримышечно. Они должны соответствовать статье «Инъекции», если нет других указаний в частных статьях.
Суспензии могут быть готовыми к применению, а также в виде порошков или гранул для суспензий, к которым перед применением прибавляют воду или другую подходящую жидкость; количество воды или другой жидкости должно быть указано в частных статьях.
В качестве вспомогательных используют вещества, увеличивающие вязкость дисперсионной среды, поверхностно-активные и буферные вещества, корригенты, консерванты, антиокислители, красители и другие, разрешенные к медицинскому применению. Перечень вспомогательных веществ должен быть указан в частных статьях. Не допускается изготовление суспензий, содержащих ядовитые вещества.
Отклонение в содержании действующих веществ в 1 г (мл) суспензии не должно превышать±10 %.
Перед употреблением суспензии взбалтывают в течение 1-—2 мин. при этом должно наблюдаться равномерное распределение частиц твердой фазы в жидкой дисперсионной среде. Время седиментационной устойчивости суспензии или размер частиц твердой фазы должны быть указаны в частных статьях.
Маркировка. Для суспензий, полученных из порошков или гранул, должны быть указаны условия и время хранения после прибавления воды. Все виды суспензий должны иметь указание: «Перед употреблением взбалтывать»-
Упаковка. С соответствующим дозирующим устройством. Хранение. В упаковке, обеспечивающей стабильность при хранении и транспортировании и. если необходимо, в прохладном месте.
Фарм. экспертиза рецепта.
Проверка доз
ВРД-0.06 РД0,05
ВСД-0,18 СДО,05*3=0,15
Число приемов: 120:5=24
РД=1,2:24=0,05
Дозы не завышены.
Для приготовления такой суспензии в ступке в течение 30 с измельчают 1.2 гфталазола. Затем туда же вносят 0.6 мл 1 % р-ра метилцеллюлозы. Полученную смесь диспергируют еще в течение 60 с, затем постепенно разбавляют 1% р-ром метилцеллюлозы и смывают во флакон для отпуска. 1% р-ра метилцеллюлозы обеспечивает возможность получения очень тонко диспергированных суспензий.
Срок годн - при Т не выше 25С 3 суток.
ВопросЗ. Folia Vitis idaeae (Folia Vaccinii vitisidaeac)
Брусника (Vaccinium vitis-idaea L) из сем. вересковых (Ericaceae), подсем.брусничных (Vaccinio-deae); используют в качестве лекарственного средства.
Химический состав. Листья брусники содержат арбутин (4-9 %), свободный гидрохинон; флавоноиды— гиперозид, кверцитрин. изокверцит-рин, рутин, кемпферол; дубильные вещества преимущественно конденсированного ряда (до 15 %); кислоты урсоловую. эллаговую и хинную.

Качественные реакции. Подлинность сырья устанавливают также по присутствию арбутина и дубильных веществ. Качественные реакции. Измельченные листья в количестве 0,5 г (кипятят с 10 мл воды в течение 2—3 мин и фильтруют через бумажный фильтр.К 1 мл фильтрата (в фарфоровой чашке) прибавляют 4 мл раствора аммиака и по каплям 1 мл 10% раствора натрия фос-форно-молибденовокислого в хлористоводородной кислоте; появляется синее окрашивание (арбутин).
К 2—3 мл фильтрата (в фарфоровой чашке) прибавляют 2— 3 капли раствора железоаммониевых квасцов; появляется черно-синее окрашивание и осадок (дубильные вещества).
Числовые показатели. Арбутина, определяемого йодометрическим титрованием, не менее 4,5 % (листья); не менее 4 % (побеги); влажность не более 13 %; золы общей не более 7 %; золы, нерастворимой в 10 % растворе
Хранение. На складах и в аптечных учреждениях сырье хранят в сухих, хорошо проветриваемых помещениях. Срок годности 3 года.
Количественное определение. 1.Взятие аналитической пробы, предварительно измельченной. 2. Извлечение арбутина из ЛРС (повторяют 2 раза)
3. Фильтрование горячего извлечения с промывкой фильтра.
4. К фильтрату прибавляют 3 мл раствора свинца ацетата основного, перемешивают и по охлаждении доводят объем фильтрата водой до метки.
5. Колбу помещают в кипящую водяную баню и выдерживают до полной коагуляции осадка.
6. Горячую жидкость полностью отфильтровывают в сухую колбу через бумажный фильтр диаметром 10 см, прикрывая воронку часовым стеклом. После охлаждения к фильтрату прибавляют 1 мл концентрированной серной кислоты, колбу взвешивают с погрешностью ±0,01 г, присоединяют к обратному холодильнику и нагревают на плитке в течение 1,5 ч, поддерживая равномерное и слабое кипение.
7. Нейтрализация фильтрата натрия гидрокарбонатом.
8. Титрование йодом из микробюретки.
9. Расчет содер. арбутина.
Применение. В виде отвара или настоя как дезинфицирующее и мочегонное средство прициститах. ревматизме, препарат обладает диуретическим средством. ^С/^- //VV
Вопрос 4.Рецепт выписан не верно, рецепт д.б. выписан на бланке ф.№Ю7/У, заверенным личной печатью и подписью врача. £/% —" fa'z/^fcc^Cr? ^W^^^z^ /-zfttf-fz&fae }J/
Срок действия рецепта - 2 мес. Рецепт отдается больному с указание на обороте количества отпущенного препарата и даты отпуска и не хранится в аптеке. По истечении срока действия рецепт гасится штампом «Рецепт не действителен».
Способ применения ЛС обозначается на русском или русском и национальном языках с указанием дозы, частоты, времени приема и его длительности, а для ЛС, взаимодействующих с пищей, времени их употребления относительно приема пищи (до, во время, после еды).
Условия хранения в аптеке: Готовые средства укладываются в упаковке этикеткой наружу. На шкафы и полки прикрепляется стеллажная карта, в которой отражены наименование лекарства, серия и срок годности.
Такая карта заводится на каждую вновь поступившую серию, что позволяет осуществлять контроль своевременной ее реализации.
В отделе должна находиться картотека по срокам годности препаратов.
Лекарственные средства с истекшим сроком годности хранятся отдельно и подлежат переконтролю (после получения результатов анализа).
Таблетки и драже необходимо хранить отдельно от других средств в заводской упаковке в сухом и при необходимости в защищенном от света месте.
Лекарственное растительное сырье хранят в сухом хорошо вентилируемом помещении в хорошо закрытой таре.
Лицензирование в сфере обращения лекарственных средств
В любой стране с целью обеспечения качества лекарственных препаратов и оказания фармацевтической помощи создаются системы взаимодействующих органов, центров иорганизаций, выполняющих определенные функции, среди которых немаловажное значение имеет функция лицензирования. В частности, ВОЗ создана и функционирует Система сертификации лекарственных препаратов для международной торговли, в соответствии с которой осуществляется лицензирование лекарственных препаратов, производителей и оптовиков.
Для государственного регулирования и контроля за отдельными приоритетными видами деятельности в России предусмотрена специальная норма права, которая называется лицензированием, введенная в процессе рыночных преобразований в начале 90-х гг. XX в. Эта норма права способствует защите свобод, прав, законных интересов, нравственности и здоровья граждан, обеспечению обороны страны и безопасности государства.
Лицензируемый вид деятельности — это деятельность, на осуществление которой на территории РФ требуется получение лицензии.
Основным критерием отнесения к лицензируемым видам деятельности является возможность нанесения в результате осуществления данной деятельности ущерба правам', законным интересам, здоровью граждан, обороне и безопасности государства, культурному наследию народов РФ, а также то, что их регулирование не может осуществляться иными методами, кроме как лицензированием.
Правовая основа лицензирования.Правовой основой лицензирования фармацевтической деятельности являются федеральные законы, постановления Правительства РФ, приказы Министерства здравоохранения Российской Федерации и другие правовые акты.
Вопросы лицензирования затрагиваются в нескольких статьях Федерального закона «О лекарственных средствах». В ст. 15 «Лицензирование производства лекарственных средств» определены лицензионные требования на производство ЛС, перечень необходимых документов, сроки и условия получения лицензии. В ст. 17 «Изготовление лекарственных средств» указывается на необходимость получения лицензии на осуществление фармацевтической деятельности, в частности на изготовление ЛС. В ст. 23 «Лицензирование внешнеторговой деятельности» определена необходимость получения лицензии на внешнеторговую деятельность предприятиями-изготовителями и предприятиями оптовой торговли. Лицензия выдается федеральными органами исполнительной власти. На основании данной лицензии осуществляется ввоз и вывоз лекарственных препаратов. В ст. 30 «Лицензирование оптовой торговли лекарственными средствами» определена необходимость лицензирования, установлены территориальные ограничения на действие лицензии. Федеральные лицензии действуют на всей территории РФ, а лицензии, выданные территориальным органом исполнительной власти, действуют на территории данного региона. В той же статье указано на необходимость разработки Правил оптовой торговли ЛС. В ст. 34 «Лицензирование фармацевтической деятельности аптечных учреждений» установлено, что лицензия на розничную реализацию ЛС выдается органами исполнительной власти субъектов Федерации, дан перечень документов, необходимых для ее получения.
Для регулирования отношений, возникающих между федеральными органами исполнительной власти, органами исполнительной власти субъектов РФ, юридическими лицами и индивидуальными предпринимателями в связи с осуществлением лицензирования отдельных видов деятельности, принят специальный Федеральный закон «О лицензировании отдельных видов деятельности».
Под лицензированием понимаются мероприятия, связанные с выдачей лицензий, переоформлением документов, подтверждающих наличие лицензий, приостановлением и аннулированием лицензий и контролем лицензирующих органов за соблюдением лицензиатами при осуществлении лицензируемых видов деятельности соответствующих лицензионных требований и условий.
Все существующие виды деятельности с точки зрения лицензирования можно разделить на три группы: 1) деятельность, не требующая лицензирования; 2) деятельность, требующаяспециального лицензирования; 3) деятельность, лицензирование которой проводится в соответствии с Федеральным законом «О лицензировании отдельных видов деятельности».
К первой группе можно отнести оказание некоторых фармацевтических услуг, например доставку лекарств на дом. Культивирование лекарственных растений, проведение научных исследований в области изыскания, создания, получения, разработки технологии некоторых ЛС (кроме наркотических средств и психотропных веществ) также не требуют лицензирования.
Ко второй группе относятся виды деятельности, лицензирование которых осуществляется в соответствии со специальными нормативными документами и на которые действие Федерального закона о «Лицензировании отдельных видов деятельности» не распространяется. Например, деятельность в области производства и оборота этилового спирта, алкогольной и спиртосодержащей продукции; деятельность в области таможенного дела; страховая деятельность: осуществление внешнеэкономических операций; использование результатов интеллектуальной деятельности: использование природных ресурсов, в том числе недр, лесного фонда, объектов растительного и животного мира, образовательная деятельность и др. В данном случае Правительством РФ принимаются специальные законы о лицензировании. Так, принят Федеральный закон от 07.01.99 № 18-ФЗ «О государственном регулировании производства и оборота этилового спирта, алкогольной и спиртосодержащей продукции».
К третьей группе относятся виды деятельности, на которые распространяется действующий Федеральный закон «О лицензировании отдельных видов деятельности» и которые перечислены в соответствующей статье. В последнем принятом законе значительно сокращено количество лицензируемых видов деятельности, в настоящее время их названо 116 против 250, определенных предыдущим документом.
Принципы лицензирования.Основными законодательно утвержденными принципами осуществления лицензирования в РФ являются:
обеспечение единства экономического пространства на территории РФ;
установление единого перечня лицензируемых видов деятельности;
установление единого порядка лицензирования на территории РФ;
установление лицензионных требований и условий положениями о лицензировании конкретных видов деятельности;
гласность и открытость лицензирования;
соблюдение законности при осуществлении лицензирования.
Единство экономического пространства. В целях обеспечения единства экономического пространства на территории РФ правительство утверждает Положения о лицензировании конкретных видов деятельности, определяет федеральные органы исполнительной власти, осуществляющие лицензирование конкретных видов деятельности, устанавливает виды деятельности, лицензирование которых осуществляется органами исполнительной власти субъектов Федерации.
В принятом Федеральном законе «О лицензировании отдельных видов деятельности» даются общие нормы права, единые для всех видов деятельности, регулируемых данным законом. Таким образом, для учета особенностей лицензируемых видов деятельности Правительством РФ специальными постановлениями утверждаются Положения о лицензировании конкретных видов деятельности. Любое изменение в федеральном законодательстве должно сопровождаться приведением в соответствие с ним всех подзаконных актов. Так. в связи с выходом в 2001 г. Федерального закона, регулирующего процесс лицензирования, началась работа по приведению существующих положений в соответствие с новым законом. В настоящее время приняты постановления Правительства РФ: «Об утверждении Положения о лицензировании фармацевтической деятельности» от 01.07.2002 № 489, «О лицензировании деятельности, связанной с оборотом наркотических средств и психотропных веществ» от 21,06.2002 № 454. «Об утверждении Положения о лицензировании деятельности по культивированию растений, используемых для
производства наркотических средств и психотропных веществ» от 14.06.2002 № 423, «Об утверждении Положения о лицензировании производства лекарственных средств» от 04.07.2002 № 500, «Об утверждении Положения о лицензировании медицинской деятельности» от 04.07.2002 № 499 и др.
Единый перечень лицензируемых видов деятельности. Он устанавливается Федеральным законом, где в соответствующей статье перечислены подпадающие под его действие виды деятельности (в Федеральном законе «О лицензировании отдельных видов деятельности» — это ст. ] 7). Среди перечисленных видов деятельности так или иначе связаны с деятельностью субъектов фармацевтического рынка следующие: фармацевтическая деятельность; производство ЛС; производство медицинской техники; деятельность по распространению ЛС и ИМИ; культивирование растений, используемых для производства наркотических средств и психотропных веществ; деятельность, связанная с оборотом наркотических средств и психотропных веществ (разработка, производство, изготовление, переработка, хранение, перевозки, отпуск, реализация, распределение, приобретение, использование, уничтожение), внесенных в Список II в соответствии с Федеральным законом «О наркотических средствах и психотропных веществах»; деятельность, связанная с оборотом наркотических средств и психотропных веществ (разработка, производство, изготовление, переработка, хранение, перевозки, отпуск, реализация, распределение, приобретение, использование, уничтожение), внесенных в Список III в соответствии с Федеральным законом «О наркотических средствах и психотропных веществах»; деятельность, связанная с использованием возбудителей инфекционных заболеваний; производство дезинфекционных, дезинсекционных, дератизационных средств; аудиторская деятельность; деятельность по изготовлению и ремонту средств измерений; ветеринарная деятельность; медицинская деятельность и др.
Как уже упоминалось, для учета особенностей каждого конкретного вида деятельности разрабатываются специальные положения, которые утверждаются постановлениями Правительства РФ. Аналогичные положения могут быть утверждены в субъектах РФ. которые представляют региональный уровень управления и которым дано право определять порядок лицензирования на своей территории в соответствии с местными условиями. Например, в Москве распоряжением мэра утверждено Временное положение о порядке лицензирования фармацевтической деятельности на территории города Москвы, которое разработано с учетом федеральных правовых документов, специальным приказом Комитета здравоохранения Правительства Москвы № 369 от 20.08.2001 утверждено Положение о лицензировании медицинской и фармацевтической деятельности в городе Москве, определяющее порядок получения лицензии в столице.
Единый порядок лицензирования. Он обусловлен:
едиными правами и полномочиями, предоставленными лицензирующим органам;
требованиями, предъявляемыми к соискателям лицензий и лицензиатам;
процедурой лицензирования,
К лицензирующим органам в России относятся федеральные органы исполнительной власти и органы исполнительной власти субъектов РФ. которые осуществляют лицензирование в соответствии с действующим законом.
С Билет 9. Вопрос 1. }■
^Тюе—как-^етвор—готовился без стабилизатора, то при значительных увеличениях рН раствора (сильно щелочное стекло) иногда наблюдается выделение сильных свободных оснований, например новокаина. При значительных увеличениях рН раствора (сильно щелочное стекло) иногда наблюдается выделение сильных свободных оснований, например новокаина.
Procaine Hydrochloride — прокаина гидрохлорид (Новокаин) 
в-диэтиламиноэтилового эфира
n-аминобензойной кислоты гидрохлорид
Бесцветные кристаллы или белый кристаллический порошок
без запаха. Т. пл. 154-158 С
Прокаина гидрохлорид очень легко растворим в воде, растворим в этаноле. Прокаина гидрохлорид мало растворим в хлороформе и практически нерастворим в эфире.
Подлинность прокаина гидрохлорида устанавливают по идентичности ИК-спектров, снятых после прессования в таблетках бромида калия в области 4000-400 см"1 и прилагаемых к ФС рисунков спектров стандартных образцов.
УФ-спектры должны иметь характеристики, приведённые в соответствующих ФС. Водный 0,001% раствор прокаина гидрохлорида имеет максимум поглощения при 290 нм. ля идентификации производных п-аминобензойной кислоты использованы также различные оптические характеристики электронных полос поглощения (сила осциллятора, фактор асимметрии и др.).
НД рекомендуют как общие, так и частные реакции для испытания подлинности сложных эфиров п-аминобензойной кислоты. Одна из них основана на образовании азокрасителя. Это общая реакция для соединений, имеющих незамещенную первичную ароматическую аминопшшу.



Идентификацию производных п-аминобензойной кислоты можно осуществить с помощью общих реакций на первичные ароматические амины. Они образуют шиффовы основания,вступая во взаимодействие с альдегидами, например, с п-диметиламинобензальдегидом в присутствии концентрированной серной кислоты. Появляется желтое или оранжевое окрашивание:

Являясь сложным эфиром прокаин при взаимодействии с гидроксиламином в щелочной среде образуют гидроксамовые кислоты:

После подкисления хлороводородной кислотой и прибавления раствора хлорида железа (III) образуются гидроксаматы железа, имеющие у прокаина —- вишневое окрашивание:

Выполняя гидроксамовую реакцию следует строго соблюдать требования методики, т.к. она дает положительные результаты только при определенном значении рН.
Первичные ароматические амины вступают в реакции конденсации с 2,4-динитрохлорбензолом, образуя имеющие хиноидную структуру -— соединения цвиттер-ионы:

Появляется желто-оранжевое окрашивание после дооавления этого реактива, раствора гидроксида натрия и нагревания. Окрашенное соединение извлекается хлороформом после подкисления уксусной кислотой.
Под действием хлороформа и спиртового раствора гидроксида натрия первичные ароматические амины образуют изонитрилы — вещества, имеющие тошнотворный запах:

Прокаин может быть идентифицирован с помощью некоторых осадительных (общеалкалоидных) реактивов (пикриновой, фосфорновольфрамовой,
фосфорномолибденовой кислотами, хлоридом ртути (И) и др.).

а также с помощью реакции галогенирования. I юдобно другим первичным ароматическим аминам, прокаина гидрохлорид образуют дибром- или дииодпроизводные. 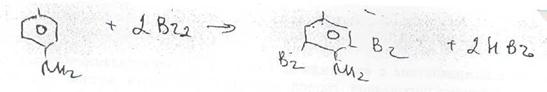
Сложные эфиры п-аминобензойной кислоты при окислении образуют окрашенные или бесцветные продукты реакции. Для установления подлинности прокаина гидрохлорида выполняют реакцию с пергидролем и концентрированной серной кислотой. Постепенно появляется сиреневое окрашивание. Со смесью концентрированных серной и азотной кислот прокаин при нагревании образует оранжево-красное окрашивание.
При добавлении к 2,5%-ному водному раствору прокаина гидрохлорида 0.15 мл хлороводородной кислоты и 1 мл 0.1 М раствора перманганата калия фиолетовое окрашивание тотчас исчезает. Эта реакция позволяет отличать прокаина гидрохлорид от других местн о анестезирующих лекарственных веществ.
Тетракаина гидрохлорид из растворов осаждается иодидом калия в виде иодоводородной
Для количественного определения сложных эфиров п-аминобензойной кислоты, ФС рекомендует нитритометрический метод. При определении прокаина гидрохлорида, как и других первичных ароматических аминов, происходит образование солей диазония:

Э ~ м новокаина t—
X (%) - Т*У*Кпер* 100% g
При нитритометрическом титровании сложных эфиров п-аминобензойной кислоты точку эквивалентности можно устанавливать либо потенциометрически, либо используя внутренние индикаторы: нейтральный красный или смесь тропеолина 00 с метиленовым синим.
Гидрохлориды прокаина могут быть количественно определены по связанной хлороводородной кислоте методом алкалиметрии:

Титрование ведут в присутствии хлороформа, который извлекает выделяющееся основание. Возможно также аргентометрическое определение этих лекарственных веществ по хлорид-иону.

Известны методики бромид-броматометрического и иодхлорометрического определения прокаина гидрохлорида, основанные на образовании дибром- и дииодпроизводных: 
Для их количественного определения используют также неводное титрование в среде безводной уксусной кислоты 0,1 М раствором хлорной кислоты с визуальным или потенциометрическим установлением точки эквивалентности.

Количественное определение сложных эфиров п-аминобензойной кислоты выполняют также спектрофотометрическим методом в максимумах светопоглощения: прокаина гидрохлорид при 298 нм (вода) или при 290 нм (0,001 М раствор хлороводородной кислоты
Прокаина гидрохлорид хранят по списку Б в хорошо укупоренной таре, предохраняющей от действия света (б банках из оранжевого стекла"). Производные сложных эфиров и-аминобензойной кислоты — местноанестезирующие средства. Прокаина гидрохлорид широко применяют для спинно-мозговой и инфильтрационной анестезии в виде 0,25-0,5%-ных водных растворов.
Вопрос 2.
При изготовлении и хранении лекарственных препаратов нередко наблюдается изменение их свойств, протекающее с различной скоростью и степенью проявления. Это связано с уменьшением содержания лекарственных веществ или снижением их фармакологической активности, изменением, свойств лекарственных форм и т. д. Подобные изменения влияют на срок годности (хранения) препаратов, который может колебаться от нескольких часов (растворы антибиотиков) или дней (растворы ферментов) до нескольких лет. Вопросам стабильности лекарственных средств в настоящее время уделяется большое внимание.
Стабильность препарата — это способность биологически активного вещества сохранять физико-химические свойства и фармакологическую активность в течение определенного срока хранения, предусмотренного нормативно-технической документацией.
Стабильность лекарственных препаратов зависит от многих факторов — температуры хранения, освещенности, состава окружающей атмосферы, способа приготовления, т. е. технологии лекарственной формы, вспомогательных веществ, вида лекарственной формы, особенно ее агрегатного состояния, упаковки и др.
Используемые в настоящее время методы стабилизации лекарственных средств — химический и физический, нередко применяются в комплексе, дополняя друг друга. Химические методы основаны на добавлении химических веществ — стабилизаторов, антиоксидантов и консервантов. Физические методы базируются на защите лекарственных веществ от неблагоприятных воздействий внешней среды, применении лекарственных и вспомогательных веществ высокой степени очистки, использовании современного технологического оснащения и результатов научных исследований в технологии лекарственных форм — применение неводных растворителей, обезвоживание препаратов, ампулирование в токе инертных газов и др.Таким образом, стабильность препарата — это способность биологически активъ. вещества сохранять физико-химические свойства и фармакологическую активность ,_ течение определенного срока хранения, предусмотренного нормативно-технической документацией.
Химические методы стабилизации.Стабилизация гомогенных дисперсных систем основана на подавлении процесса разложения лекарственных веществ за счет связывания или нейтрализации тех химических соединений, которые активируют деструкцию лекарственного вещества. Такие соединения находятся в растворе в незначительных количествах, либо переходят в раствор из упаковки (стекла) при его технологической обработке (стерилизации) и хранении.
Стабильность инъекционных растворов, в первую очередь, зависит от качества исходных растворителей и лекарственных веществ, класса и марки стекла ампул и флаконов, наличия кислорода в воде и растворах, рН растворов, температуры и времени стерилизации, наличия ионов тяжелых металлов, условий хранения препаратов и т. д.
Основной принцип стабилизации препаратов предусматривает максимальное устранение факторов, способствующих изменению лекарственных веществ.
Влияние качества стекла на стабильность веществ. Медицинское стекло представляет, собой твердый раствор, полученный в результате охлаждения расплавленной смеси силикатов, оксидов металлов и некоторых солей. В зависимости от качественного и количественного соотношения оксидов металлов в стекле различают классы и марки медицинского стекла, обладающие различной химической устойчивостью»..
На поверхности стекла ампул или флаконов при контакте с водными инъекционными растворами во время хранения, и особенно при тепловой стерилизации, в зависимости от его марки и значения рН раствора может происходить процесс выщелачивания или растворения верхнего слоя стекла. Выщелачивание — это выход из стекла преимущественно оксидов щелочных и щелочноземельных металлов, благодаря высокой подвижности ионов этих металлов по сравнению с. высоким зарядом четырехвалентного иона кремния. По этой причине ион натрия даже при комнатной температуре может замещаться другими ионами. При более глубоких процессах выщелачивания ионы щелочных металлов легко перемещаются из внутренних слоев стекла на место ионов, вступивших в реакцию. Выщелачивание из стекла компонентов и их гидролиз ведут к увеличению или уменьшению величины рН раствора. Это приводит к изменениям свойств лекарственных веществ, в основе которых лежат различные химические процессы: гидролиз, окисление, восстановление, омыление, декарбоксилирование, изомеризация и др.
Оптимальная концентрация водородных ионов в инъекционных растворах — существенный стабилизирующий фактор. Она достигается путем добавления стабилизаторов, которые предусмотрены в нормативно-технической документации, а также использованием комплекса технологических приемов в процессе приготовления парентеральных растворов.
Стабилизаторы могут замедлять или ускорять нежелательные химические реакции, создавать, определенные значения рН растворов, повышать растворимость лекарственных веществ или удерживать их во взвешенном состоянии. Выбор стабилизатора, в первую очередь, зависит от природы лекарственных веществ.
Среди требований, предъявляемых к стабилизаторам, можно отметить: терапевтическую индифферентность, хорошую растворимость в растворителе, эффективность в применяемых концентрациях, химическую чистоту, доступность.
Несмотря на многообразие и чрезвычайную сложность процессов в растворах, лекарственные вещества, требующие стабилизации, можно условно разделить на три группы:
1. Растворы солей, образованных слабыми основаниями и сильными кислотами.
2. Растворы солей, образованных сильными основаниями и слабыми кислотами.
3. Растворы легкоокисляющихся веществ..^^««wjwiwi и фармакологическое действие его снижается
Для подавления данного типа гидролиза создается кислая среда за счет добавления 0,1 н раствора кислоты хлороводородной. Количество кислоты зависит от свойств препарата.
Дата добавления: 2015-01-13; просмотров: 408; Мы поможем в написании вашей работы!; Нарушение авторских прав |