
КАТЕГОРИИ:
АстрономияБиологияГеографияДругие языкиДругоеИнформатикаИсторияКультураЛитератураЛогикаМатематикаМедицинаМеханикаОбразованиеОхрана трудаПедагогикаПолитикаПравоПсихологияРиторикаСоциологияСпортСтроительствоТехнологияФизикаФилософияФинансыХимияЧерчениеЭкологияЭкономикаЭлектроника
Вопрос 28. В основе зонной теории лежат следующие главные приближения[1]:
В основе зонной теории лежат следующие главные приближения[1]:
Твёрдое тело представляет собой идеально периодический кристалл.
Равновесные положения узлов кристаллической решётки фиксированы, то есть ядра атомов считаются неподвижными (адиабатическое приближение). Малые колебания атомов вокруг равновесных положений, которые могут быть описаны как фононы, вводятся впоследствии как возмущение электронного энергетического спектра.
Многоэлектронная задача сводится к одноэлектронной: воздействие на данный электрон всех остальных описывается некоторым усредненным периодическим полем.
Диэлектрики – вещества, обладающие малой электропроводностью, т.к. у них очень мало свободных заряженных частиц – электронов и ионов. Эти частицы появляются в диэлектриках только при нагреве до высоких температур. Существуют диэлектрики газообразные (газы, воздух), жидкие (масла, жидкие органические вещества) и твердые (парафин, полиэтилен, слюда, керамика и т.п.).
Полупроводники — это вещества, удельное сопротивление которых убывает с повышением температуры, наличием примесей, изменением освещенности. По этим свойствам они разительно отличаются от металлов. Обычно к полупроводникам относятся кристаллы, в которых для освобождения электрона требуется энергия не более 1,5—2 эВ. Типичными полупроводниками являются кристаллы германия и кремния, в которых атомы объединены ковалентной связью.
Проводни́к — вещество, хорошо проводящее электрический ток[1]; в таком веществе имеются свободные носители заряда, то есть заряженные частицы, которые могут свободно перемещаться внутри объёма вещества. Среди наиболее распространённых твёрдых проводников известны металлы, полуметаллы, углерод (в виде угля и графита). Пример проводящих жидкостей при нормальных условиях — ртуть, электролиты, при высоких температурах — расплавы металлов. Пример проводящих газов — ионизированный газ (плазма). Некоторые вещества, при нормальных условиях являющиеся изоляторами, при внешних воздействиях могут переходить в проводящее состояние, а именно проводимость полупроводников может сильно варьироваться при изменении температуры, освещённости, легировании и т. п.
вопрос 29. Полярность химических связей— характеристика химической связи, показывающая изменение распределения электронной плотности в пространстве вокруг ядер в сравнении с распределением электронной плотности в образующих данную связь нейтральных атомах.
В качестве количественной меры полярности связи используются так называемые эффективные заряды на атомах.
Эффективный заряд определяется как разность между зарядом электронов, находящимся в некоторой области пространства вблизи ядра, и зарядом ядра. Однако эта мера имеет лишь условный и приблизительный смысл, поскольку невозможно однозначно выделить в молекуле область, относящуюся исключительно к отдельному атому, а при нескольких связях — к конкретной связи.
Наличие эффективного заряда может быть указано символами зарядов у атомов (например, Н+δ — Cl−δ, где δ — некоторая доля элементарного заряда).
Практически все химические связи, за исключениям связей в двухатомных гомоядерных молекулах — в той или иной степени полярны. Ковалентные связи обычно слабо полярны. Ионные связи — сильно полярны.
Физический и вычислительный смысл дипольного момента состоит в том, что он дает поправки первого порядка (чаще всего — малые) в положение каждого заряда системы по отношению к началу координат (которое может быть условным, но приближенно характеризует положение системы в целом — система при этом подразумевается достаточно компактной). Эти поправки входят в него в виду векторной суммы, и везде, где при вычислениях такая конструкция встречается (а в силу принципа суперпозиции и свойства сложения линейных поправок — см.Полный дифференциал — такая ситуация встречается часто), там в формулах оказывается дипольный момент.
Электри́ческий ди́польный моме́нт — векторная физическая величина, характеризующая, наряду с суммарным зарядом (и реже используемыми высшими мультипольными моментами), электрические свойства системы заряженных частиц (распределения зарядов) в смысле создаваемого ею поля и действия на нее внешних полей. Главная после суммарного заряда и положения системы в целом (ее радиус-вектора) характеристика конфигурации зарядов системы при наблюдении ее издали.
Вопрос 30 Межмолекулярное взаимодействие — взаимодействие между электрически нейтральными молекулами или атомами.
Бывает электростатическим и донорно-акцепторным. Агрегатные состояния вещества (от латинского aggrego — присоединяю, связываю) — это состояния одного и того же вещества, переходам между которыми соответствуют скачкообразные изменения свободной энергии, энтропии, плотности и других физических параметров вещества.
Газ (французское gaz, происшедшее от греческого chaos — хаос) — это агрегатное состояние вещества, в котором силы взаимодействия его частиц, заполняющих весь предоставленный им объем, пренебрежимо малы. В газах межмолекулярные расстояния велики и молекулы движутся практически свободно.
Жидкость - это агрегатное состояние вещества, промежуточное между твердым и газообразным.
Аморфное твердое состояние вещества является разновидностью переохлажденного состояния жидкости и отличается от обычных жидкостей существенно большей вязкостью и численными значениями кинетических характеристик.
Кристаллическое твердое состояние вещества — это агрегатное состояние, которое характеризуется большими силами взаимодействия между частицами вещества (атомами, молекулами, ионами). Виды межмолекулярных взаимодействийОснову межмолекулярных взаимодействий составляют кулоновские силы взаимодействия между электронами и ядрами одной молекулы и ядрами и электронами другой. В экспериментально определяемых свойствах вещества проявляется усредненное взаимодействие, которое зависит от расстояния R между молекулами, их взаимной ориентации, строения и физических характеристик (дипольного момента, поляризуемости и др.). При больших R, значительно превосходящих линейные размеры l самих молекул, вследствие чего электронные оболочки молекул не перекрываются, силы межмолекулярного взаимодействия можно достаточно обоснованно подразделить на три вида - электростатические, поляризационные (индукционные) и дисперсионные. Электростатические силы иногда называют ориентационными, однако это неточно, поскольку взаимная ориентация молекул может обусловливаться также и поляризационными силами, если молекулы анизотропны.
Вопрос 31 Скорость химической реакции — изменение количества одного из реагирующих веществ за единицу времени в единице реакционного пространства. Является ключевым понятием химической кинетики. Скорость химической реакции — величина всегда положительная, поэтому, если она определяется по исходному веществу (концентрация которого убывает в процессе реакции), то полученное значение умножается на −1.
В 1865 году Н. Н. Бекетовым и в 1867 году Гульдбергом и Вааге был сформулирован закон действующих масс:
Скорость химической реакции в каждый момент времени пропорциональна концентрациям реагентов, возведенным в степени, равные их стехиометрическим коэффициентам.
Константа скорости реакции (удельная скорость реакции) — коэффициент пропорциональности в кинетическом уравнении.
Физический смысл константы скорости реакции k следует из уравнения закона действующих масс: k численно равна скорости реакции при концентрации каждого из реагирующих веществ равной 1 моль/л.
Константа скорости реакции зависит от температуры, от природы реагирующих веществ, но не зависит от их концентрации. Размерность константы скорости реакции зависит от порядка реакции.[1] Если концентрация реагирующих веществ измерена в моль·л-1 (M):
Для реакции первого порядка, k имеет размерность с-1
Для реакции второго порядка, k имеет размерность л·моль-1·с-1 (или M-1·с-1)
Для реакции третьего порядка, k имеет размерность л2·моль-2·с-1 (или M-2·с-1)
Вопрос 32. Кроме концентрации на скорость химической реакции оказывают влияние следующие факторы:
природа реагирующих веществ, наличие катализатора, температура (правило Вант-Гоффа), давление, площадь поверхности реагирующих веществ.
Правило Вант-Гоффа — эмпирическое правило, позволяющее в первом приближении оценить влияние температуры на скорость химической реакции в небольшом температурном интервале (обычно от 0 °C до 100 °C). Я. Х. Вант-Гофф на основании множества экспериментов сформулировал следующее правило:
При повышении температуры на каждые 10 градусов константа скорости гомогенной элементарной реакции увеличивается в два—четыре раза.
Уравнение, которое описывает это правило, следующее:
~V_2=V_1\cdot\gamma^{\frac{T_2-T_1}{10}}
где ~V_2 — скорость реакции при температуре ~T_2, ~V_1 — скорость реакции при температуре ~T_1, ~\gamma — температурный коэффициент реакции (если он равен 2, например, то скорость реакции будет увеличиваться в 2 раза при повышении температуры на 10 градусов).
3.Влияние концентрации реагирующих веществ.При повышении концентрации хотя бы одного из реагирующих веществ скорость химической реакции возрастает в соответствии с кинетическим уравнением.
Вопрос 33 Реакции 0-го порядка. Скорость этих реакций не зависит от концентрации:
 ,
,
где [A] - концентрация исходного вещества. Нулевой порядок встречается в гетерогенных и фотохимических реакциях.
Реакции 1-го порядка. В реакциях типа A  B скорость прямо пропорциональна концентрации:
B скорость прямо пропорциональна концентрации:
 .
.
При решении кинетических уравнений часто используют следующие обозначения: начальная концентрация [A]0 = a, текущая концентрация [A] = a -x(t), где x(t) - концентрация прореагировавшего вещества A. В этих обозначениях кинетическое уравнение для реакции 1-го порядка и его решение имеют вид:
 .
.
Решение кинетического уравнения записывают и в другом виде, удобном для анализа порядка реакции:
 .
.
ПЕРИОД ПОЛУРАСПАДА, промежуток времени, в течение которого распадается половина данного количества ядер радиоактивного изотопа (которые превращаются в другой элемент или изотоп). Измеряется только период полураспада, так как полного распада не происходит. Период полураспада остается постоянным при любой температуре и давлении, но сильно отличается у разных изотопов.
Вопрос 36. Правило Вант-Гоффа — эмпирическое правило, позволяющее в первом приближении оценить влияние температуры на скорость химической реакции в небольшом температурном интервале (обычно от 0 °C до 100 °C). Я. Х. Вант-Гофф на основании множества экспериментов сформулировал следующее правило:
| При повышении температуры на каждые 10 градусов константа скорости гомогенной элементарной реакции увеличивается в два—четыре раза. |
Уравнение, которое описывает это правило, следующее:

где  — скорость реакции при температуре
— скорость реакции при температуре  ,
,  — скорость реакции при температуре
— скорость реакции при температуре  ,
,  — температурный коэффициент реакции (если он равен 2, например, то скорость реакции будет увеличиваться в 2 раза при повышении температуры на 10 градусов).
— температурный коэффициент реакции (если он равен 2, например, то скорость реакции будет увеличиваться в 2 раза при повышении температуры на 10 градусов).
Следует помнить, что правило Вант-Гоффа применимо только для реакций с энергией активации 60-120 кДж/моль в температурном диапазоне 10-400oC. Правилу Вант-Гоффа также не подчиняются реакции, в которых принимают участие громоздкие молекулы, например, белки в биологических системах. Температурную зависимость скорости реакции более корректно описывает уравнение Аррениуса.
Из уравнения Вант-Гоффа температурный коэффициент вычисляется по формуле:
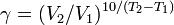
Вопрос 37. Уравне́ние Арре́ниуса устанавливает зависимость константы скорости  химической реакции от температуры
химической реакции от температуры  .
.
Согласно простой модели столкновений, химическая реакция между двумя исходными веществами может происходить только в результате столкновения молекул этих веществ. Но не каждое столкновение ведёт к химической реакции. Необходимо преодолеть определённый энергетический барьер, чтобы молекулы начали друг с другом реагировать. То есть молекулы должны обладать некой минимальной энергией (энергия активации  ), чтобы этот барьер преодолеть. Из распределения Больцманадля кинетической энергии молекул известно, что число молекул, обладающих энергией
), чтобы этот барьер преодолеть. Из распределения Больцманадля кинетической энергии молекул известно, что число молекул, обладающих энергией  , пропорционально
, пропорционально  . В результате скорость химической реакции представляется уравнением, которое было получено шведским химиком Сванте Аррениусом из термодинамических соображений:
. В результате скорость химической реакции представляется уравнением, которое было получено шведским химиком Сванте Аррениусом из термодинамических соображений:

Здесь  характеризует частоту столкновений реагирующих молекул,
характеризует частоту столкновений реагирующих молекул,  — универсальная газовая постоянная.
— универсальная газовая постоянная.
В рамках теории активных соударений  зависит от температуры, но эта зависимость достаточно медленная:
зависит от температуры, но эта зависимость достаточно медленная:

Оценки этого параметра показывают, что изменение температуры в диапазоне от 200 °C до 300 °C приводит к изменению частоты столкновений  на 10 %.
на 10 %.
В рамках теории активированного комплекса получаются другие зависимости  от температуры, но во всех случаях более слабые, чем экспонента.
от температуры, но во всех случаях более слабые, чем экспонента.
Уравнение Аррениуса стало одним из основных уравнений химической кинетики, а энергия активации — важной количественной характеристикой реакционной способности веществ.
Энергия активации в химии и биологии — минимальное количество энергии, которое требуется сообщить системе (в химии выражается в джоулях на моль), чтобы произошла реакция.
Вопрос 38. Химическим равновесием называется такое состояние химической системы, при котором количества исходных веществ и продуктов не меняются со временем.
Константа равновесия- величина, определяющая для данной химической реакции соотношение между термодинамическими активностями исходных веществ и продуктов в состоянии химического равновесия.
Смещение химического равновесия:
Положение химического равновесия зависит от следующих параметров реакции: температуры, давления и концентрации. Влияние, которое оказывают эти факторы на химическую реакцию, подчиняется закономерности, которая была высказана в общем виде в 1885 году французским ученым Ле-Шателье.
Факторы, влияющие на химическое равновесие:
1) температура
При увеличении температуры химическое равновесие смещается в сторону эндотермической (поглощение) реакции, а при понижении - в сторону экзотермической (выделение) реакции.
CaCO3=CaO+CO2 -Q t↑ →, t↓ ←
N2+3H2↔2NH3 +Q t↑ ←, t↓ →
2) давление
При увеличении давления химическое равновесие смещается в сторону меньшего объёма веществ, а при понижении - в сторону большего объёма. Этот принцип действует только на газы, т.е. если в реакции участвуют твердые вещества, то они в расчет не берутся.
CaCO3=CaO+CO2 P↑ ←, P↓ →
1моль=1моль+1моль
3) концентрация исходных веществ и продуктов реакции
При увеличении концентрации одного из исходных веществ химическое равновесие смещается в сторону продуктов реакции, а при повышении концентрации продуктов реакции - в сторону исходных веществ.
S2+2O2=2SO2 [S],[O]↑ →, [SO2]↑ ←
Вопрос 40. Принцип Ле-Шателье:
Принцип Ле Шателье — Брауна (1884 г.) — если на систему, находящуюся в устойчивом равновесии, воздействовать извне, изменяя какое-либо из условий равновесия (температура, давление, концентрация, внешнее электромагнитное поле), то в системе усиливаются процессы, направленные на компенсацию внешнего воздействия.
Влияние температуры. Для реакций, идущих с уменьшением энтальпии (экзотермических), повышение температуры будет препятствовать протеканию прямого процесса, то есть смещать реакцию в сторону исходных веществ. Эндотермические реакции при этом будут смещаться в сторону конечных продуктов. Например, при обычных условиях реакция N2 + O2 не идет (ΔH > 0), но повышение температуры может сделать эти реакцию осуществимой. Реакция CO + 1/2O2 = CO2, ΔH < 0 с повышением температуры будут смещаться в сторону исходных веществ.
Влияние давления. Если реагируют газообразные вещества, то при неизменном числе молей начальных и конечных реагентов повышение общего давления не приведет к смещению равновесия. Если число молей при реакции меняется, то изменение общего давления приведет к смещению равновесия. В частности, реакция 2CO + O2 = 2CO2, протекающая с уменьшением Δn, при повышении общего давления сместится в сторону образования СO2.
Влияние концентраций. В тех реакциях, в которых лучше оперировать концентрациями (реакции в растворах), увеличение концентраций исходных веществ приводит к смещению равновесия в сторону конечных продуктов и наоборот. Так, в реакции этерификации (образование сложного эфира)
Вопрос 41. ) Химическая теория катализа, основанна на знаниях, полученных в ходе изучения элементарных химических реакций, как модельных (взаимодействие специально полученных химически активных частиц), так и при исследовании элементарных стадий сложных каталитических превращений.
КАТАЛИЗАТОРЫ-вещества, изменяющие скорость хим. реакцииции или вызывающие ее, но не входящие в состав продуктов.
Катализаторы подразделяются на гомогенные и гетерогенные. Гомогенный катализатор находится в одной фазе с реагирующими веществами, гетерогенный — образует самостоятельную фазу, отделённую границей раздела от фазы, в которой находятся реагирующие вещества.
ПОЧЕМУ КАТАЛИЗАТОР УСКОРЯЕТ ПРЕВРАЩЕНИЕ
Еще в XIX веке в поисках ответа на этот вопрос было высказано много разных предположений: фазовые превращения и уплотнение реагентов у поверхности катализаторов; передача энергии от катализатора; из- менение максвелл-больцмановского распределения по энергии. Эти факторы могут играть роль, но не всегда. В основу современных представлений положена идея образования в ходе превращения нового промежуточного соединения для получения которого требуется меньше энергии .
Дата добавления: 2015-01-29; просмотров: 336; Мы поможем в написании вашей работы!; Нарушение авторских прав |