
КАТЕГОРИИ:
АстрономияБиологияГеографияДругие языкиДругоеИнформатикаИсторияКультураЛитератураЛогикаМатематикаМедицинаМеханикаОбразованиеОхрана трудаПедагогикаПолитикаПравоПсихологияРиторикаСоциологияСпортСтроительствоТехнологияФизикаФилософияФинансыХимияЧерчениеЭкологияЭкономикаЭлектроника
Влияние состава металла на растворимость газов
Примеси могут влиять на растворимость газа:
1термодинамчески (на активность газа), если примеси склонны образовывать с газом соединения, то они образовывают прочные связи и за счет этого уменьшается активность газа в металле, следовательно, растворимость увеличивается.
{ Г2 }=2[ Г ]
[ Г ]=(( Кр* p{Г2 } )/f [ Г ])^(0,5)
f [ Г ] = f(состава) f-коэффициент активности.
[%i] растет с уменьшением fг меньше единицы, растворимость [ Г ] увеличивается.
Углерод везде способствует уменьшению растворимости
47. Коэффициент распределения фосфора между металлом и шлаком, его зависимость от температуры и состава фаз. В каких металлургических агрегатах проводится, в основном, дефосфорация стали? Чем определяется полнота дефосфорации? (см. лекции Климов 129-130)
Более полное представление о равновесии процесса дефосфорации дает коэффициент распределения LP= (Р2О5)/[Р]2. Возрастание этой величины свидетельствует о повышении обесфосфоривающей способности шлака.
Во всех случаях окисление растворенного в металле фосфора сопровождается выделением тепла. При окислении фосфора газообразным кислородом выделяется значительное количество тепла. Для некоторых процессов, связанных с переделом фосфористых чугунов (например, томасовского), благодаря окислению фосфора происходит нагрев металла. При повышении температуры могут создаться благоприятные условия для восстановления фосфора. Повышение окисленности шлака способствует процессам окисления фосфора и, наоборот, снижение активности оксидов железа в шлаке затрудняет протекание этих процессов.
Влияние состава металла. Присутствие в металле повышенных количеств легкоокисляющихся примесей (Si, Mn, С и др.) затрудняет процесс удаления фосфора, так как эти примеси взаимодействуют с оксидами железа и окисленность шлака снижается. В середине плавки при максимальной скорости окисления углерода, сопровождающейся снижением активности оксидов железа и замедлением роста основности шлака, содержание фосфора в расплаве существенно не изменяется, а иногда может наблюдаться даже некоторое его восстановление.
По мере снижения концентрации углерода в расплаве, роста окис-ленности шлака и его основности наблюдается дальнейшее удаление фосфора. Высокая температура расплава в этот период несколько снижает интенсивность его окисления, но высокоосновный железистый шлак обеспечивает получение металла с низким (<0,02 % Р) содержанием фосфора.
Большое значение имеет количество шлака, поскольку при одной и той же достигнутой величине коэффициента распределения, количество фосфора, перешедшего в шлак, будет тем больше, чем больше масса шлака. Поэтому при повышенном содержании фосфора в чугуне обычно увеличивают количество конвертерного шлака.
Дефосфорация в основном проводится в Электро-дуговых печахВ течение всего окислительного периода идет дефосфорация Ме по реакции 2[P] + 5(FeO) + 3(CaO) = (3CaO·P2O5) + 5Fe + 767290 Дж/моль. Для успешного протекания этой реакции необходимы высокие основность шлака и концентрация окислов железа в нем, а также пониженная Т. Именно эти условия создаются при совместном введении в печь извести и руды. Полнота дефосфорации повышается в результате перемешивания шлака и Ме при кипении и вследствие непрерывного обновления шлака. Коэффициент распределения фосфора изменяется в пределах от 50 до 100 обычно возрастая приросте основности и окисленности шлака. Эффективным способом ускорения дефосфорации, повышения степени ее полноты и сокращения длительности окислительного периода зарекомендовало себя вдувание в ванну дефосфорирующих порошкообразных смесей в струе кислорода.
Допустимо 0,03-0,05% - прив. К охрупчиванию Me попадает с рудами.
P и Me как правило нах-ся в форме фосфида Fe2P, в шлаке – P2O5 или PO43-.
-5e + Fe2P + 4(O2-) → 2[Fe] + (PO43-) – окисление
2,5(Fe2+) + 5e → 2,5[Fe]
[Fe2P] + 2,5 (Fe2+) + 4(O2-) → (PO43-) + 4,5[Fe]

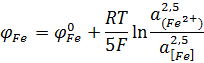
φp = φFe

£P=f(T) T↑ £P↓,
(£-коэффициент распределения, £p'-показатель распределения)
Дефосфор. прав-ся при пониженных температурах
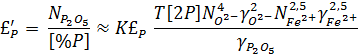
a[Fe] → 1
£p'↑ =>NO2- - ↑ R ↑ - повыш. Основности шлака
CaO ↑ или FeO ↑ - const полимериз. расх-ся на 3 порядка.
NFe2+ ↑
Для дефосфорации исп-ся железистые шлаки => необх. Подобрать оптимальный состав.
Дата добавления: 2015-04-18; просмотров: 315; Мы поможем в написании вашей работы!; Нарушение авторских прав |