
КАТЕГОРИИ:
АстрономияБиологияГеографияДругие языкиДругоеИнформатикаИсторияКультураЛитератураЛогикаМатематикаМедицинаМеханикаОбразованиеОхрана трудаПедагогикаПолитикаПравоПсихологияРиторикаСоциологияСпортСтроительствоТехнологияФизикаФилософияФинансыХимияЧерчениеЭкологияЭкономикаЭлектроника
Билет №6
1. Взаимное влияние атомов и способы его передачи в молекулах органических соединений. Сопряжённые системы с открытой цепью. Сопряжённые системы с замкнутой цепью. Ароматичность.
Наличие в молекуле полярной σ-связи вызывает поляризацию ближайших σ-связей и ведёт к возникновению частичных зарядов на соседних атомах (обозначаются буквой δ с указанием знака: «+» или «-»). Таким образом, заместители вызывают поляризацию не только «своей», но и соседних σ-связей. Вид передачи электронного влияния заместителей за счёт смещения электронов σ-связей принято называть индуктивным эффектом (I-эффект). Из-за слабой поляризуемости σ-связи индуктивный эффект затухает через три-четыре связи в цепи. Направление индуктивного эффекта заместителя принято качественно оценивать путём сравнения с атомом водорода, индуктивный эффект которого принят за ноль. Графически его действие обозначают прямой стрелкой, совпадающей с положением валентной чёрточки и направленной в сторону более электроотрицательного атома. Заместители, притягивающие электронную плотность сильнее, чем атом водорода, принято называть электроноакцепторами, а их индуктивный эффект – отрицательным (-I). Такие заместители снижают электронную плотность системы. К ним относятся большинство функциональных групп и катионы. Соответственно, заместители, смещающие электронную плотность в сторону атома углерода цепи, проявляет положительный электронный эффект (+I) и являются электроноакцепторами. Такие заместители ведут к повышению электронной плотности. К их числу относятся алкильные группы, металлы и анионы.
В сопряжённых системах в передаче электронного влияния основную роль играют π-электроны делокализованных ковалентных связей. Эффект, проявляющийся в смещении электронной плотности делокализованной (сопряжённой) π-системы, называется мезомерным (М-эффект), или эффектом сопряжения. При этом заместитель сам является участником сопряжённой системы. Он может вносить в систему сопряжения π-связь, неподелённую пару электронов гетероатома, валентную или заполненную одним или двумя электронами р-атомную орбиталь. Аналогично индуктивному эффекту, заместители, повышающие электронную плотность в сопряжённой системе, проявляют +М-эффект и являются электронодонорами (им обладают заместители, содержащие атомы с неподелённой парой электроновили целым отрицательным зарядом), а понижающие электронную плотность проявляют –М эффект и являются электроноакцепторами (им обладают ненасыщенные группировки и положительно заряженные атомы). Графически смещение электронной плотности обозначается изогнутыми стрелками, начало которых показывает, какие р- или π-электроны смещаются, а конец – связь или атом, к которым они смещаются. В отличие от индуктивного, мезомерный эффект передаётся по системе сопряжённых связей на значительно большее расстояние.
В таблице ниже указаны индуктивный и мезомерный эффекты некоторых заместителей, а также их результирующее действие.
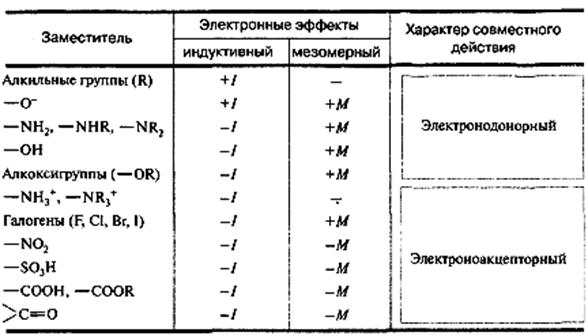
Ковалентная связь может быть локализованной и делокализованной. О последней говорят в тех случаях, когда молекулярная орбиталь ковалентной связи охватывает более двух атомов. В большинстве случаев делокализованные связи являются π-связями. Они характерны для сопряжённых систем – соединений, содержащих кратные связи, отделённых одной простой связью от соседнего атома, имеющего р-орбиталь. Участвующие в сопряжении делокализованные р-орбитали могут принадлежать либо двум и более π-связям, либо π-связи и одному атому с р-орбиталью. В соответствии с этим разделяют π,π-сопряжение и р,π-сопряжение. Система сопряжения может быть открытой или замкнутой и содержать не только атомы углерода, но и гетероатомы.
Простейшим представителем π,π-сопряжённых систем с углеродной цепью служит бутадиен-1,3.
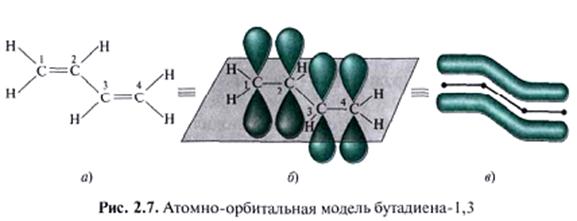
Все атомы углерода в молекуле находятся в состоянии sp2-гибридизации, а длины связей из-за наличия сопряжения имеют промежуточные значения.
В p,π-сопряжённых системах с углеродной цепью сопряжение может осуществляться при наличии рядом с π-связью атома углерода с негибридизированной р-орбиталью. Очевидно, что такими системами не могут быть нейтральные молекулы, а могут быть только промежуточные частицы – карбанионы, карбокатионы, свободные радикалы.
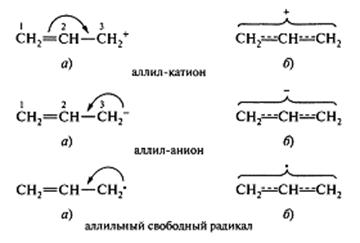
По приведённой схеме видно, что сопряжение приводит к выравниванию связей и зарядов в реальной молекуле по сравнению с идеальной (резонансной), но несуществующей структурой.
Образование сопряжённой системы – энергетически выгодный процесс.
Среди циклических сопряжённых систем наибольший интерес представляюе группа соединений, отличительной чертой которых является повышенная термодинамическая устойчивость по сравнению с сопряжёнными открытыми системами. Эти соединения обладают и другими особыми свойствами, совокупность которых объединяется общим понятием ароматичность. К ним, в первую очередь, относятся способность таких формально ненасыщенных соединений вступать в реакции замещения, а не присоединения, устойчивость к действию окислителей и температуры. Циклы этих систем по химическому строению могут быть как только углеродными, так и содержащими гетероатомы, и в них может осуществляться как π,π-, так и р,π-сопряжение.
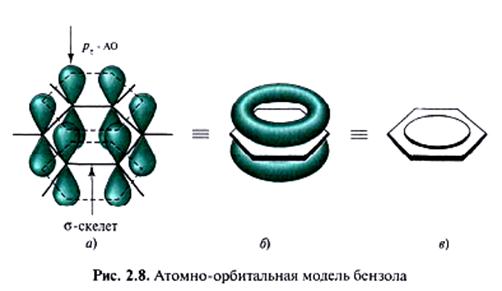
Соединение ароматично, если оно имеет плоский замкнутый цикл и сопряжённую π-электронную систему, охватывающую все атомы цикла и содержащую (4n + 2) π-электронов. Это правило применимо ко всем плоским конденсированным системам, в которых нет атомов, общих более чем для двух циклов.
В гетероциклических ароматических соединениях встречаются оба вида сопряжения. π,π-сопряжение характерно для шестичленных гетероциклов с одним или несколькими гетероатомами. Простейшим их представителем является пиридин, содержащий в цикле один атом азота. Этот атом находится в состоянии sp2-гибридизации и поставляет в ароматический секстет один р-электрон. Неподелённая электронная пара на sp2-гибридной орбитали обуславливает свойства пиридина как основания. Атом азота с таким электронным строением принято называть пиридиновым. В результате большей электроотрицательности по сравнению с атомом углерода пиридиновый атом азота понижает электронную плотность на атомах углерода ароматического кольца. Поэтому системы с пиридиновым атомом азота называют π-недостаточными. р,π-сопряжение осуществляется в пятичленных гетероциклах с атомами азота, кислорода, серы. Довольно часто в составе биологически значимых соединений встречается гетероцикл с одним атомом азота – пиррол. В пирроле от атома азота в ароматический секстет включается находящаяся на негибридизированной р-орбитали пара электронов. Три электрона на sp2-гибридных орбиталях участвуют в образовании трёх σ-связей. Атом азота в таком электронном состоянии получил название пиррольного. Шестиэлектронное облако в пирроле делокализовано на пяти атомах цикла, поэтому пиррол представляет собой π-избыточную систему.
2. Декарбоксилирование α-аминокислот – путь к образованию биогенных аминов и биорегуляторов (коламин, гистамин, триптамин, серотонин, кадаверин, β-аланин, γ-аминомасляная кислота).
Процесс декарбоксилирования α-аминокислот ведёт к образованию биогенных аминов.

Α-аминокислоты содержат в α-положении к карбоксильной группе электронакцепторную аминогруппу (точнее, протонированую аминогруппу NH3+), в связи с чем способны к декарбоксилированию. В лабораторных условиях эта реакция протекает при нагревании α-аминокислот в присутствии поглотителей диоксида углерода, например, гидроксида бария.
В организме процесс проиходит с участием ферментов декарбоксилаз и кофермента пиридоксальфосфата (см. билет №4, вопрос 2). Эта реакция осуществляется за счёт разрава в альдимине I полярной связи между α-углеродным атомом и карбоксилатной группой. Промежуточная «хиноидная» форма за счёт присоединения протона превращается в альдимин Ia, в результате гидролиза которого получаются пиридоксальфосфат и амин.

Биогенные амины в организме выполняют важные биологические функции. Например, получающийся при декарбоксилировании гистидина биогенный амин гистамин обладает широким спектром биологического действия и участвует в регуляции жизненно важных функций организма. γ-аминомасляная кислота, образующаяся при декарбоксилировании глутаминовой кислоты, является нейромедиаторром. Большое биологическое значение имеет декарбоксилирование многих природных α-аминокислот – серина, цистеина, лизина, триптофана, аспарагиновой кислоты и др. На всякий случай привожу формулы некоторых биогенных аминов и биорегуляторов, получающихся в организме таким образом.


Триптамин Гистамин

Кадаверин: NH2(CH2)5NH2
β-аланин: NH2 – CH2 – CH2 – COOH
γ-аминомасляная кислота: NH2(CH2)3COOH
Коламин: HO – CH2 – CH2 – NH2
Серотонин
3. Напишите проекционные формулы стереоизомеров α-броммасляного альдегида. Назовите их по заместительной номенклатуре ИЮПАК.
CH3 – CH2 – C*H – COH
|
Br
COH COH
 |

 H Br Br H
H Br Br H
 C2H5 C2H5
C2H5 C2H5
D-2-бромбутаналь L-2-бромбутаналь
4. Напишите уравнения реакций ацетилирования тиофена ацетилхлоридом и нитрования пиридина азотной кислотой. Что общего в их механизмах?

Итак, обе предложенные реакции протекают по механизму электрофильного замещения, и поэтому имеют все свойства, характерные для данных реакций. В частности, они имеют ряд общих стадий: генерирование электрофильной частицы, атака сгенерированной частицей ароматического субстрата с образованием нестойкого π-комплекса, образование σ-комплекса, отщепление от образовавшегося комплекса протона.
5. Рассмотрите возможные пути превращения 3-хлорбутаналя в присутствии этоксида натрия. Приведите уравнения реакций, укажите механизмы, назовите продукты реакции.

Первые две реакции идут по механизму мономолекулярного нуклеофильного замещения, третья – нуклеофильного присоединения.
Продукты:
1) гидрид натрия, этил-3-хлорбутират;
2) хлорид натрия, 3-этоксибутаналь;
3) 1-этокси-3-хлорбутират натрия.
Дата добавления: 2015-02-10; просмотров: 1313; Мы поможем в написании вашей работы!; Нарушение авторских прав |