
КАТЕГОРИИ:
АстрономияБиологияГеографияДругие языкиДругоеИнформатикаИсторияКультураЛитератураЛогикаМатематикаМедицинаМеханикаОбразованиеОхрана трудаПедагогикаПолитикаПравоПсихологияРиторикаСоциологияСпортСтроительствоТехнологияФизикаФилософияФинансыХимияЧерчениеЭкологияЭкономикаЭлектроника
Физико-химические методы. Наиболее доступным в школьных условиях является качественныйанализ
Наиболее доступным в школьных условиях является качественныйанализ. Он всегда предшествует количественному, так как выбор метода количественного определения зависит от данных качественного анализа [8].
Качественные реакции на катионы
Li+ - пламя (красное)
Na+- пламя (желтое)
К+ - пламя (фиолетовое)
Са2+- пламя (кирпично-красное)
карбонат-ионы (белый осадок)
оксалат-ионы (белый осадок)
Ва2+- пламя (желто-зеленое)
сульфат-ионы (белый осадок)
хромат-ионы (желтый осадок)
Сu2+-пламя (зеленое)
в водном растворе гидратированные ионы [Cu(H2O)4]2+ имеют голубую окраску
водный раствор аммиака (сине-фиолетовая окраска)
Рb2+-сульфид-ионы (черный осадок)
йодид-ионы (желтый осадок)
хромат-ионы (желтый осадок)
Ag+ - хлорид-ионы (белый осадок)
хромат-ионы (кирпично-красный осадок)
Fe2+ - красная кровяная соль (синий осадок)
Fe3+ - желтая кровяная соль (синий осадок)
роданид-ионы (красное окрашивание)
Cd2+ - сульфид-ионы (желтый осадок)
Zn2+ - сульфид-ионы (белый осадок)
NH4+- раствор щелочи (запах аммиака)
[Hg]2+- раствор щелочи (черный осадок)
хромат-ионы (красный осадок)
Hg2+- сульфид-ионы (черный осадок)
йодид-ионы (красный осадок)
Sn2+ - сероводород (темно-коричневый осадок)
Sn4+ - сероводород (желтый осадок)
Качественные реакции на анионы
 - соли бария (белый осадок)
- соли бария (белый осадок)
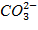 - соляная или серная кислоты (выделяется углекислый газ)
- соляная или серная кислоты (выделяется углекислый газ)
известковое молоко (белый осадок)
 - магнезиальная смесь: MgCI2+ NH4OH + NH4Cl (белый осадок)
- магнезиальная смесь: MgCI2+ NH4OH + NH4Cl (белый осадок)
нитрат серебра (желтый осадок)
 - разбавленные растворы кислот (студенистый осадок)
- разбавленные растворы кислот (студенистый осадок)
соли аммония (то же)
 - пламя (зеленое окрашивание)
- пламя (зеленое окрашивание)
и  - нитрат серебра (желтый осадок)
- нитрат серебра (желтый осадок)
 - соли свинца (желтый осадок)
- соли свинца (желтый осадок)
хлорная вода + крахмал (синее окрашивание)
Cl – - нитрат серебра (белый осадок)
Вr– - нитрат серебра (желтоватый осадок)
 - металлическая медь в концентрированной серной кислоте (газ бурого цвета)
- металлическая медь в концентрированной серной кислоте (газ бурого цвета)
металлический алюминий в сильнощелочной среде (запах аммиака)
смесь H2SO4 + FeSO4 (окраска от фиолетовой до коричневой)
 - сульфаниловая кислота + α-нафтиламин (красное окрашивание)
- сульфаниловая кислота + α-нафтиламин (красное окрашивание)
 - соли бария (желтый осадок)
- соли бария (желтый осадок)
и  - соли свинца (черный осадок)
- соли свинца (черный осадок)
S2– - соли кадмия (желтый осадок)
Из количественныхметодов в школьной практике могут быть рекомендованы гравиметрический, титриметрический (объемный) и метод визуальной колориметрии.
Дата добавления: 2015-04-11; просмотров: 370; Мы поможем в написании вашей работы!; Нарушение авторских прав |