
КАТЕГОРИИ:
АстрономияБиологияГеографияДругие языкиДругоеИнформатикаИсторияКультураЛитератураЛогикаМатематикаМедицинаМеханикаОбразованиеОхрана трудаПедагогикаПолитикаПравоПсихологияРиторикаСоциологияСпортСтроительствоТехнологияФизикаФилософияФинансыХимияЧерчениеЭкологияЭкономикаЭлектроника
РАСЧЕТ МАССЫ РАСТВОРЕННЫХ ВЕЩЕСТВ ПО РЕЗУЛЬТАТАМ ТИТРОВАНИЯ
Прямое титрование осуществляется двумя методами: методом отдельных навесок и методом пипетирования
Метод пипетирования
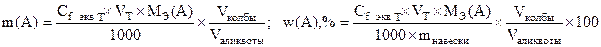
Метод отдельных навесок
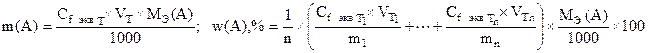
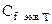 – молярная концентрация эквивалента (нормальность) титранта, моль/л; VТ – объем титранта, мл; МЭ(А) – молярная масса эквивалента (эквивалент) титруемого вещества А; m1, …mn – навески; n – число навесок.
– молярная концентрация эквивалента (нормальность) титранта, моль/л; VТ – объем титранта, мл; МЭ(А) – молярная масса эквивалента (эквивалент) титруемого вещества А; m1, …mn – навески; n – число навесок.
Пример: В колбе на 200 см3 было растворено 0,6596 г. Na2CO3 на титрование 15,00 см3 полученного раствора было израсходовано 13,9 см3 HCl. Определить ТHCl и Сf экв. HCl.
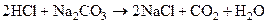
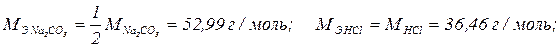
 ;
;
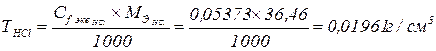
В методах обратного титрования массу и массовую долю определяемого вещества рассчитывают по формулам:
В методе пипетирования:
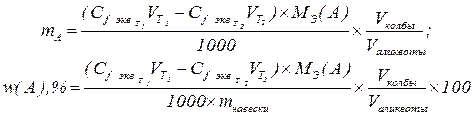
В методе отдельных навесок:
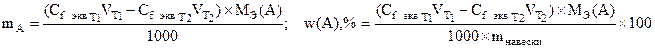
Метод замещения используется тогда, когда определяемое вещество с титрантом не взаимодействует или их взаимодействие протекает нестехиометрично. Расчет результатов титрования проводят по формулам, приведенным выше.
Пример. Из колбы вместимостью 100,0 см3,содержащей раствор хлорида аммония взяли аликвоту 10,00 см3. К анализируемому раствору хлорида аммония прибавили избыток раствора формальдегида. Образовавшиеся в результате реакции ионы водорода оттитровали 12,5 см3 0,1000 М NaOH. Рассчитать массу хлорида аммония. Проявлением слабокислотных свойств формальдегида пренебречь.
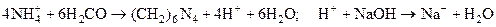
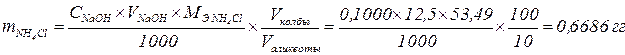
Дата добавления: 2015-04-15; просмотров: 553; Мы поможем в написании вашей работы!; Нарушение авторских прав |