
КАТЕГОРИИ:
АстрономияБиологияГеографияДругие языкиДругоеИнформатикаИсторияКультураЛитератураЛогикаМатематикаМедицинаМеханикаОбразованиеОхрана трудаПедагогикаПолитикаПравоПсихологияРиторикаСоциологияСпортСтроительствоТехнологияФизикаФилософияФинансыХимияЧерчениеЭкологияЭкономикаЭлектроника
Влажный воздух
Вариант 1
1.1Начальное состояние влажного воздуха при атмосферном давлении 700 мм рт.ст. задано параметрами: Т= 300К и φ=70%. Воздух охлаждается до температуры Т=280 К и φ=100%. Определить, сколько влаги выпадает из каждого килограмма воздуха.
1.2Определить точку, изображающую данное состояние воздуха и значения остальных параметров, если tв=20°С и φ=30%.
1.3Приточной системой подается в помещение воздух с температурой 10°С и относительной влажностью φ=50%. Удаляется воздух из помещения с температурой 16°С. В помещение выделяются 10 кг/ч пара при давлении 2 атм и 10000 ккал/ч тепла от различных источников. Построить процесс поглощения тепла и влаги в I-d диаграмме и определить параметры и количество удаляемого воздуха.
Вариант 2
2.1Известно, что температура воздуха 18°С и относительная влажность φ=50%. Определить остальные параметры воздуха.
2.2Воздух при t=18°С, φ=50% и d=6,4 г/кг увлажняется до 90%. Определить параметры воздуха после увлажнения, количество испарившейся воды и температуру увлажняющей воды, если применена рециркуляция воды.
2.3 Определить точку росы для воздуха с параметрами: t=18°С, φ=50%.
Контрольные квалификационные задания по дисциплине «Термодинамика»
Тест 1
1. Назвать параметры состояния, доступные измерению.
Ответ: энтальпия, давление, энтропия, температура, внутренняя энергия, удельный объем, энергия, работа.
2. Уравнение Ван-дер-Ваальса.
1). (Р + π)(V-b)=RT
2). РV=RT(1-  )
)
3). (Р+а/V2)(V-b)=RT
3. Что есть дифференциал dl?
1). - есть полный дифференциал;
2). - есть элементарная работа в бесконечно малом процессе расширения (сжатия)
4. Всегда ли энтальпия является теплосодержанием?
1). Всегда;
2). Нет.
5. За счет, какой энергии производится работа в адиабатном процессе?
1). За счет подвода энергии извне;
2). За счет внутренней энергии.
6. Какой процесс изображен на диаграмме?

7. Указать какое неравенство (угловой коэффициент какого процесса больше) справедливо.
1). 
2). 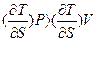
8. Универсальная газовая постоянная
Ответ: 8000 Дж/кмоль 0К; 8310 Дж/кмоль 0К; 7310 Дж/кмоль 0К.
9. Укажите формулу Майера:
1). К=Ср/Сv;
2). Ср-Сv=R;
3). РV=const.
10. Как называется термодинамическая система, которая может обмениваться энергией с окружающей средой?
1). Замкнутая;
2). Разомкнутая.
11. Определить среднюю теплоемкость и расход теплоты для нагревания 20 кг кислорода О2 от 600 до 18000С. Для расчета использовать данные из таблицы теплоемкостей.
t1=6000С; Срm1=31,79 кДж/кмоль град;
t2=18000С; Срm2=34,84 кДж/кмоль град.
12. Определить газовую постоянную смеси газов, состоящей из 1 м3 генераторного газа и 1,5 м3 воздуха, взятых при нормальных условиях и найти парциальные давления составляющих смеси. Плотность генераторного газа принять равной 1,2кг/м3.
13. Смесь СО2 и N2 находится в резервуаре при температуре 370С и давлении 1400 Мбар. Парциальное давление углекислоты равно 350 Мбар. Найти массовый и объемный состав смеси, ее молекулярный вес, газовую постоянную и плотность.
Тест 2
1. Какое давление является термодинамическим параметром состояния?
Ответ: абсолютное давление, избыточное давление, вакуум.
2. Что понимают под истинной или мгновенной теплоемкостью?
1). Количество теплоты, подведенной к рабочему телу;
2). Предел отношения подводимой к газу теплоты Δq к изменению температуры Δt, при Δt→0.
3. Уравнение работы расширения:
1) 
2) 
4. Выражение первого закона термодинамики в изобарном процессе:
1).dq=du$
2).Cv(t2-t1)+P(V2-V1).
5. Чему равно изменение внутренней энергии рабочего тела в замкнутом процессе?
1) ΔU=Cv(t2-t1);
2) ΔU=0.
6. К каким заключениям приводит анализ циклов Карно?
1) Тепловую энергию нельзя полностью преобразовать в работу и перенос тепловой энергии с низшего теплового уровня на высший обязательно сопровождается затратой работы;
2) Вся подведенная энергия расходуется на совершение работы и изменение энергии.
7. Какой процесс является изохорным на диаграмме:

8. Как задаются смеси газов?
Ответ: массовыми долями, процентами, объемными долями.
9. Как называется термодинамическая система, которая не может обмениваться энергией с окружающей средой?
1). Замкнутая;
2).Разомкнутая.
10. Из каких процессов состоит цикл Карно?
1). Из 2 адиабатных и 2 изотермических;
2). Из 2 изохорных и 2 изобарных.
11. Начальное состояние азота задано параметрами t=2000С, U=1,9 м3/кг. Азот нагревается в процессе при постоянном давлении, причем объем азота увеличивается до 5,7 м3/кг. Определить конечную температуру.
12. Объемный состав сухих продуктов сгорания топлива следующий: СО2=12,3%, О2=7,2%, N2=80,5%. Найти молярную массу и газовую постоянную, а также плотность и удельный объем продуктов сгорания при В=100 кПа и t=8000С.
Тест 3
1. Является ли удельный объем осредненной макроскопической величиной?
2. Уравнение состояния смеси газов, заданной объемными долями:
1). PiVсм=miRiTсм;
2). PсмVсм=mсм 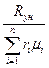 Tсм;
Tсм;
3).  PсмVсмriμi=
PсмVсмriμi=  mimсмRунТсм.
mimсмRунТсм.
3. Перечислить функции процесса: энтальпия, работа, теплота, энтропия, температура, давление, внутренняя энергия.
Какая система координат называется рабочей:
P-V, T-S, i-S, i-d.
4. Когда энтальпию можно назвать теплосодержанием?
1) Во всех термодинамических процессах;
2) Когда процесс нагревания или охлаждения изобарный.
5. Какой процесс изображен на диаграмме?

6. Указать показатель политропы:
1). n=(c-cp)/(c-cv);
2) k=cp/cv
7. От каких термодинамических параметров зависит термический к.п.д. цикла Карно?
1) От абсолютных давлений теплоприемника и теплоотдатчика;
2) От абсолютных температур.
8. Какой процесс изображен на диаграмме?

9. Что выражает уравнение Ср-Сv=R.
1) Взаимосвязь между теплоемкостями реального газа;
2) Взаимосвязь между теплоемкостями идеального газа.
10. В трубках воздухоподогревателя парогенератора проходит воздух в количестве приведен. В нормальные условия V=11000 м3/ч температура на входе 450С. Какова температура воздуха на выходе из воздухоподогревателя, если топочные газы сообщают воздуху количество теплоты Q=2600 МДж, определить работу расширения воздуха, которую он совершает в течении 1 ч. Процесс подогрева воздуха изобарный при р=1 бар Нср=29,09+0,00241t.
11. 0,2 м3 воздуха с начальной температурой 180С подогревают в цилиндре d=0,5 м при постоянном давлении равном 0,2 МПа до температуры 2000С. Определить работу расширения, перемещение поршня h и количество затраченной теплоты. Считать зависимость линейной.
12. воздух в количестве 5 м3/мин при t=200С и давлении р=110Н/м2 поступает в компрессор, где сжимается, затем проходит по трубам холодильника и охлаждается водой. Определить часовой расход охлаждающей воды, если на выходе из компрессора воздух р=8 бар, t=1800С, температура за холодильником 350С при этом Δt воды =180С.
13. выражение первого закона термодинамики при изохорном процессе6
1)dq=du+pdv;
2) q=Δu.
Тест 4
1. Единица измерения температуры в абсолютной термодинамической стоградусной температурной шкале.
Ответ: градус Кельвина, градус Цельсия, градус Реомюра, градус Фаренгейта.
2. R=Rун/μ
Ответ: газовая постоянная, газовая постоянная азота.
3. По какому уравнению вычисляют теплоемкость для двухатомных газов?
1) С=а+bt;
2) С=а+bt+сt2+dt3.
4. Зависит ли изменение внутренней энергии от вида процесса?
1). Да;
2). Нет.
5. Для какого процесса справедливо выражение q=i2-i1?
1). Изотермический;
2). Изохорный;
3). Изобарный;
4). Адиабатный.
6. Уравнение адиабатного процесса:
1). Т=const;
2).V=const;
3).P=const;
4).q=const.
7. Может ли термический к.п.д. быть больше единицы?
1). Да;
2). Нет.
8. При совершении обратного цикла что происходит с работой?
1) Затрачивается;
2) Производится.
9. Что называется энтропией?
1).Полный дифференциал некоторой термодинамической функции, характеризующей состояние рабочего тела;
2). Функцию процесса.
10. Какой процесс является изобарным на диаграмме?

11. Вентиляционная система помещения с внутренним V=4000 м3, осуществляет 4-х кратный объем воздуха в 1 час. Определить часовой расход горючего газа на нагревание наружного воздуха в калориферной камере от -150С до +250С. Если Рвоз.=780 мм.рт.ст. теплотворная способность газа 35000 Дж/кг м3, n калориф. q=80%.
12. Определить плотность воздуха и водорода при нормальных условиях р=101325 Па; Т=293 К.
13. в цилиндре с подвижным поршнем находится кислород при температуре 800С и разрежении (вакууме), равном 320 мм.рт.ст. При постоянной температуре кислород сжимается до избыточного давления 12 бар. Барометрическое давление равно 745 мм.рт.ст. Во сколько раз уменьшится объем кислорода?
Тест 5
1. PV=RT
Ответ: уравнение Клайперона-Менделеева, уравнение Бойля-Мариота.
2. Как рассчитать кажущийся молекулярный вес смеси, если известны массовые доли?
1) μсм=μ1+μ2+μ3+.....;
2) 
3) 
3. Единица измерения массовой теплоемкости:
1) Дж/кг К;
2) Дж/кмоль К;
3) Дж/м3 К;
4. Определяется ли изменение внутренней энергии начальным и конечным состоянием рабочего тела?
1) Да;
2) Нет.
5.По какой зависимости определяется внутренняя энергия?
1) dU=dq;
2) dU=СvdТ;
3) dU=СрdV.
6. Аналитическое выражение энтальпии:
1). I=U+PV;
2). di=dU+pdV.
7. Какой процесс изображен на диаграмме?

8. Указать уравнение изотермического процесса:
1). Р2/Р1=V1/V2;
2). V1/V2=Т2/Т1;
3). Р2/Р1=Т2/Т1.
9. Какой термодинамический процесс описывается уравнением РV=const?
1). Адиабатный;
2). Изохорный;
3). Изобарный;
4). Изотермический.
10. Как называется Т-S - диаграмма?
1) Тепловая;
2) Рабочая.
11. Смесь азота и водорода массовым отношением 4:1 при Р=const нагревается от 200-12000С. Найти среднюю теплоемкость и расход теплоты на нагревание 100кг смеси.
12. Определить массовый и объемный составы смеси водорода с азотом, если газовая постоянная ее равна R=922 Дж/кг град. Давление смеси 720 мм.рт.ст. определить также парциальное давление компонентов.
13. Составить формулу мольной средней теплоемкости при Р=const для смеси со следующим объемным составом: СО-15%; О-20%; N-65%.
Тест 6
1. Рсм=Р1+Р2+Р3+.....+Рn
Ответ: сумма давлений компонентов, закон Дальтона.
2. Можно ли вычислить изменение внутренней энергии по формуле:

1) Да;
2) Нет.
3. Какое уравнение является аналитическим выражением первого начала термодинамики?
1) dq=du+dl;
2) 
4. Какой процесс изображен на диаграмме?

5. Указать уравнение работы в изотермическом процессе:
1) I=RTlnV2/V1;
2) I=R(V2-V1).
6. По какой зависимости вычисляют теплоемкость многоатомных газов?
1). с=а+bt+сt2;
2). с=а+bt+сt2+dt3.
7. Вычислите теплоемкости смеси газов, если заданы массовые доли:
1) cсм=  сimi;
сimi;
2) cсм=с1m1+с2m2+…+сnmn
8. Указать уравнение, справедливое для обратного термодинамического цикла:
1) Iпол=q1-q2;
2) q1=q2+Iзат.
9. Указать аналитическое выражение второго начала термодинамики:
1) dS=dq/T;
2) q1/T1-q2/T2=0.
10. Какой процесс изображен на диаграмме?

11. Баллон емкостью 100 литров заполнен окисью углерода СО под абсолютным давлением 50 атм при температуре +200С. Определить количество теплоты, приобретенной газом и давление газа в баллоне.
12. Баллон, в котором находится азот, представляет собой цилиндр длиной 4 м и диаметром 1,2 м, абсолютное давление газа в баллоне 8 бар, начальная температура 520С. Вследствие разности температур азот охлаждается. Определить, на сколько градусов понизиться температура азота через 2 ч., если 1 м2 поверхности баллона теряет в окружающее пространство 12 кДж теплоты в течении 1 часа.
13. Воздух в количестве 800 м3 охлаждается от температуры 20000С до 2000С при постоянном давлении 1,5 бар. Определить среднюю теплоемкость и количество выделенной теплоты при охлаждении.
Дата добавления: 2014-11-13; просмотров: 1018; Мы поможем в написании вашей работы!; Нарушение авторских прав |