
КАТЕГОРИИ:
АстрономияБиологияГеографияДругие языкиДругоеИнформатикаИсторияКультураЛитератураЛогикаМатематикаМедицинаМеханикаОбразованиеОхрана трудаПедагогикаПолитикаПравоПсихологияРиторикаСоциологияСпортСтроительствоТехнологияФизикаФилософияФинансыХимияЧерчениеЭкологияЭкономикаЭлектроника
Следующим образом

Подставив это выражение в (7.14), после интегрирования получим

|
(7.16)

|
где J - постоянная интегрирования, которую можно определить, зная Кр при одной какой-либо температуре. Чтобы использовать уравнение (7.16), надо знать:
1) Зависимость теплоёмкостей всех реагирующих веществ от
температуры;
Хотя бы одно значение теплового эффекта реакции для
вычисления значения  ΔrH00;
ΔrH00;
3) Значение константы равновесия реакции при некоторой
температуре для определения постоянной интегрирования J.
Если теплоёмкости реагирующих веществ не известны в нужном интервале температур, то можно воспользоваться более точными формулами, чем (7.15). Приведём две таких формулы.
1 Предположим, что от 298 К и до температуры Т, при которой ищется  , величины
, величины 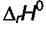 и
и  не меняются. Тогда
не меняются. Тогда
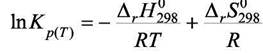
|
(7.17)
Значения констант равновесия, рассчитанные по (7.17), оказываются более точными, чем вычисленные по формуле (7.15). Укажем причины такого вывода. Выражения температурной зависимости энтальпии и энтропии реакции запишем в виде

|

|
Тогда
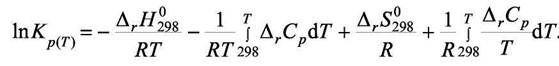
|
Дата добавления: 2014-12-23; просмотров: 274; Мы поможем в написании вашей работы!; Нарушение авторских прав |