
КАТЕГОРИИ:
АстрономияБиологияГеографияДругие языкиДругоеИнформатикаИсторияКультураЛитератураЛогикаМатематикаМедицинаМеханикаОбразованиеОхрана трудаПедагогикаПолитикаПравоПсихологияРиторикаСоциологияСпортСтроительствоТехнологияФизикаФилософияФинансыХимияЧерчениеЭкологияЭкономикаЭлектроника
Значения твердости в единицах HRC примерно в 10 раз меньше, чем в единицах НВ, т.е. твердость 30 HRC примерно соответствует 300НВ.
Метод Виккерса
Метод основан на вдавливании четырехгранной алмазной пирамидки с углом между противоположными гранями, равным 136°. Твердость (она обозначается HV ) определяется отношением нагрузки к площади поверхности отпечатка.
Значения твердости по Бринеллю и Виккерсу практически равны.
Метод Шора .
При измерении твердости по Шору груз вместе с укрепленным на нем индентором (обычно это стальной шарик) падает с высоты на образец перпендикулярно его поверхности. Твердость по Шору определяется по высоте отскока шарика(груз с индентором).

Определение ударной вязкости и вязкости разрушения
Для определения ударной вязкости используют образцы с надрезом, который служит концентратором напряжений. Образец устанавливают на маятниковом копре так, чтобы удар маятника происходил против надреза, раскрывая его. Маятник поднимают на высоту, при падении он разрушает образец, поднимаясь на высоту(так как часть запасенной при подъеме работы тратится на разрушение образца).

Ударная вязкость — это относительная работа разрушения, т.е. работа, отнесенная к площади образца до разрушения.
Вязкость разрушения. Более полную информацию о вязкости металлов дают испытания на вязкости разрушения.
 Кристаллизация сплавов.
Кристаллизация сплавов подчиняется тем же закономерностям, что и кристаллизация чистых металлов. Необходимым условием является стремление системы в состояние с минимумом свободной энергии.
Основным отличием является большая роль диффузионных процессов, между жидкостью и кристаллизующейся фазой. Эти процессы необходимы для перераспределения разнородных атомов, равномерно распределенных в жидкой фазе.
В сплавах в твердых состояниях, имеют место процессы перекристаллизации, обусловленные аллотропическими превращениями компонентов сплава, распадом твердых растворов, выделением из твердых растворов вторичных фаз, когда растворимость компонентов в твердом состоянии меняется с изменением температуры.
Эти превращения называют фазовыми превращениями в твердом состоянии.
При перекристаллизации в твердом состоянии образуются центры кристаллизации и происходит их рост.
Обычно центры кристаллизации возникают по границам зерен старой фазы, где решетка имеет наиболее дефектное строение, и где имеются примеси, которые могут стать центрами новых кристаллов. У старой и новой фазы, в течение некоторого времени, имеются общие плоскости. Такая связь решеток называется когерентной связью. В случае различия строения старой и новой фаз превращение протекает с образованием промежуточных фаз.
Нарушение когерентности и обособления кристаллов наступает, когда они приобретут определенные размеры.
Процессы кристаллизации сплавов изучаются по диаграммам состояния.
Диаграмма состояния.
Диаграмма состояния представляет собой графическое изображение состояния любого сплава изучаемой системы в зависимости от концентрации и температуры (рис. 4.5)
.
Кристаллизация сплавов.
Кристаллизация сплавов подчиняется тем же закономерностям, что и кристаллизация чистых металлов. Необходимым условием является стремление системы в состояние с минимумом свободной энергии.
Основным отличием является большая роль диффузионных процессов, между жидкостью и кристаллизующейся фазой. Эти процессы необходимы для перераспределения разнородных атомов, равномерно распределенных в жидкой фазе.
В сплавах в твердых состояниях, имеют место процессы перекристаллизации, обусловленные аллотропическими превращениями компонентов сплава, распадом твердых растворов, выделением из твердых растворов вторичных фаз, когда растворимость компонентов в твердом состоянии меняется с изменением температуры.
Эти превращения называют фазовыми превращениями в твердом состоянии.
При перекристаллизации в твердом состоянии образуются центры кристаллизации и происходит их рост.
Обычно центры кристаллизации возникают по границам зерен старой фазы, где решетка имеет наиболее дефектное строение, и где имеются примеси, которые могут стать центрами новых кристаллов. У старой и новой фазы, в течение некоторого времени, имеются общие плоскости. Такая связь решеток называется когерентной связью. В случае различия строения старой и новой фаз превращение протекает с образованием промежуточных фаз.
Нарушение когерентности и обособления кристаллов наступает, когда они приобретут определенные размеры.
Процессы кристаллизации сплавов изучаются по диаграммам состояния.
Диаграмма состояния.
Диаграмма состояния представляет собой графическое изображение состояния любого сплава изучаемой системы в зависимости от концентрации и температуры (рис. 4.5)
.  Рис. 4.5. Диаграмма состояния
Диаграммы состояния показывают устойчивые состояния, т.е. состояния, которые при данных условиях обладают минимумом свободной энергии, и поэтому ее также называют диаграммой равновесия, так как она показывает, какие при данных условиях существуют равновесные фазы.
Построение диаграмм состояния наиболее часто осуществляется при помощи термического анализа.
В результате получают серию кривых охлаждения, на которых при температурах фазовых превращений наблюдаются точки перегиба и температурные остановки.
Температуры, соответствующие фазовым превращениям, называют критическими точками. Некоторые критические точки имеют названия, например, точки отвечающие началу кристаллизации называют точками ликвидус, а концу кристаллизации – точками солидус.
По кривым охлаждения строят диаграмму состава в координатах: по оси абсцисс –концентрация компонентов, по оси ординат – температура.
Шкала концентраций показывает содержание компонента В. Основными линиями являются линии ликвидус (1) и солидус (2), а также линии соответствующие фазовым превращениям в твердом состоянии (3, 4).
По диаграмме состояния можно определить температуры фазовых превращений, изменение фазового состава, приблизительно, свойства сплава, виды обработки, которые можно применять для сплава.
Рис. 4.5. Диаграмма состояния
Диаграммы состояния показывают устойчивые состояния, т.е. состояния, которые при данных условиях обладают минимумом свободной энергии, и поэтому ее также называют диаграммой равновесия, так как она показывает, какие при данных условиях существуют равновесные фазы.
Построение диаграмм состояния наиболее часто осуществляется при помощи термического анализа.
В результате получают серию кривых охлаждения, на которых при температурах фазовых превращений наблюдаются точки перегиба и температурные остановки.
Температуры, соответствующие фазовым превращениям, называют критическими точками. Некоторые критические точки имеют названия, например, точки отвечающие началу кристаллизации называют точками ликвидус, а концу кристаллизации – точками солидус.
По кривым охлаждения строят диаграмму состава в координатах: по оси абсцисс –концентрация компонентов, по оси ординат – температура.
Шкала концентраций показывает содержание компонента В. Основными линиями являются линии ликвидус (1) и солидус (2), а также линии соответствующие фазовым превращениям в твердом состоянии (3, 4).
По диаграмме состояния можно определить температуры фазовых превращений, изменение фазового состава, приблизительно, свойства сплава, виды обработки, которые можно применять для сплава.
 Рис. 1. Диаграмма состояния, кривые охлаждения и схемы структур сплавов системы Pb—Sb при полном охлаждении до комнатной температуры
Сплав, содержащий 13 % Sb и 87 % РЬ, также имеет один горизонтальный участок, т. е. одну критическую точку (245 °С) -температуру затвердевания этого сплава. Этот сплав характеризуется тем, что в нем происходит одновременнаякристаллизацияиз жидкой фазы кристаллов РЬ и Sb (в общем случае компонентов А и В) с образованием механической смеси. Такая механическая смесь двух (или более) видов кристаллов, одновременно кристаллизующихся из жидкости, называется эвтектикой. Сам сплав с 13 % Sb и 87 % РЬ является эвтектическим, а его микроструктура представляет собой попеременно чередующиеся выделения сурьмы в свинцовой основе (рис. 1). Принято эвтектическую реакцию записывать так: Ж —> Pb + Sb, или в общем виде Ж —> А + В.
Кристаллизация любого сплава, имеющего 0 % < Sb < 13 %, начинается с выделения кристаллов РЬ. Эти сплавы затвердевают в интервале температур, и на кривых охлаждения имеются две критические точки, соответствующие началу и концу затвердевания (например, сплав с 5 % Sb, рис. 1). Все они называются до эвтектическими сплавами, претерпевают эвтектическое превращение при охлаждении ниже температуры 245 °С и имеют после окончательного охлаждения структуру РЬ + Э(РЬ + Sb), рис. 1. В этой структуре имеется две структурные составляющие: кристаллы РЬ и эвтектика Э(РЬ + Sb), которые получаются на базе двух фаз: кристаллов РЬ и кристаллов Sb.
Кристаллизация любого сплава с концентрацией 100 % > Sb >> 13 % начинается с выделения кристаллов Sb. Эти сплавы также
затвердевают в интервале температур - начала и конца затвердевания (например, сплав с 40 % Sb, рис. 5.1). При охлаждении ниже температуры 245 °С в них протекает эвтектическое превращение. Эти сплавы называются заэвтектическими и имеют после охлаждения окончательную структуру Sb + Э(РЬ + Sb), рис. 1. Структура заэвтектических сплавов также является двухфазной (кристаллы Sb и РЬ) и состоит из двух структурных составляющих: кристаллов Sb и эвтектики Э (Pb + Sb).
На диаграмме можно выделить три характерные зоны: область, где существует только жидкая фаза, - выше системы линий, ограниченной точками: температура 327 °С - эвтектическая точка 245 °С - температура 631 °С; область, где существует только твердая фаза (кристаллы РЬ и Sb), - ниже эвтектической линии (вся горизонтальная линия на уровне температуры 245 °С с концами в месте ее пересечений с ординатами со 100 % РЬ и 100 % Sb); область, где одновременно сосуществует жидкая и твердая фаза (область с жидко-твердой фазой) - между линиями, ограничивающими соответственно жидкое и твердое состояние сплавов.
Линия, ограничивающая на диаграмме область жидкой фазы сплавов, называется линией ликвидус. Линия, ограничивающая область полностью затвердевшего сплава от остальной области на диаграмме состояний, называется линией солидус.
Рис. 1. Диаграмма состояния, кривые охлаждения и схемы структур сплавов системы Pb—Sb при полном охлаждении до комнатной температуры
Сплав, содержащий 13 % Sb и 87 % РЬ, также имеет один горизонтальный участок, т. е. одну критическую точку (245 °С) -температуру затвердевания этого сплава. Этот сплав характеризуется тем, что в нем происходит одновременнаякристаллизацияиз жидкой фазы кристаллов РЬ и Sb (в общем случае компонентов А и В) с образованием механической смеси. Такая механическая смесь двух (или более) видов кристаллов, одновременно кристаллизующихся из жидкости, называется эвтектикой. Сам сплав с 13 % Sb и 87 % РЬ является эвтектическим, а его микроструктура представляет собой попеременно чередующиеся выделения сурьмы в свинцовой основе (рис. 1). Принято эвтектическую реакцию записывать так: Ж —> Pb + Sb, или в общем виде Ж —> А + В.
Кристаллизация любого сплава, имеющего 0 % < Sb < 13 %, начинается с выделения кристаллов РЬ. Эти сплавы затвердевают в интервале температур, и на кривых охлаждения имеются две критические точки, соответствующие началу и концу затвердевания (например, сплав с 5 % Sb, рис. 1). Все они называются до эвтектическими сплавами, претерпевают эвтектическое превращение при охлаждении ниже температуры 245 °С и имеют после окончательного охлаждения структуру РЬ + Э(РЬ + Sb), рис. 1. В этой структуре имеется две структурные составляющие: кристаллы РЬ и эвтектика Э(РЬ + Sb), которые получаются на базе двух фаз: кристаллов РЬ и кристаллов Sb.
Кристаллизация любого сплава с концентрацией 100 % > Sb >> 13 % начинается с выделения кристаллов Sb. Эти сплавы также
затвердевают в интервале температур - начала и конца затвердевания (например, сплав с 40 % Sb, рис. 5.1). При охлаждении ниже температуры 245 °С в них протекает эвтектическое превращение. Эти сплавы называются заэвтектическими и имеют после охлаждения окончательную структуру Sb + Э(РЬ + Sb), рис. 1. Структура заэвтектических сплавов также является двухфазной (кристаллы Sb и РЬ) и состоит из двух структурных составляющих: кристаллов Sb и эвтектики Э (Pb + Sb).
На диаграмме можно выделить три характерные зоны: область, где существует только жидкая фаза, - выше системы линий, ограниченной точками: температура 327 °С - эвтектическая точка 245 °С - температура 631 °С; область, где существует только твердая фаза (кристаллы РЬ и Sb), - ниже эвтектической линии (вся горизонтальная линия на уровне температуры 245 °С с концами в месте ее пересечений с ординатами со 100 % РЬ и 100 % Sb); область, где одновременно сосуществует жидкая и твердая фаза (область с жидко-твердой фазой) - между линиями, ограничивающими соответственно жидкое и твердое состояние сплавов.
Линия, ограничивающая на диаграмме область жидкой фазы сплавов, называется линией ликвидус. Линия, ограничивающая область полностью затвердевшего сплава от остальной области на диаграмме состояний, называется линией солидус.
 Рис. 2. Диаграмма состояния, кривые охлаждения и схемы типовых структур сплавов с неограниченной растворимостью в твердом состоянии
Чтобы определить количественное соотношение жидкой и твердой фаз, необходимо составить обратно пропорциональную зависимость между их количеством и отрезками горизонтальной линии, образованными между точкой, характеризующей состояние сплава, и точками, определяющими состав жидкой и твердой фаз.
Рассмотрим на примере двух типов диаграмм (рис. 3), как с помощью правила отрезков можно определить количество и состав фаз, например, для состояния, соответствующего точке k.
Для определения соотношения фаз и их состава через точку k проводим горизонтальную линию до пересечения с линиями, ограничивающими двухфазную область на диаграмме (точки las, рис. 3, а, б). Проекции точек пересечения на ось концентраций показывают состав жидкой фазы (точка V - проекция точки I, лежащей на линии ликвидус) и твердой фазы (точка s' - проекция точки s, соответствующей на рис. 3, а концентрации 100 % Sb и лежащей на линии солидус на рис. 3, б). В соответствии с правилом рычага отрезки горизонтальной линии между точкой k и точками, определяющими составы фаз, обратно пропорциональны количествам этих фаз, т. е. можно записать:
Рис. 2. Диаграмма состояния, кривые охлаждения и схемы типовых структур сплавов с неограниченной растворимостью в твердом состоянии
Чтобы определить количественное соотношение жидкой и твердой фаз, необходимо составить обратно пропорциональную зависимость между их количеством и отрезками горизонтальной линии, образованными между точкой, характеризующей состояние сплава, и точками, определяющими состав жидкой и твердой фаз.
Рассмотрим на примере двух типов диаграмм (рис. 3), как с помощью правила отрезков можно определить количество и состав фаз, например, для состояния, соответствующего точке k.
Для определения соотношения фаз и их состава через точку k проводим горизонтальную линию до пересечения с линиями, ограничивающими двухфазную область на диаграмме (точки las, рис. 3, а, б). Проекции точек пересечения на ось концентраций показывают состав жидкой фазы (точка V - проекция точки I, лежащей на линии ликвидус) и твердой фазы (точка s' - проекция точки s, соответствующей на рис. 3, а концентрации 100 % Sb и лежащей на линии солидус на рис. 3, б). В соответствии с правилом рычага отрезки горизонтальной линии между точкой k и точками, определяющими составы фаз, обратно пропорциональны количествам этих фаз, т. е. можно записать:
 - где Q„ Q, - количество твердой и жидкой фаз соответственно.
Для определения отношения какой-либо фазы (твердой или жидкой) ко всему количеству сплава Qs +, используются выражения:
- где Q„ Q, - количество твердой и жидкой фаз соответственно.
Для определения отношения какой-либо фазы (твердой или жидкой) ко всему количеству сплава Qs +, используются выражения:
 где si - вся длина горизонтальной линии.
Правило отрезков может использоваться не только для изучения процесса кристаллизации сплавов, но и для рассмотрения процессов, происходящих в твердом состоянии. Оно применимо ко всем двухфазным сплавам независимо от их агрегатного состояния.
где si - вся длина горизонтальной линии.
Правило отрезков может использоваться не только для изучения процесса кристаллизации сплавов, но и для рассмотрения процессов, происходящих в твердом состоянии. Оно применимо ко всем двухфазным сплавам независимо от их агрегатного состояния.
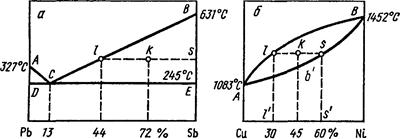 Рис. 3. Применение правила отрезков для сплавов, образующих механические смеси (а) и твердые растворы (б)
Если вернуться к рассмотрению диаграммы состояния с неограниченной растворимостью компонентов в твердом состоянии (рис. 2), то следует обратить внимание на то, что во всем интервале кристаллизации (например, от точки а' до Ь') из жидкого сплава с концентрацией компонентов, отвечающей точке k (45 % Си + 55 % Ni) (рис. 3), происходит постоянное выделение новых кристаллов. Причем состав первых кристаллов определяется проекцией точки s, лежащей на линии солидус. Заканчивается выделение новых кристаллов сплава k в точке Ь', когда затвердевает последняя капля жидкости, имеющая состав, определяемый проекцией точки I, лежащей на линии ликвидус.
Отсюда следует, что при охлаждении сплава в интервале кристаллизации состав жидкой фазы в соответствии с правилом отрезков меняется по линии ликвидус, а твердой фазы - по линии солидус.
Рис. 3. Применение правила отрезков для сплавов, образующих механические смеси (а) и твердые растворы (б)
Если вернуться к рассмотрению диаграммы состояния с неограниченной растворимостью компонентов в твердом состоянии (рис. 2), то следует обратить внимание на то, что во всем интервале кристаллизации (например, от точки а' до Ь') из жидкого сплава с концентрацией компонентов, отвечающей точке k (45 % Си + 55 % Ni) (рис. 3), происходит постоянное выделение новых кристаллов. Причем состав первых кристаллов определяется проекцией точки s, лежащей на линии солидус. Заканчивается выделение новых кристаллов сплава k в точке Ь', когда затвердевает последняя капля жидкости, имеющая состав, определяемый проекцией точки I, лежащей на линии ликвидус.
Отсюда следует, что при охлаждении сплава в интервале кристаллизации состав жидкой фазы в соответствии с правилом отрезков меняется по линии ликвидус, а твердой фазы - по линии солидус.
 Рис. 4. Диаграмма состояния, кривые охлаждения и схемы образования структур сплавов с ограниченной растворимостью в твердом состоянии и с эвтектическим превращением
EN и справа от линии DF. В этих областях все сплавы кристаллизуются в интервале между ликвидусом и солидусом, так же, как этот процесс проходит в любом сплаве на диаграммах состояния II рода (см. разд. 5.2). Соответственно в области, лежащей слева от линии EN при кристаллизации из жидкости начинают выделяться кристаллы твердого раствора а (например, для сплава I в точке 1). В интервале кристаллизации сплавы имеют двухфазную структуру Ж + а. После завершения кристаллизации и вплоть до окончательного охлаждения все эти сплавы имеют структуру однородного твердого раствора а. Аналогичная ситуация имеет место у всех сплавов, расположенных правее точки F, с той лишь разницей, что вместо a-твердого раствора у них выделяются кристаллы (3-твердого раствора.
У сплавов, расположенных в интервале между точкой F и проекцией точки D, первичная кристаллизация в интервале междуликвидусом и солидусом протекает аналогично ранее описанной. При этом эти сплавы после завершения кристаллизации вплоть до пересечения с линией DF имеют однородную структуру Р-твердого раствора (например, сплав IV в интервале между точками 2 и 3). При дальнейшем же охлаждении этих сплавов (например, сплаваIV ниже точки 3) вплоть до полного охлаждения в структуре этих сплавов происходят изменения, связанные с выделением из Р-твердого раствора второй фазы ап (например, у сплава IV), причиной появления которой является уменьшение предела растворимости P-твердого раствора при снижении температуры сплава. На это указывает наклонный характер кривой DF. При понижении температуры твердый раствор Р становится пересыщенным компонентом А, и для приведения системы в равновесие из этого твердого раствора Р выделяется избыток растворенного компонента А. Но так как в рассматриваемой системе чистые компоненты не могут существовать как самостоятельные фазы (они должны образовывать твердые растворы), то на базе избыточных кристаллов компонента А образуется сразу же a-твердый раствор, кристаллы которого и выделяются из P-твердого раствора и располагаются в виде мелкодисперсных включений внутри зерен основной фазы (см. рис. 4). Такие избыточные кристаллы, выделяющиеся не из жидкости, а из твердой фазы, обозначаются ап (вторичные а кристаллы), а сам процесс выделения новой фазы в твердом состоянии называется вторичной кристаллизацией.
Точки Е и N характеризуют предельную растворимость компонента В в компоненте А, т. е. предельную растворимость а-твер-дого раствора при эвтектической и комнатной температурах, а точки D и F - предельную растворимость компонента А в компоненте В, т. е. предельную растворимость P-твердого раствора также при эвтектической и комнатной температурах.
Как видно, предельная растворимость a-твердого раствора не изменяется с понижением температуры (линия EN - вертикальная), а предельная растворимость p-твердого раствора с понижением температуры уменьшается (линия DF — наклонная).
Точки Е и D являются границами линии ED, в пределах которой протекает эвтектическое превращение, а точка С — эвтектической точкой. Следовательно, во всех сплавах, расположенных в пределах границ эвтектической линии, будет проходить эвтектическое превращение, аналогичное тому, которое имеет место на диаграммах состояния I рода (см. разд. 5.2) с той лишь разницей, что в данном случае эвтектика состоит не из механической смеси компонентов А и В, а из механической смеси их твердых растворов а и р. В данном случае эти твердые растворы как бы являются компонентами сплавов для той части диаграммы, которая ограничена длиной эвтектической линии. Соответственно, эвтектика в этом случае будет иметь вид: Э(а + (3), а эвтектическая реакция может быть записана так: Ж —> а? + рв. Сплав с концентрацией компонентов А и В, соответствующей проекции точки С, т. е. сплав состава точки С, называется эвтектическим.
Все сплавы, расположенные между точками С и Е, называются до эвтектическими. Их кристаллизация будет начинаться с выделения кристаллов a-твердого раствора (например, сплава II в точке 1). В интервале кристаллизации (например, между точками
1 и 2) у этих сплавов будет двухфазная структура Ж + а. На линии ЕС (например, в точке 2) в доэвтектических сплавах будет проходить эвтектическая реакция у той части жидкости Ж, которая еще осталась в сплаве на этот момент (ее количество можно определить по правилу отрезков). Поэтому для доэвтектических сплавов правомерно будет записать эвтектическую реакцию в следующем виде: а + Ж —» а + Э(а + (3). Они после окончательного охлаждения будут иметь структуру а + Э (а + Р).
Все сплавы, расположенные между точками С и D, называются заэвтектическими. Их кристаллизация будет начинаться с выделения кристаллов (3-твердого раствора (например, у сплава III в точке Г). В интервале кристаллизации (например, у сплава III между точками 1 и 2) эти сплавы имеют двухфазную структуру Ж + (3. На линии CD у заэвтектических сплавов будет проходить эвтектическая реакция, подобная реакция доэвтектических сплавов, т. е. Р + Ж —> (3 + Э(а + (3). Но при дальнейшем охлаждении заэвтектических сплавов в их структуре будут проходить последующие превращения, которых не было в доэвтектических сплавах. Причиной этих превращений является наклонный характер линии DF. Как уже было показано ранее, при наклонном характере кривой растворимости компонента А в компоненте В (линия DF) с понижением температуры предельная растворимость А в В становится меньше того количества А, которое в данный момент присутствует в сплаве. Поэтому из твердого раствора Р будет выделяться ап. Следовательно, все заэвтектические сплавы ниже температуры эвтектического превращения (например, сплав III ниже точки 2) будут иметь следующую структуру: р + Э (а + Р) + ап Эта структура содержит три структурных составляющих: р, Э(а + Р) и а„, но при этом структура является двухфазной: a-фаза и Р-фаза.
Рис. 4. Диаграмма состояния, кривые охлаждения и схемы образования структур сплавов с ограниченной растворимостью в твердом состоянии и с эвтектическим превращением
EN и справа от линии DF. В этих областях все сплавы кристаллизуются в интервале между ликвидусом и солидусом, так же, как этот процесс проходит в любом сплаве на диаграммах состояния II рода (см. разд. 5.2). Соответственно в области, лежащей слева от линии EN при кристаллизации из жидкости начинают выделяться кристаллы твердого раствора а (например, для сплава I в точке 1). В интервале кристаллизации сплавы имеют двухфазную структуру Ж + а. После завершения кристаллизации и вплоть до окончательного охлаждения все эти сплавы имеют структуру однородного твердого раствора а. Аналогичная ситуация имеет место у всех сплавов, расположенных правее точки F, с той лишь разницей, что вместо a-твердого раствора у них выделяются кристаллы (3-твердого раствора.
У сплавов, расположенных в интервале между точкой F и проекцией точки D, первичная кристаллизация в интервале междуликвидусом и солидусом протекает аналогично ранее описанной. При этом эти сплавы после завершения кристаллизации вплоть до пересечения с линией DF имеют однородную структуру Р-твердого раствора (например, сплав IV в интервале между точками 2 и 3). При дальнейшем же охлаждении этих сплавов (например, сплаваIV ниже точки 3) вплоть до полного охлаждения в структуре этих сплавов происходят изменения, связанные с выделением из Р-твердого раствора второй фазы ап (например, у сплава IV), причиной появления которой является уменьшение предела растворимости P-твердого раствора при снижении температуры сплава. На это указывает наклонный характер кривой DF. При понижении температуры твердый раствор Р становится пересыщенным компонентом А, и для приведения системы в равновесие из этого твердого раствора Р выделяется избыток растворенного компонента А. Но так как в рассматриваемой системе чистые компоненты не могут существовать как самостоятельные фазы (они должны образовывать твердые растворы), то на базе избыточных кристаллов компонента А образуется сразу же a-твердый раствор, кристаллы которого и выделяются из P-твердого раствора и располагаются в виде мелкодисперсных включений внутри зерен основной фазы (см. рис. 4). Такие избыточные кристаллы, выделяющиеся не из жидкости, а из твердой фазы, обозначаются ап (вторичные а кристаллы), а сам процесс выделения новой фазы в твердом состоянии называется вторичной кристаллизацией.
Точки Е и N характеризуют предельную растворимость компонента В в компоненте А, т. е. предельную растворимость а-твер-дого раствора при эвтектической и комнатной температурах, а точки D и F - предельную растворимость компонента А в компоненте В, т. е. предельную растворимость P-твердого раствора также при эвтектической и комнатной температурах.
Как видно, предельная растворимость a-твердого раствора не изменяется с понижением температуры (линия EN - вертикальная), а предельная растворимость p-твердого раствора с понижением температуры уменьшается (линия DF — наклонная).
Точки Е и D являются границами линии ED, в пределах которой протекает эвтектическое превращение, а точка С — эвтектической точкой. Следовательно, во всех сплавах, расположенных в пределах границ эвтектической линии, будет проходить эвтектическое превращение, аналогичное тому, которое имеет место на диаграммах состояния I рода (см. разд. 5.2) с той лишь разницей, что в данном случае эвтектика состоит не из механической смеси компонентов А и В, а из механической смеси их твердых растворов а и р. В данном случае эти твердые растворы как бы являются компонентами сплавов для той части диаграммы, которая ограничена длиной эвтектической линии. Соответственно, эвтектика в этом случае будет иметь вид: Э(а + (3), а эвтектическая реакция может быть записана так: Ж —> а? + рв. Сплав с концентрацией компонентов А и В, соответствующей проекции точки С, т. е. сплав состава точки С, называется эвтектическим.
Все сплавы, расположенные между точками С и Е, называются до эвтектическими. Их кристаллизация будет начинаться с выделения кристаллов a-твердого раствора (например, сплава II в точке 1). В интервале кристаллизации (например, между точками
1 и 2) у этих сплавов будет двухфазная структура Ж + а. На линии ЕС (например, в точке 2) в доэвтектических сплавах будет проходить эвтектическая реакция у той части жидкости Ж, которая еще осталась в сплаве на этот момент (ее количество можно определить по правилу отрезков). Поэтому для доэвтектических сплавов правомерно будет записать эвтектическую реакцию в следующем виде: а + Ж —» а + Э(а + (3). Они после окончательного охлаждения будут иметь структуру а + Э (а + Р).
Все сплавы, расположенные между точками С и D, называются заэвтектическими. Их кристаллизация будет начинаться с выделения кристаллов (3-твердого раствора (например, у сплава III в точке Г). В интервале кристаллизации (например, у сплава III между точками 1 и 2) эти сплавы имеют двухфазную структуру Ж + (3. На линии CD у заэвтектических сплавов будет проходить эвтектическая реакция, подобная реакция доэвтектических сплавов, т. е. Р + Ж —> (3 + Э(а + (3). Но при дальнейшем охлаждении заэвтектических сплавов в их структуре будут проходить последующие превращения, которых не было в доэвтектических сплавах. Причиной этих превращений является наклонный характер линии DF. Как уже было показано ранее, при наклонном характере кривой растворимости компонента А в компоненте В (линия DF) с понижением температуры предельная растворимость А в В становится меньше того количества А, которое в данный момент присутствует в сплаве. Поэтому из твердого раствора Р будет выделяться ап. Следовательно, все заэвтектические сплавы ниже температуры эвтектического превращения (например, сплав III ниже точки 2) будут иметь следующую структуру: р + Э (а + Р) + ап Эта структура содержит три структурных составляющих: р, Э(а + Р) и а„, но при этом структура является двухфазной: a-фаза и Р-фаза.
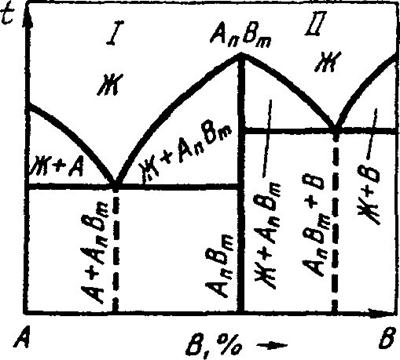 Рис. 6. Диаграмма состояния с устойчивым химическим соединением
Рассмотрим диаграмму состояния с устойчивым химическим соединением. Такая диаграмма изображена на рис. 6.
Примером диаграмм этого типа является диаграмма состояния сплавов системы Mg—Са.
Химическое соединение (например,
А„Вт) характеризуется определенным соотношением компонентов (например, п % компонента А и т % компонента В). На оси концентрации компонентов (ось абсцисс) химическое соединение обозначает точку, из которой выходит вертикальная линия, фактически разбивающая диаграмму на две простые диаграммы, в которых химическое соединение выступает уже в качестве самостоятельного компонента и, соответственно, образует эвтектики с компонентом А по реакции Ж —» А + А„Вт (7 простая диаграмма) и с компонентом В по реакции Ж —» В + А,Д,„ (II простая диаграмма).
Кристаллизация сплавов в пределах I и II простых диаграмм проходит аналогично кристаллизации сплавов, образующих эвтектику из чистых компонентов (диаграмма I рода). Поэтому после окончательного остывания у эвтектического сплава на I простой диаграмме структура будет состоять только из эвтектики Э(А + А(1В„,), у эвтектического сплава на II простой диаграмме -из эвтектики Э(В + А„Вт); у доэвтектических сплавов соответственно на I простой диаграмме и на II простой диаграмме структура будет иметь вид: А + Э(А + А„Вт) и А„В,„ + Э(В + А„Вт); у заэв-тектических сплавов на I простой диаграмме - А„ВШ + Э (А + А„Вт) и у заэвтектических сплавов на II простой диаграмме - В + Э (В + + АяВт).
Диаграмма состояния сплавов, испытывающих полиморфные превращения
Исходные данные: оба компонента неограниченно растворимы в жидком состоянии, в твердом состоянии могут образовывать механические смеси, в результате эвтектического или пе-ритектического превращения, а также могут образовывать непрерывные твердые растворы, и, кроме всего перечисленного, хотя бы один из компонентов обладает полиморфизмом.
Компоненты: химические элементы: А, В (К — 2).
Фазы: жидкость Ж, твердые растворы а, (З (Ф = 3).
8,%— N B,°/o —
Рис. 6. Диаграмма состояния с устойчивым химическим соединением
Рассмотрим диаграмму состояния с устойчивым химическим соединением. Такая диаграмма изображена на рис. 6.
Примером диаграмм этого типа является диаграмма состояния сплавов системы Mg—Са.
Химическое соединение (например,
А„Вт) характеризуется определенным соотношением компонентов (например, п % компонента А и т % компонента В). На оси концентрации компонентов (ось абсцисс) химическое соединение обозначает точку, из которой выходит вертикальная линия, фактически разбивающая диаграмму на две простые диаграммы, в которых химическое соединение выступает уже в качестве самостоятельного компонента и, соответственно, образует эвтектики с компонентом А по реакции Ж —» А + А„Вт (7 простая диаграмма) и с компонентом В по реакции Ж —» В + А,Д,„ (II простая диаграмма).
Кристаллизация сплавов в пределах I и II простых диаграмм проходит аналогично кристаллизации сплавов, образующих эвтектику из чистых компонентов (диаграмма I рода). Поэтому после окончательного остывания у эвтектического сплава на I простой диаграмме структура будет состоять только из эвтектики Э(А + А(1В„,), у эвтектического сплава на II простой диаграмме -из эвтектики Э(В + А„Вт); у доэвтектических сплавов соответственно на I простой диаграмме и на II простой диаграмме структура будет иметь вид: А + Э(А + А„Вт) и А„В,„ + Э(В + А„Вт); у заэв-тектических сплавов на I простой диаграмме - А„ВШ + Э (А + А„Вт) и у заэвтектических сплавов на II простой диаграмме - В + Э (В + + АяВт).
Диаграмма состояния сплавов, испытывающих полиморфные превращения
Исходные данные: оба компонента неограниченно растворимы в жидком состоянии, в твердом состоянии могут образовывать механические смеси, в результате эвтектического или пе-ритектического превращения, а также могут образовывать непрерывные твердые растворы, и, кроме всего перечисленного, хотя бы один из компонентов обладает полиморфизмом.
Компоненты: химические элементы: А, В (К — 2).
Фазы: жидкость Ж, твердые растворы а, (З (Ф = 3).
8,%— N B,°/o —
 Рис. 7. Диаграммы состояний с полиморфными превращениями
При полиморфных превращениях в сплавах происходит перекристаллизация существующих твердых фаз, которая подчиняется тем же закономерностям, что определяют процесс кристаллизации из жидкого состояния.
Если в сплавах один или оба компонента обладают полиморфизмом, то и сами сплавы из этих компонентов претерпевают полиморфные превращения в твердом состоянии. В этом случае диаграммы состояния становятся "многоярусными", причем верхний ярус диаграммы характеризует первичную кристаллизацию из жидкого состояния, а нижняя часть диаграммы - вторичную (перекристаллизацию), т. е. выделение кристаллов новой твердой фазы из твердой первичной фазы, например кристаллов a-твердого раствора из первичного (3-твердого раствора с другой кристаллической решеткой (рис. 7, а).
В общем случае вид диаграммы рассматриваемого случая зависит от того, какие фазы образуются в сплавах в процессе полиморфных превращений. Всевозможных вариантов может быть много. Но мы рассмотрим два наиболее характерных случая (рис. 7, а, б).
В первом случае (рис. 7, а) компонент А имеет аллотропические модификации Аа и Ар, которые образуют с компонентом В два твердых раствора а и р.
Кристаллизация сплавов в интервале кристаллизации с учетом перитектического превращения уже была ранее описана. В результате сплавы до температуры, соответствующей точке С (температуры полиморфного превращения), имеют либо однофазную структуру Р-твердого раствора, либо двухфазную структуру а + Р-твердого раствора. В этих сплавах при охлаждении ниже температуры полиморфного превращения проходит полиморфное превращение Р —» а с изменением кристаллической решетки.
Во втором случае (рис. 7, б) оба компонента испытывают полиморфные превращения, при этом низкотемпературные модификации их ограниченно растворимы друг в друге, а высокотемпературные модификации - неограниченно.
Не останавливаясь на деталях процесса кристаллизации сплавов из жидкого состояния (см. разд. 5.2), отметим, что в нижнем ярусе диаграммы фактически представлена диаграмма III рода, т. е. диаграмма с образованием ограниченных твердых растворов и протеканием эвтектического превращения. Однако отличительная черта данного эвтектического превращения состоит в том, что исходной фазой распада является не жидкость Ж, а твердый раствор у, который при переходе через линию KCN распадается на два новых раствора а и (3 по реакции у —> а + р.
Такое превращение, по сути аналогичное эвтектическому, но происходящее в твердом состоянии, называется эвтектоидным, а полученная механическая смесь - эвтектоидом. Сплав состава точки С называется эвтектоидным. Соответственно, сплавы, расположенные слева от точки С (сплав эвтектоидного состава) называются доэвтектоидными, а справа от нее - заэвтектоидными.
Рис. 7. Диаграммы состояний с полиморфными превращениями
При полиморфных превращениях в сплавах происходит перекристаллизация существующих твердых фаз, которая подчиняется тем же закономерностям, что определяют процесс кристаллизации из жидкого состояния.
Если в сплавах один или оба компонента обладают полиморфизмом, то и сами сплавы из этих компонентов претерпевают полиморфные превращения в твердом состоянии. В этом случае диаграммы состояния становятся "многоярусными", причем верхний ярус диаграммы характеризует первичную кристаллизацию из жидкого состояния, а нижняя часть диаграммы - вторичную (перекристаллизацию), т. е. выделение кристаллов новой твердой фазы из твердой первичной фазы, например кристаллов a-твердого раствора из первичного (3-твердого раствора с другой кристаллической решеткой (рис. 7, а).
В общем случае вид диаграммы рассматриваемого случая зависит от того, какие фазы образуются в сплавах в процессе полиморфных превращений. Всевозможных вариантов может быть много. Но мы рассмотрим два наиболее характерных случая (рис. 7, а, б).
В первом случае (рис. 7, а) компонент А имеет аллотропические модификации Аа и Ар, которые образуют с компонентом В два твердых раствора а и р.
Кристаллизация сплавов в интервале кристаллизации с учетом перитектического превращения уже была ранее описана. В результате сплавы до температуры, соответствующей точке С (температуры полиморфного превращения), имеют либо однофазную структуру Р-твердого раствора, либо двухфазную структуру а + Р-твердого раствора. В этих сплавах при охлаждении ниже температуры полиморфного превращения проходит полиморфное превращение Р —» а с изменением кристаллической решетки.
Во втором случае (рис. 7, б) оба компонента испытывают полиморфные превращения, при этом низкотемпературные модификации их ограниченно растворимы друг в друге, а высокотемпературные модификации - неограниченно.
Не останавливаясь на деталях процесса кристаллизации сплавов из жидкого состояния (см. разд. 5.2), отметим, что в нижнем ярусе диаграммы фактически представлена диаграмма III рода, т. е. диаграмма с образованием ограниченных твердых растворов и протеканием эвтектического превращения. Однако отличительная черта данного эвтектического превращения состоит в том, что исходной фазой распада является не жидкость Ж, а твердый раствор у, который при переходе через линию KCN распадается на два новых раствора а и (3 по реакции у —> а + р.
Такое превращение, по сути аналогичное эвтектическому, но происходящее в твердом состоянии, называется эвтектоидным, а полученная механическая смесь - эвтектоидом. Сплав состава точки С называется эвтектоидным. Соответственно, сплавы, расположенные слева от точки С (сплав эвтектоидного состава) называются доэвтектоидными, а справа от нее - заэвтектоидными.
| Стали обыкновенного качества. Углеродистые конструкционные сталиявляются самыми дешевыми сталями. Не обладают особыми свойствами, широко применяются для изготовления не ответственных деталей, конструкций, механизмов работающих в обычных условиях. Стали качественные. Углеродистые конструкционные сталиизготовленные также как и обыкновенного качество, но с более строгим контролем технологического процесса, для достижения более высоких показателей чистоты химического состава и механических свойств металла. Применяют для изготовления ответственных деталей и механизмов, но не требующих особых свойств. Стали высококачественные. Углеродистые и легированные, конструкционные и инструментальные стали полученные в дуговых электропечах, также с применением процесса электрошлакового переплава. Стали повышенной чистоты химического состава, с особыми свойствами. Применяются для изготовления ответственных деталей машин и механизмов, работающих в особых условиях и средах. Применяются для изготовления инструмента и оснастки. Стали особовысококачественные. Легированные инструментальные стали повергаются электрошлаковому переплаву позволяющему получить максимальную степень очистки от сульфидов и оксидов. Стали производятся в электропечах методами специальной металлургии. Полученные стали обладают специальными свойствами, в зависимости от сферы применения. Из них изготавливают особо ответственные узлы и детали машин, авиационной косметической отрасли, особо нагруженные механизмы, детали, работающие в экстремальных температурных, химических, физических условиях и средах. |
Дата добавления: 2014-12-30; просмотров: 388; Мы поможем в написании вашей работы!; Нарушение авторских прав |