
КАТЕГОРИИ:
АстрономияБиологияГеографияДругие языкиДругоеИнформатикаИсторияКультураЛитератураЛогикаМатематикаМедицинаМеханикаОбразованиеОхрана трудаПедагогикаПолитикаПравоПсихологияРиторикаСоциологияСпортСтроительствоТехнологияФизикаФилософияФинансыХимияЧерчениеЭкологияЭкономикаЭлектроника
Энтропия. Ее статистический смысл.
Энтропия является мерой вероятности осуществления какого-либо макроскопического состояния. Количественная мера неупорядоченности. Это новая функция состояния, определяемая соотношением: dS=dq/T, где dq - поглощаемое системой тепло в обратимом равновесном процессе.В любом процессе приращение энтропии больше или равно приведенной теплоте процесса dq/T: dS ³ dq/T
Энтропия растет до максимального значения, соответствующего положению равновесия. Т.о., S дает критерий самопроизвольного протекания процесса (dS>0) и критерий равновесия (dS = 0, d2S < 0).
В рамках статистической физики мерой неупорядоченности системы, состоящей из большого числа частиц, является число возможных микросостояний, соответствующих данному макросостоянию (термодинамическая вероятность системы W). Микросостояние задается набором координат и импульсов всех частиц системы, а макросостояние - набором функций состояния (Т,Р.V,U и др). Число микросостояний очень велико, и термодинамическая вероятность >>1. Энтропия в статистической физике определяется по Больцману:
S=klnW, где к - постоянная Больцмана.
48. Изменение энтропии при квазиравновесных процессах(изобарный, изотермический, изохорный, адиабатический процессы если что))
Каждый из изопроцессов идеального газа характеризуется своим изменением энтропии, а именно:
изохорический: 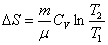 , т.к.
, т.к. 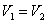 ; изобарический:
; изобарический:  т.к. Р1 = Р2;
т.к. Р1 = Р2;
изотермический:  т.к.
т.к.  ; адиабатический:
; адиабатический:  , т.к.
, т.к. 
Отметим, что в последнем случае адиабатический процесс называют изоэнтропийным процессом, т.к. 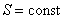 .
.
т.е. энтропия адиабатически изолированной системы может только возрастать (если есть необратимые процессы), или оставаться неизменной (если все процессы обратимые). – это закон возрастания энтропии.
Дата добавления: 2015-01-15; просмотров: 433; Мы поможем в написании вашей работы!; Нарушение авторских прав |