
КАТЕГОРИИ:
АстрономияБиологияГеографияДругие языкиДругоеИнформатикаИсторияКультураЛитератураЛогикаМатематикаМедицинаМеханикаОбразованиеОхрана трудаПедагогикаПолитикаПравоПсихологияРиторикаСоциологияСпортСтроительствоТехнологияФизикаФилософияФинансыХимияЧерчениеЭкологияЭкономикаЭлектроника
Основы расчета термохимических свойств топлива
Задачи расчета – составление условных (эквивалентных) формул топлива, расчет стехиометрического соотношения компонентов  и коэффициента избытка окислителя
и коэффициента избытка окислителя  , а также энтальпии топлива I, его компонентов и ПС.
, а также энтальпии топлива I, его компонентов и ПС.
Пример. Составить условную формулу окислителя. Состоящего из четырехокиси азота  (массовая доля
(массовая доля 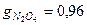 ) и воды
) и воды  (массовая доля
(массовая доля  .
.
Условную формулу запишем в виде:
 ,
,
т.е. на один моль  приходится x молей
приходится x молей  .
.
Зная массовые доли и молекулярные массы веществ (  ;
;  ), можно составить пропорцию для определения x: на
), можно составить пропорцию для определения x: на 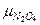 граммов
граммов  приходится
приходится  граммов воды
граммов воды  , с другой стороны, соотношение между массами этих веществ определяется их массовыми долями. Следовательно, из пропорции получим:
, с другой стороны, соотношение между массами этих веществ определяется их массовыми долями. Следовательно, из пропорции получим:

Таким образом условную формулу можно записать в виде  +0,211
+0,211  или в виде одночлена, суммируя количество грамм-атомов одинаковых элементов: количество грамм-атомов азота в условной формуле
или в виде одночлена, суммируя количество грамм-атомов одинаковых элементов: количество грамм-атомов азота в условной формуле  , кислорода
, кислорода  , водорода
, водорода  . В итоге условная формула
. В итоге условная формула  имеет вид
имеет вид  .
.
Иногда удобнее рассматривать сгорание не одного условного моля вещества, а одного килограмма. Тогда составляют, так называемую удельную формулу. Для перехода к такой формуле надо число грамм-атомов в условной формуле умножить на  , где
, где  – условная молекулярная масса окислителя. Для рассмотренного примера
– условная молекулярная масса окислителя. Для рассмотренного примера
 .
.
В итоге удельная формула окислителя  . В данном случае условная молекулярная масса равна 1000 г/моль.
. В данном случае условная молекулярная масса равна 1000 г/моль.
Дата добавления: 2015-01-19; просмотров: 218; Мы поможем в написании вашей работы!; Нарушение авторских прав |