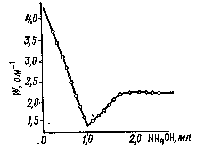КАТЕГОРИИ:
АстрономияБиологияГеографияДругие языкиДругоеИнформатикаИсторияКультураЛитератураЛогикаМатематикаМедицинаМеханикаОбразованиеОхрана трудаПедагогикаПолитикаПравоПсихологияРиторикаСоциологияСпортСтроительствоТехнологияФизикаФилософияФинансыХимияЧерчениеЭкологияЭкономикаЭлектроника
Г) Титрование смеси кислот и оснований
При титровании смеси сильной и слабой кислот в растворе, например, соляной и уксусной, кривая имеет два излома, соответствующих двум точкам эквивалентности (рис.8, 9). Первая показывает объем гидроксида натрия, пошедший на титрование сильной кислоты, а вторая дает общий объем гидроксида натрия, израсходованный на титрование обеих кислот. С увеличением константы диссоциации слабой кислоты первый излом будет становиться менее резким, а второй - более четким, и, наоборот, чем слабее кислота, тем резче будет первый излом, и более закругленным второй.

Рис.8. Кривая кондуктометрического титрования смеси сильной и слабой кислот
|
Рис.9. Кривая кондуктометрического титрования смеси 0,1М НСl и 0,1М СН3СООН
раствором 1М NH4OH
Кисло́тно-осно́вное равнове́сие — относительное постоянство соотношения кислота-основание внутренней среды живого организма. Также называют кисло́тно-щелочно́е равнове́сие, кислотно-щелочной баланс, равновесие кислот и оснований. Является составной частью гомеостаза. Количественно характеризуется либо концентрацией водородных ионов (протонов) в молях на 1 л, либо водородным показателем pH.
Дата добавления: 2015-01-29; просмотров: 438; Мы поможем в написании вашей работы!; Нарушение авторских прав |