
КАТЕГОРИИ:
АстрономияБиологияГеографияДругие языкиДругоеИнформатикаИсторияКультураЛитератураЛогикаМатематикаМедицинаМеханикаОбразованиеОхрана трудаПедагогикаПолитикаПравоПсихологияРиторикаСоциологияСпортСтроительствоТехнологияФизикаФилософияФинансыХимияЧерчениеЭкологияЭкономикаЭлектроника
Технологические схемы получения карбамида.
Все известные схемы производства карбамида из NH3 и СО2 разделены на пять групп:
1)Процессы без рецикла (с переработкой NH3, а иногда и СО2, в соли аммония).
2)Пр-сы с частичным рециклом аммиака.
3)Пр-сы с рециркуляцией горячих газов.
4)Пр-сы с рециркуляцией углеаммонийных солей в растворе или в виде суспензии (жидкостный рецикл).
5)Пр-сы, основанные на селективном извлечении из газовой фазы одного из компонентов и раздельном возврате NH3 и СО2 в цикл (газовый рецикл).
1)Впервые осуществлен в 1922 г на установке производит-ю 1,2 т/ч. Газообр-й СО2 компрессором сжимается до 150 ат, подогревается до 200° С и на медно-никелевом катализаторе освобождается от кислорода. Далее конденсируется и смешивается со сжатым до 150 ат жидким NH3, подаваемым в избытке. Тепло обр-я карбамата аммония отводится в реакторе. В нем поддерживается давление 130 ат и температура 160° С; Охлажденный плав направляется в пять последовательно соединенных автоклавов, обогреваемых паром. Здесь в течение 2 ч при 160-1700С и давлении 100 ат около 50% карбамата аммония превращается в карбамид. Выпарка осуществляется в 2 ступени. концентрация раствора увеличивается в 1 от 72 до 80% и во 2— до 93%. Раствор после выпарки направляется в сборник. Полученный порошок падает на транспортер и передается в сушильный барабан. Газы из сепаратора и соковый конденсат, обр-ся при выпарке, направл-ся в башню, орошаемую серной к-й, для получения р-ра сульфата аммония.
Основной недостаток— низкая степень использования сырья (30—35% NH3,45—50% СО2).
2) основан на возврате NH3. Основным отличием схемы с частичным рециклом аммиака от процесса без рецикла является двухступенчатое дросселирование и дистилляция плава, полученного в колонне синтеза. При этом в 1 ступени дистилляции поддерживается такое давление, которое позволяет конденсировать выделившийся NH3 охлаждением водой. Давление во 2 ступени приближается к атм-му.
Газообр-й СО2 сжим-ся до 200 ат и нагнетается во внутренний стакан колонны синтеза. Сюда же подается NH3. Свежий NH3 нагнетается в зазор между стаканом и корпусом колонны. В колонне поддержив-ся 200 ат и t 185—200 С. Плав, вых-й из колонны синтеза подвергается дистилляции. В колонне дистилляции происходит выделение из плава избыточного аммиака и разлож-е карбамата аммония. Пары NH3 с t 50—60°С направл-ся для сжижения в два конденсатора. Жидкий NH3 возвращается в колонну синтеза. Раствор карбамида из колонны дистилляции, частично освобожденный от NH3, дросселируется до 1,5—1,7 ат и подается на тарелку колонны дистилляции, сюда же подается раствор углеаммонийных солей. Р-р с тарелки подается в кипятильник и возвращ-ся в нижнюю часть колонны, где происходит разложение карбамата аммония и отгонка СО2 и NH3 в газовую фазу, которая направл-ся в скруббер-нейтрализатор для получ-я р-ра нитрата аммонии. Р-р, содержащий 70—80% карбамида подается в кипятильник выпарного ап-та, где упарив-ся до 99,5—99,8%. Преим-во пр-в с частичным рециклом по сравнению с пр-м без рецикла состоит в том, что они позволяют повысить степень превращя NH3 в карбамид.
3) аммиак и СО2 отгоняются из плава при атм-м давл-и и t 60°С направл-ся в абсорбер, где поглощ-ся аммиачной водой. Полученный р-р углеаммонийных солей, содерж-й 20% NН3 и 15—16% СО2, сжим-ся до 150 ат и подается через теплообм-к и подогреватель в колонну ректификации. Здесь в газовую фазу отгоняются NH3 и СО2. Газовая фаза после дефлегматора направл-ся через холодильник в автоклав для синтеза карбамида, а аммиачная вода, вытекающая из нижней части ректификационной колонны через теплообм-к подается на орошение абсорбера. Свежие NH3 и СО2 смешив-ся с циркулирующим газом перед реактором карбамата. Способ проверялся на опытной установке, но вследствие высоких энергетических затрат промышленного распространения не получил.
4) Процессы производства карбамида с полным рециклом углеаммонийных солей нашли широкое применение в пром-ти. Конкуренция между фирмами разных стран ( «Хемико» - США;«Стамикарбон» — Голландия, «Toe-Коацу» — Япония, и т. д.). Рассмотрим схему "Стамикарбон":
Стиппинг процесс основан на принципе разложения карбомата непрореагировавшего в карбамид, за счет интенсивной продувки р-ра диоксидом углерода. В аппарате отдувки (стриппере) используется тоже давление, что и в колонне синтеза.
Диоксид углерода сжатый до 14,5 – 15,2 МПа компрессором подают в стриппер, где происходит разложение оставшегося после колонны синтеза карбамата аммония на аммиак и СО2 по р-ии:
NH2CO2NH4 → 2 NH3 + CO2, ΔH = -125.6 кДж. Из стриппера газовая фаза (NH3 + CO2) поступает в конденсатор высокого давления, в котором происходит образование NH2CO2NH4.
Для осуществления р-ии в условиях избытка аммиака в конденсатор подают жидкий аммиак, через инжектор высокого давления.
Образовавшийся р-р карбомата аммония из конденсатора, подают в колонну синтеза, где 50 – 68 % карбомата аммония превращается в карбамид по р-ии: NH2СООNH4(ж) ↔ CO(NH2)2(ж) + H2O (ж); ΔН = 15,5кДж. Р-р из реактора состоящий из карбамида, карбомата аммония, аммиака и воды, поступает в стриппер, где при 170 – 190 0С и 14,3 – 15,2 МПа и благодаря интенсивному перемешиванию барботирующим СО2 происходит разложение карбомата, после стриппера р-р карбамида поступает в ректификационную колонну, в нижней части она имеет теплообменник обогреваемый паром, здесь при 130 – 140 0С и 0,25 МПа происходит разложение оставшегося карбомата и отгон из р-ра аммиака и СО2 . Тепло необходимое для разложения карбомата аммония обеспечивается подачей пара в теплообменник, р-р выходящий из разлогателя подают, через сепаратор на упарку, газовая фаза поступает в конденсатор, полученный р-р из сборника подают в скруббер высокого давления. Из него р-р поступает в реактор.Газовая фаза из скруббера проходит трехступенчатую кислую промывку где окончательно очищается от аммиака, очищенные газы из скруббера выбрасываются в атм. Р-р карбамида (м.д.73 – 75 %) подается в отделение 2-х ступенчатой упарки, после выпарки упаренный р-р (плав) подают на грануляцию, готовый гранулированный карбамид (гранулы 1 – 4 мм) поступает на склад и затем на отгрузку потребителям.
5) основан на избирательном поглощении аммиака водным раствором нитрата аммония и карбамида. Аммиак и СО2 под Р=170—210 ат подаются в реактор (160—190°С); образующийся пар используется в дальнейшем для разложения карбамата аммония. Плав из реактора дросселируется до 4,5—21 ат и поступает в трубчатый теплооб-к, обогреваемый паром. происходит частичное разлож-е карбамата аммония, после чего газовая фаза отделяется от жидкой в сепараторе. Жидкая фаза снова дросселируется для разложения оставшегося карбамата аммония. Очищенный от карбамата аммония раствор карбамида конц-и 80—90% поступает либо на приготовление жидких удобрений, либо перерабатывается в гранулированный продукт. В последнем случае раствор упаривается до концентрации 99% в выпарном аппарате; плав подвергается грануляции.
Вопрос №37: Производство аммиачной селитры. Сырье и требования к качеству продукционной аммиачной селитры. Физико-химические свойства нитрата аммония. Слеживаемость продукта и способы ее устранения. Расходные коэффициенты на 1 т аммиачной селитры.
NH4NО3 – распространенное азотное удобрение, содержащее 34,4 % масс. азота в аммонийной и нитратной формах. Аммиачная селитра вырабатывается в соответствии с требованиями ГОСТ 2-85. В качестве сырья используется аммиак и азотная кислота.
Требования к качеству АС.
Согласно ГОСТ 2-85 АС выпускают двух марок: А – для промышленности, Б – для с/х. Высшая категория качества АС марки Б должна соответствовать следующим нормам:
М.д. азота, % не менее …….34,4
М.д. одной из след. Добавок, %
- сульфата аммония …………….0,3-0,7
- нитрата магния в пересчете на МgO .0,2-0,5
- фосфатов в пересчете на Р2О5.0,5-1,2
3. М.д. воды методом сушки, % не более ….0,3
4. рН 10 % водного р-ра, не менее…..5
5. Гранулометрический состав, м.д. гранул:
от 1 до 4 мм, % н.м…….95, от 2 до 3 мм, % н.м……50
менее 1 мм, % н.б……… 3, более 6 мм, % не более……0
6. Статическая прочность гранул, г/гранулу, не менее .700
7. Рассыпчатость, % не иене ………100
Основные физико-химические свойства АС:
Внешний вид – гранулированный продукт без посторонних механических примесей. Молярная масса – 80,04 г/моль, кг/кмоль
Плотность т/м3: Истинная – 1,69-1,73, Насыпная - ~ 1,16
Температура плавления, оС – 169,6. Теплота плавления, кДж/кг -73,21
В основе технологии АС лежит р-ция нейтрализации. HNO3+NH3 →NH4NO3, ΔH = -146,49 кДж (1)
Твердый NH4NO3 в зависимости от температуры сущ-ет в 5 кристаллических модификациях т/д устойчивых при атмосферном давлении. Каждая модификация сущ-ет в определ. обл-ти температур и переход одной модификации в другую сопровождается изменениями кристаллической структуры, выделение (поглоще-нием) тепла, скачкообразным изменением удельного объема и теплоемкости. Полиморфные переходы обратимы. В таблице приведены температуры полиморфных превращений NH4NO3 и происходящие при этом изменения удельного объема.
| Превращ-е | Т-ра превращ-я | Изменения V при охл-ии, дм3/кг | Форма кристаллов |
| Плав ↔ I | 169,6 | Уменьш на 0,054 | I - кубическая |
| I↔II | 125,8 | Уменьш на 0,014 | II - тетрагональная |
| II ↔ III | 84,2 | Уменьш на 0,008 | III – ромбическая моноклинная |
| III↔ IV | 32,2 | Увелич на 0,022 | IV – ромбическая бипирамидальная |
| IV ↔ V | -16,9 | Уменьш на 0,017 | V - тетрагональная |
| II ↔ IV | 50,5 | Увелич на 0,014 | IV – ромбическая бипирамидальная |
Температурные границы и скорость взаимопревращений модификаций для NH4NO3 несколько отл-ся от табличных данных для NH4NO3, в зависимости от влажности селитры и наличия в ней примесей. Нитрат аммония очень хорошо растворим в воде. Растворение нитрата аммония в воде протекает с поглощением большого кол-ва тепла. Нитрат аммония весьма гигроскопичен. Гигроскопические точки нитрата аммония при разных температурах следующие.
| Температура, оС | |||||
| W,% | 75,3 | 66,9 | 59,4 | 52,5 | 48,4 |
АС сильно слеживается. По р-ции (1) получается р-р NH4NO3, выпаркой к-рого при температуре выше температуры его кристаллизации воду можно удалить практически полностью и р-р превратить в расплавленную соль (расплав - плав). Гигроскопичность нитрата аммония и скорость поглощения им влаги из воздуха как правило увеличиваются при добавке растворимых неорганических солей. Из-за большой растворимости в воде, гигроскопичности и полиморфных превращений нитрат аммония сильно слеживается и теряет рассыпчатость, что затрудняет его применение.
Исп-ют следующие средства борьбы со слеживаемостью:
· Выпуск продукта в гранулированном виде, вместо порошкообразного, с минимальным содержанием влаги (не более 0,25%) и максимальным охлаждением гранул. Охлаждение необходимо для образования формы IV стабильной при температуре ниже 32,2 оС .
· Применение кондиционирующих добавок, вводимых в р-р нитрата аммония до его кристаллизации. Такими добавками явл-ся нитрат магния, смесь нитратов кальция и магния, сульфат аммония, смесь фосфорной и серной кислот. Механизм действия добавок различен. Так, добавка Мg(NO3)2 способствует связыванию свободной воды плава вследствие образования кристаллогидрата Мg(NO3)2• 6 Н2О, она замедляет переход II ↔ III и обеспечивает переход II ↔ IV, что увеличивает прочность гранул.
· Обработка гранул ПАВ, способными образовывать гидрофобные пленки. Для этой цели применяют 40% р-р диспергатора НФ. Упаковка соли в плотную, хорошо герметизированную тару ( Н: в полиэтиленовые мешки и контейнеры).
· Применение средств, повышающих качество продукта и снижающих его слеживаемость, позволяет осуществить его бестарное хранение и транспортировку насыпью в вагонах-хопперах и вагонах – минераловозах.
При нагревании выше 110 оС нитрат аммония начинает разлагаться на аммиак и азотную кислоту: NH4NO3 (т) → HNO3 (г) +NH3 (г), ΔH = 185,58 кДж (2)
Скорость этой реакции невелика. При 200-270 оС идет интенсивное разложение по реакции: NH4NO3 (т) → N2О (г) + 2Н2О (г), ΔH = -36,8 кДж (3)
При быстром нагревании до 400-500 оС происходит разложение со взрывом по реакции NH4NO3 (т) → N2(г) + 2Н2О (г) + О2, ΔH = -118 кДж (4)
Практически взрывоопасна темп-ра 300оС. АС относится к взрывчатым вещ-м средней силы.
Расходные коэффициенты на 1т. NH4NO3, полученные в агрегате АС-72М.
1. Аммиак, кг/т 213-215 практ
17 кг/кмоль NH3 – 80 кг/кмоль NH4NO3
Х кг/кмоль NH3 – 1000 кг/кмоль NH4NO3
Х = 212,5 кг/т – теоретический.
2. Азотная кислота (100% HNO3), кг/т
Кпр=790
63 кг/кмоль НNО3 – 80 кг/кмоль NH4NO3
Х кг/кмоль НNО3 – 1000 кг/кмоль NH4NO3
Х = 787,5 кг/т – теоретический.
3. Каустический магнезит (ПМК-83), кг/т 6,0
Мощн. ИТН 56т/ч по АС.
Часовая потребность: 56*6=336кг/ч
330раб. сут: 56*24*330=443520т/год
Годовая потребность магнезита: 450000*6/1000=2700т/год
Месячная потребность 2700/12=225
4. Вода оборотная, м3 1,1
- для охл-я р-ра
Вопрос №38: Реакция нейтрализации. Технологические условия производства аммиачной селитры. Роль магнезиальной добавки к нитрату аммония. Получение нитрата магния, сырье. Оборудование стадии нейтрализации в производстве аммиачной селитры.
Технологические условия производства NH4NO3
Получение NH4NO3 основано на р-ции: HNO3+NH3 →NH4NO3, ΔH = -146,49 кДж (1).
 При нейтрализации HNO3, содержащей 47-60% HNO3 обр-ся р-р NH4NO3. Этот р-р для получения твердого продукта упаривается. При этом на 1 стадии исп-ся теплота самой р-ции нейтрализации. Кол-во тепла, выделяющееся при нейтрализации, зависит от конц-ции исходной HNO3+NH3 ( рис.1)
При нейтрализации HNO3, содержащей 47-60% HNO3 обр-ся р-р NH4NO3. Этот р-р для получения твердого продукта упаривается. При этом на 1 стадии исп-ся теплота самой р-ции нейтрализации. Кол-во тепла, выделяющееся при нейтрализации, зависит от конц-ции исходной HNO3+NH3 ( рис.1)
Чем больше конц-ция HNO3, тем более концентриров. р-р NH4NO3 м. получить на стадии нейтрализации за счет исп-ия тепла р-ции.

1-без исп-ия тепла р-ции, 2-при исп-ии тепла р-ции
Нейтрализация HNO3 аммиаком осуществляется в аппарате ИТН- использователь тепла нейтрализации.
Роль магнезиальной добавки в производстве аммиачной селитры
Так как АС сильно слеживается, приходится принимать некоторые меры по борьбе с этим явлением. Чаще всего для этого используют магнезиальную добавку. Добавка нитрата магния обеспечивает связывание свободной воды плава, образуя кристаллогидрат Mg(NO3)2*6H2O. Эта добавка замедляет переход II-III и обеспечивает переход II-IV, что увеличивает прочность гранул. Это связано с тем, что при переходе II-IV удельный объем изменяется незначительно, т.к. параметры решетки модификации II (тетрагональная) и параметры решетки IV (ромбическая бипирамидальная) – близки друг к другу.
Получение нитрата магния. Сырье.
Магнезиальную добавку получают из каустического магнезита по реакции:
MgO+2HNO3=MgO+H2O
Оборудование стадии нейтрализации в производстве аммиачной селитры.
ИТН состоит из 2-х цилиндрических частей (нижней – реакционной, диаметром 1,6 м и верхней – сепарационной, диаметром 3,8 м). Общая высота аппарата – 10м.
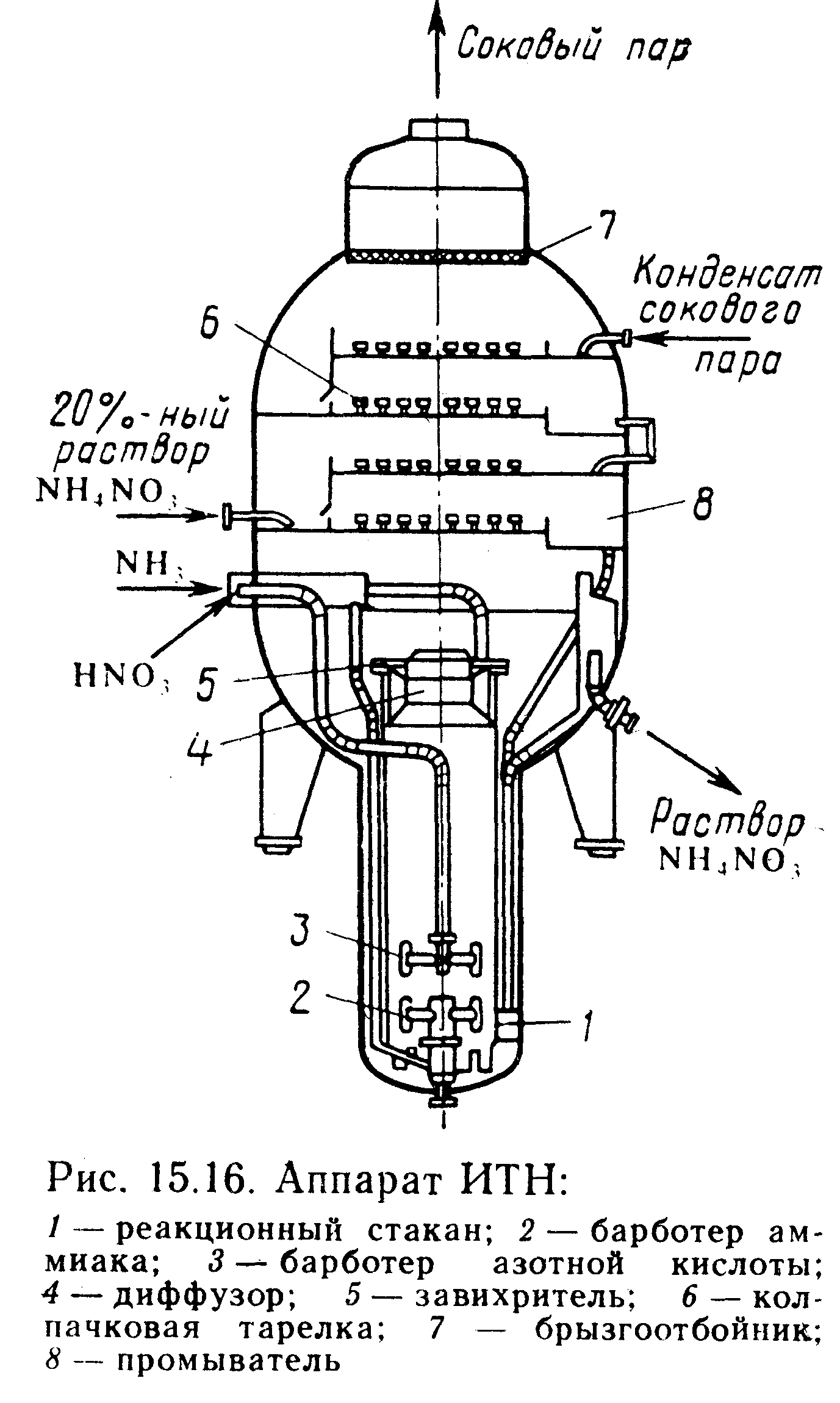
1 – реакционный стакан, 2 – барботер аммиака, 3 – барботер азотной кислоты,
4 – диффузор, 5 – завихритель, 6 – колпачковая тарелка, 7 – брызгоотбойник,
8 – промыватель.
Внутри корпуса реакционной части 1 нах-ся реакционный стакан 2 с отверстиями внизу. Внутрь стакана поступают аммиак и р-р азотной кислоты через титановые барботеры 3 и 4. Скорость аммиака в отверстиях барботера 30-50м/с. Скорость HNO3 2-3 м/с. За счет теплоты р-ции нейтрализации из образующегося р-ра NH4NO3 испаряется часть воды. Вследствие этого возникает подъемная сила, и парожидкостная эмульсия выбрасывается из верха реакционного стакана через завихритель 5, способствующий разделению парожидкостной смеси. Кратковременное пребывание реагентов в реакционном стакане 05-1с обеспечивает незначительные потери азота за счет термического разложения HNO3 и нитратов аммония. Температура пр-са нейтрализации составляет 150-160 оС. Р-р, выходящий из завихрителя 5 по кольцевому зазору между стаканом и корпусом аппарата, движется вниз, продолжая упариваться за счет тепла, получаемого через стенку стакана.Часть циркулирующего р-ра отводится для дальнейшей переработки. Кратность циркуляции в ИТН, равная отношению расходов циркулирующего и выходящего из аппарата р-ра NH4NO3 имеет величину порядка 100. Соковый пар, отделяемый в завихрителе от р-ра, содержит брызги р-ра NH4NO3, NH3 или пары HNO3. Очистка СП производится в верхней сепарационной части 6. При этом СП поднимаясь со скоростью 0,6 м/с промывается на 4-х барботажных колпачковых тарелках 7. На 2-х нижних тарелках пар отмывается от аммиака 15-20 % р-ром NH4NO3, подкисленным HNO3. При этом р-р подается на 2-ую тарелку, затем перетекает на 1-ую тарелку, а с неё по переливной трубе 9 перетекает в реакционную зону, смешиваясь с циркулирующим 90 % р-ром . На 2-х верхних тарелках из СП улавливаются пары HNO3 и брызги р-ра NH4NO3 с помощью конденсата СП. При этом КСП подается на 4 тарелку, затем перетекает на 3 и выводится из аппарата. Из аппарата ИТН выходит 89-91 % NH4NO3 .
Вопрсо№39: Методика расчета материального баланса аппарата ИТН
Расчет выполним для агрегата АС-72М производительностью 56т/ч в расчете на 100% NH4NO3.
Нейтрализация HNO3 аммиаком осуществляется в двух параллельно работающих аппаратах ИТН, производительностью 28т/ч.
Исходные данные:
Концентрация HNO3, %масс. 58
Концентрация газообразного NH3, %масс. 100
Потери HNO3 на 1000 кг NH4NO3, кг 7,5
Потери NH3 на 1000 кг NH4NO3, кг 2,5
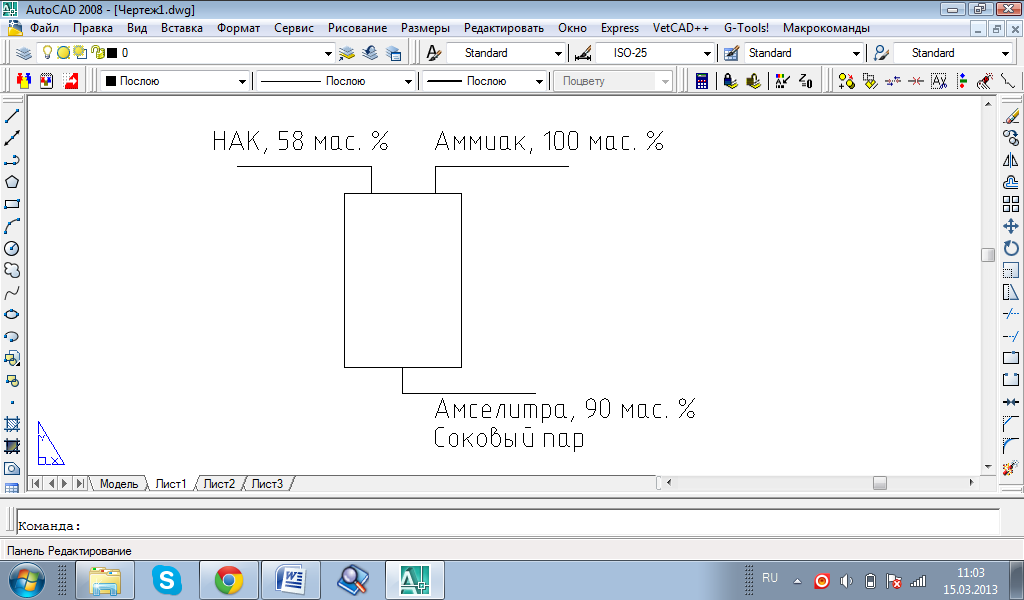
Расчет:
Нейтрализация протекает по реакции (1): 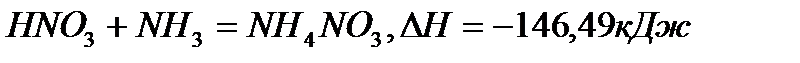 .
.
1. Рассчитываем теоретический расход азотной кислоты по уравнению реакции по формуле:
 , кг
, кг
2. Определяем практический расход с учетом потерьПрактический расход с учетом потерь:
 , кг
, кг
3. Рассчитываем теоретический расход NH3:
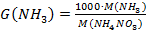 , кг
, кг
4. Определяем практический расход с учетом потерь
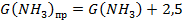 , кг
, кг
5. Часовой расход HNO3 в аппараты ИТН равен:
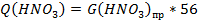 , кг/ч
, кг/ч
6. Часовые потери HNO3 составляют:
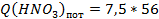 , кг/ч
, кг/ч
7. Часовой расход NH3:
 , кг/ч
, кг/ч
8. Часовые потери NН3 составляют:
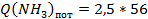 , кг/ч
, кг/ч
9. Расход 58%-ной кислоты на нейтрализацию равен:
 , кг/ч
, кг/ч
10. Масса воды, содержащаяся в растворе HNO3:
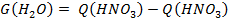 , кг/ч
, кг/ч
11. Общая масса раствора HNO3 и NH3, поступающих в аппараты ИТН:
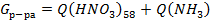 , кг/ч
, кг/ч
12. Концентрация раствора NH4NO3 в аппаратах ИТН без учета испарения воды за счет тепла реакции нейтрализации бала бы равна
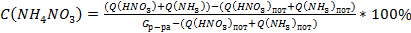 ,
,
13. С учетом испарения воды концентрация раствора NH4NO3, выходящего из ИТН, принимается равной 90%. Правильность выбранной концентрации проверяется тепловым расчетом
Масса 90%-ного раствора NH4NO3, выходящего из ИТН, равна:
 56000/0,90 = 62222 кг/ч.
56000/0,90 = 62222 кг/ч.
14. Масса воды, содержащаяся в этом растворе:
 62222 – 56000 = 6222 кг/ч.
62222 – 56000 = 6222 кг/ч.
15. Масса воды, испарившаяся за счет тепла нейтрализации и перешедшая в соковый пар:
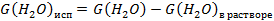 , кг/ч
, кг/ч
Итак, мы рассчитали материальный баланс аппарата ИТН по основным потокам: NH3 и раствору HNO3. Однако, с 1 тарелки сепарационной зоны по переливной трубе (9) в реакционную часть поступает 20%-ный раствор NH4NO3. Этот раствор смешивается с основной массой циркулирующего 90%-ного раствора NH4NO3. Объем такого 20%-ного раствора 6,4 м3/ч, а плотность его 1,085 т/м3.
Уточним материальный баланс с учетом прихода этого 20%-ного раствора NH4NO3 из сепарационной зоны.
16. Масса 20%-ного раствора NH4NO3:
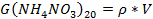 , кг/ч
, кг/ч
17. Масса NH4NO3 в 20%-ном растворе:
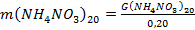 , кг/ч
, кг/ч
18. Масса 90%-ного раствора NH4NO3 после упарки 20%-ного раствора:
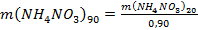 , кг/ч
, кг/ч
19. Масса испарившейся воды:
 , кг/ч
, кг/ч
20. Общая масса выходящего из ИТН 90%-ного раствора:
 , кг/ч
, кг/ч
21. Общая масса выходящего из ИТН сокового пара складывается из основной массы пара, массы потерь HNO3 и NH3, массы дополнительного пара после упарки 20%-ного раствора:
 , кг/ч
, кг/ч
Результаты расчета приведем в таблице материального баланса.
| ПРИХОД | РАСХОД | ||||
| Поток | кг/ч | % | Поток | кг/ч | % |
| 1. Аммиак | 1. Раствор NH4NO3 с м.д. 90% в том числе NH4NO3 Н2О | ||||
| 2. НАК в том числе: HNO3 Н2О | |||||
| 3. Раствор NH4NO3 с м.д. 20% в том числе NH4NO3 Н2О | 2. Соковый пар в том числе Н2О HNO3 NH3 | ||||
| Всего | Всего |
Вопрос №41:Модификационные переходы нитрата аммония и их влияние на качество продукта. Оборудование стадии выпарки, гранулирования и охлаждения в производстве аммиачной селитры. Технологические особенности производства аммиачной селитры.
Модификационные переходы нитрата аммония и их влияние на качество продукта.
Твердый NH4NO3 в зависимости от температуры сущ-ет в 5 кристаллических модификациях т/д устойчивых при атмосферном давлении. Каждая модификация сущ-ет в определ. обл-ти температур и переход одной модификации в другую сопровождается изменениями кристаллической структуры, выделение ( поглоще-нием) тепла, скачкообразным изменением удельного объема и теплоемкости. Полиморфные переходы обратимы. В таблице приведены температуры полиморфных превращений NH4NO3 и происходящие при этом изменения удельного объема.
| Превращ-е | Т-ра превращ-я | Изменения V при охл-ии, дм3/кг | Форма кристаллов |
| Плав ↔ I | 169,6 | Уменьш на 0,054 | I - кубическая |
| I↔II | 125,8 | Уменьш на 0,014 | II - тетрагональная |
| II ↔ III | 84,2 | Уменьш на 0,008 | III – ромбическая моноклинная |
| III↔ IV | 32,2 | Увелич на 0,022 | IV – ромбическая бипирамидальная |
| IV ↔ V | -16,9 | Уменьш на 0,017 | V - тетрагональная |
| II ↔ IV | 50,5 | Увелич на 0,014 | IV – ромбическая бипирамидальная |
По мере охлаждения гранул протекают переходы:
I-II (125°С) – в нижней части грануляционной бани
II-III (84°С) – в аппарате КС
III-IV (32°С) - в зимнее время в аппарате КС
При протекании этих переходов значительно изменяется удельный объем, что приводит к снижению прочности гранул. Избежать эти крайне нежелательные колебания объемов позволяет добавка нитрата магния, при этом структура нитрата аммония благодаря включениям изменяется так, что модификация III исчезает, а II сразу переходит в III при температуре примерно в 50°С.
При переходе II-IV удельный объем изменяется незначительно, т.к. параметры решетки модификации II (тетрагональная) и параметры решетки IV (ромбическая бипирамидальная) – близки друг к другу. В этом случае гранулы сохраняют совю прочность.
Выпарка растворов аммиачной селитры.
 На рис. изображен комбинированный выпарной аппарат, обеспечивающий упаривание растворов аммиачной селитры до содержания влаги не более 0,2%. Он состоит из трех частей: верхней (ɪ) – очистной(сепарационной), средней (ɪɪ) – трубчатой и нижней (ɪɪɪ) – тарельчатой концентрационной.
На рис. изображен комбинированный выпарной аппарат, обеспечивающий упаривание растворов аммиачной селитры до содержания влаги не более 0,2%. Он состоит из трех частей: верхней (ɪ) – очистной(сепарационной), средней (ɪɪ) – трубчатой и нижней (ɪɪɪ) – тарельчатой концентрационной.
В типовом аппарате производительностью 30 т/ч очистное устройство имеет диаметр 3,2 м и предназначено для очистки паровоздушной смеси, выбрасываемой в атмосферу. Оно включает сетчатый отбойник 1 и две ситчатые (переточные) тарелки 3 с отверстиями диаметром 3 мм и свободным сечением около 4%. Межтарельчатое расстояние 500 мм.
При орошении тарелок 3 конденсатом сокового пара последний через штуцер 2 поступает в аппарат и в виде слабого раствора селитры с нижней тарелки перетекает в
трубчатую часть. При подаче на нижнюю очистную тарелку исходного раствора селитры с целью его предварительного упаривания (используются змеевики 4) лишь верхняя тарелка орошается конденсатом, который затем либо выводится на сторону, либо смешивается с исходным раствором селитры. Очистная часть (ɪ) в отдельных случаях может размещаться вне аппарата как самостоятельный узел очистки. Трубчатая часть аппарата идентична трубчатке доупарочного аппарата.
Концентрационная часть аппарата состоит из пяти барботажных тарелок 6 провального типа с отверстиями диаметром 6 мм. Площадь свободного сечения такой тарелки 22%, межтарельчатое расстояние 500 мм. На трех верхних тарелках двумя рядами уложены паровые змеевики 5 общей теплообменной поверхностью 36 м2. Общая высота аппарата (при размещении очистной части над трубчаткой) 13 м.
Внедрение в выпарной аппарат дополнительного выпарного сегмента позволяет модернизировать, существующее в действующих цехах производства аммиачной селитры, выпарное отделение.
Гранулирование аммиачной селитры
Гранулирование амселитры осуществляется в полой грануляционной башне прямоугольного сечения 8х11м, обеспечивающей высоту падения гранул 50м. Гранулирование осуществляется по методу приллирования: проходя выброаккустический гранулятор плав амселитры разбивается на капли, которые падают с высоты 50м и охлаждаются во встречном потоке воздуха, образуя гранулы. Внизу гранбашни имеется металлический конус с щелевидными зазорами для забора воздуха из атмосферы. По всей высоте гранбашни так же имеются окна для дополнительного подсоса воздуха и охлаждения гранул.
Охлаждение гранул аммиачной селитры
Охлаждение гранул происходит в аппарате кипящего слоя (рисунок 19) - аппарате выносного типа прямоугольной формы, разделенного на три секции. Внутри каждой секции аппарата имеются две решётки: кипящего слоя диаметром отверстий 4мм и шагом 12мм, воздухораспределительная с диаметром отверстий 30мм и шагом 70мм. Между секциями на решётке кипящего слоя установлены шиберы, а также двери для выхода воздуха. Каждая секция имеет две выгрузочные течки. Аппарат снабжён грохотом для рассева гранул.
Грохот укомплектован редуктором с электродвигателем мощностью 3 кВт с частотой вращения 750 мин -1 с короткозамкнутым ротором во взрывозащищённом исполнении.
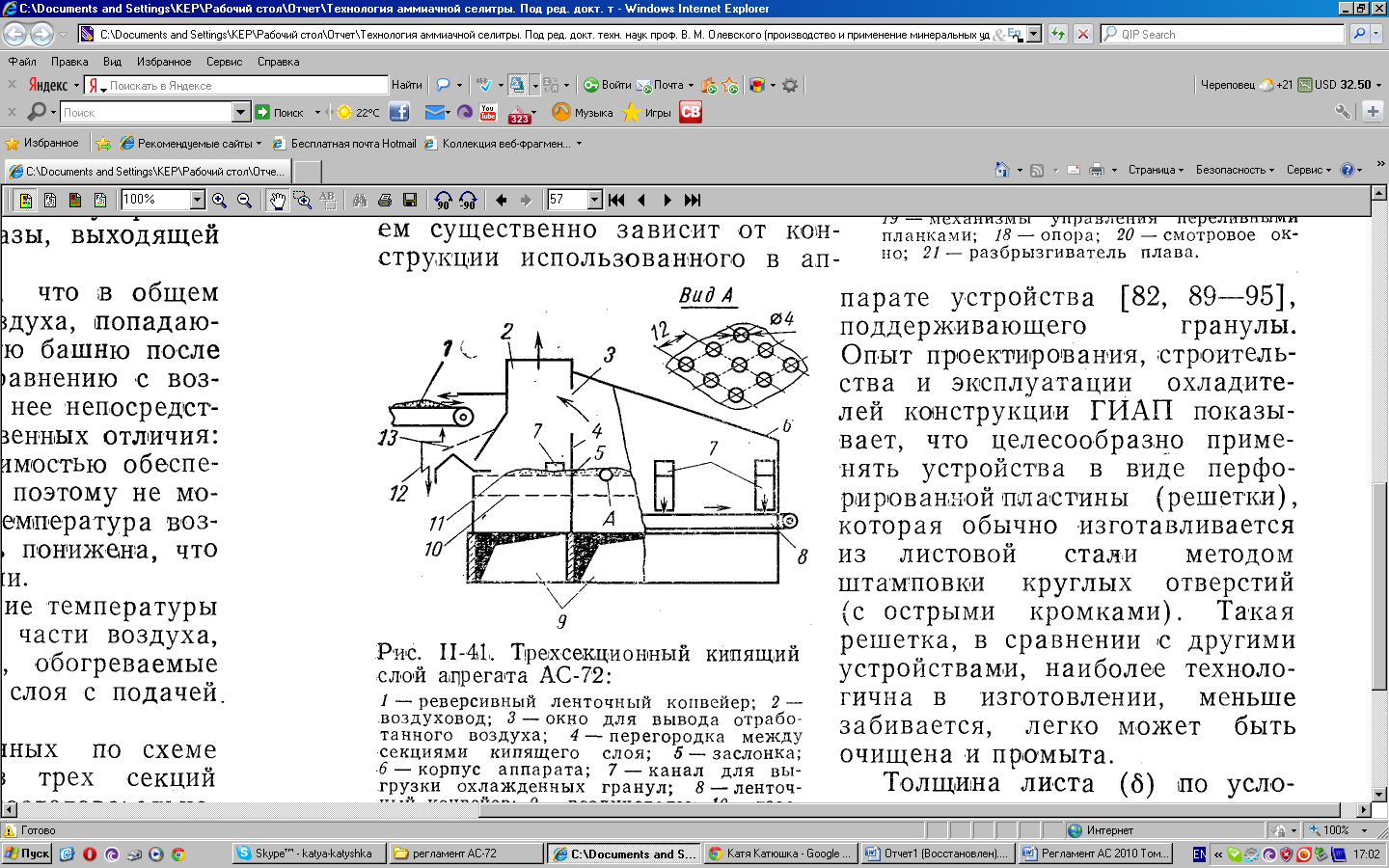
Рис. 19. Трехсекционный кипящий слой агрегата АС-72М:
1 – реверсивный ленточный конвейер, 2 – воздуховод, 3 – окно для выхода отработанного воздуха, 4 – перегородка между секциями кипящего слоя, 5 – заслонка, 6 – корпус аппарата, 7 – канал для выгрузки охлажденных гранул, 8 – ленточный конвейер, 9 – воздуховоды, 10 – газораспределительная решетка, 11 – решетка кипящего слоя, 12 – канал для удаления комков из продукта, 13 – грохот.
Технологические особенности производства аммиачной селитры
1. Используется газообразное, жидкое и твердое сырье. Твердые отходы образуются в незначительном количестве.
2. Протекает необратимая реакция нейтрализации с высокой скоростью, сильно экзотермическая. При этом выделяющееся тепло в значительной мере расходуется на первичное концентрирование раствора NH4NO3.
3. Процесс ведется под атмосферным давлением при температурах до 185°С.
4. Гранулирование осуществляется по методу приллирования (в гранбашне).
5. Продукт – аммиачная селитра – отличается значительной слеживаемостью, для снижения которой используется комплекс мер. Основная из них – применение эффективной кондиционорующей добавки Mg(NO3)2.
6. Аммиачная селитра является взрывчатым веществом средней силы, поэтому в технологическом процессе необходимо строго выдерживать нормы технологического режима и требования безопасности.
Дата добавления: 2015-04-18; просмотров: 1063; Мы поможем в написании вашей работы!; Нарушение авторских прав |