
КАТЕГОРИИ:
АстрономияБиологияГеографияДругие языкиДругоеИнформатикаИсторияКультураЛитератураЛогикаМатематикаМедицинаМеханикаОбразованиеОхрана трудаПедагогикаПолитикаПравоПсихологияРиторикаСоциологияСпортСтроительствоТехнологияФизикаФилософияФинансыХимияЧерчениеЭкологияЭкономикаЭлектроника
Определение коэффициента активности S.
Активность серы исследуют путем выдержки жидкого металла под газовой атмосферой, состоящей из сероводорода и водорода. Изучают реакцию [S]+H2=H2S. Плавку ведут в индукционной печи с графитовым нагревателем, помещенном внутри корпуса печи. Газовую смесь сероводорода и водорода к поверхности металла подводили после тщательной промывки печи аргоном с водородом. Состав смеси газов (H2, H2S) регулировали скоростями потоков. На выходе смесь отбирали и анализировали на содержание серы, когда содержание серы переставало меняться, значит в реакции достигнуто равновесие, тогда можно записать уравнение константы равновесия.
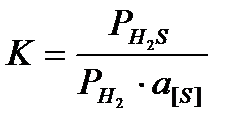
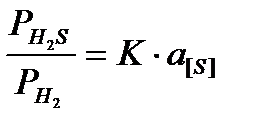
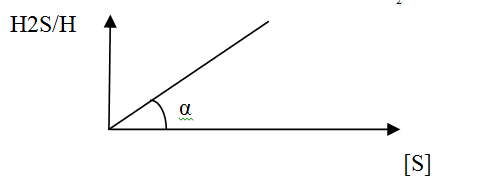
Строится график в координатах « 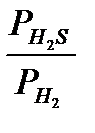 - [S]» (рис.) и экстраполируют его в область Б.Р.Р. где fS = 1, а a[S] = [S], тогда
- [S]» (рис.) и экстраполируют его в область Б.Р.Р. где fS = 1, а a[S] = [S], тогда 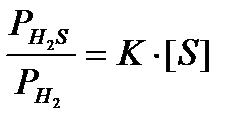 , tg α = K.
, tg α = K. 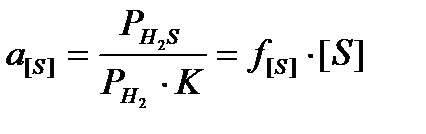
 Отсюда можно найти f[S], взяв любую точку на графике.
Отсюда можно найти f[S], взяв любую точку на графике.
56. Структурно-чувствительные свойства металлических расплавов. Приведите пример экспериментального и теоретического определения одного из структурно-чувствительных свойств: вязкость, поверхностное натяжение, коэффициент диффузии и др. (156-159) Линчевский (90-94) Арсентьев Теоретические методы расчёта спрашивать у +/-
Поверхностное натяжение (σ) – это сила, действующая на единицу периметра поверхности жидкости, она направлена по касательной к поверхности т. о. чтобы сократить поверхность.

Метод лежащей капли.
Небольшое количество металла расплавляют на поверхности с плохой смачиваемостью. Затем определяют форму капли и находят поверхностное натяжение по формуле
σ = ρg/a ρ = m/VK 
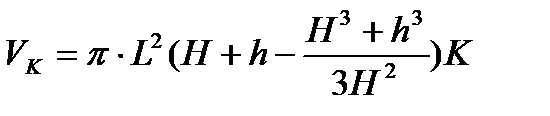
где а – капиллярная постоянная, VK – объем капли, К – учитывает отличие формы нижней части капли от эллипсоида вращения, К = f(θ), θ – угол смачивания.
Теоретическое определение поверхностного натяжения.
Расчет поверхностного натяжения по теплоте испарения.
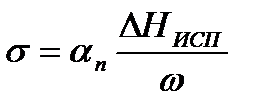

где ΔНИСП – теплота испарения вещества на 1 моль, ω – поверхность, n – координационное число жидкости в глубине фазы, nω - координационное число жидкости в поверхностном слое.
Газовая фаза при атмосферном давлении составлена из 1м3 СО, 1м3 Н2 и 1м3 О2 . Каким будет равновесный состав газовой фазы при температуре 1083К? Как он будет меняться с изменением температуры?
При температуре 1083К Кр=1 (реакция водяного пара)
H2O + CO = H2 + CO2
Все вещества участвуют в эквивалентном соотношении, а значит молей СО израсходовано столько же сколько и воды
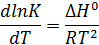
Один метр кубический пересчитываем в число молей.
1 моль газа равен =22,4 л=0,0224 м3 при нормальных условиях.
PV=RnT, находим число молей каждого газа.
К=x(a+x)/(a-x)*x=1
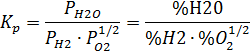

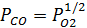

| CO+0,5O2=CO2 | ||||||||
| H2+0,5O2=H2O | ||||||||
| T,K | ||||||||
| Sub | St | DH298 | S298 | |||||
| CO | GAS | -110530 | 197,65 | |||||
| CO2 | GAS | -393510 | 213,66 | |||||
| H2O | LQ | -285830 | 69,95 | |||||
| H2O | GAS | -241810 | 188,72 | |||||
| O2 | GAS | 205,04 | ||||||
| H2 | GAS | 130,52 |
| Sub | St | -2 | Th | DSpt | ||||
| CO | GAS | 23,299 | 0,01343 | -4E-06 | 2,1E-10 | |||
| CO2 | GAS | -184150 | 26,7122 | 0,04957 | -3E-05 | 5,6E-09 | ||
| H2 | GAS | 27,3 | 0,00326 | |||||
| H2O | LQ | 0,07664 | 108,87 | |||||
| H2O | GAS | 0,01071 | ||||||
| O2 | GAS | 21,3536 | 0,02357 | -1E-05 | 1,6E-09 | |||
| O2 | GAS | 31,4054 | 0,00412 | -5E-07 | 3,3E-11 | |||
| O2 | GAS | 29,2149 | 0,00654 | -1E-06 | 1E-10 |
| ΔG | стехиом.коэф 1 | стехиом.коэф. 2 | |||
| СO | -342938,09 | ||||
| O2 | -241092,39 | 0,5 | 0,5 | ||
| CO2 | -651813,88 | ||||
| H2 | -159227,66 | ||||
| H2O | -467961,09 | ||||
| -1115298,2 | |||||
| -188329,59 | |||||
| -188187,24 | |||||
| e | 2,71828183 | ||||
| R | 8,31447315 | ||||
| T | |||||
| Kp1 | 1,2*10^(8) | ||||
| Kp2 | 1,19*10^(8) |
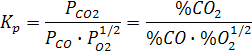
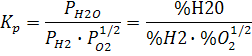


| Так как получили большие значения константы равновесия, то можем сделать вывод о том, что содержание СО2 намного больше, чем сожержание Со и О2 . | |
Для второй реакции можем сделать аналогичный вывод, содержание Н20 много больше, чем Н2 и О2 в системе.
Обобщая выводы 1 и 2 делаем заключение, что при 1083 К газовая фаза будет состоять из Н2О и СО2, с учетом стехиометрических коэффициентов они будут в соотношении 1:1 (50%:50%).
Дата добавления: 2015-04-18; просмотров: 291; Мы поможем в написании вашей работы!; Нарушение авторских прав |