
КАТЕГОРИИ:
АстрономияБиологияГеографияДругие языкиДругоеИнформатикаИсторияКультураЛитератураЛогикаМатематикаМедицинаМеханикаОбразованиеОхрана трудаПедагогикаПолитикаПравоПсихологияРиторикаСоциологияСпортСтроительствоТехнологияФизикаФилософияФинансыХимияЧерчениеЭкологияЭкономикаЭлектроника
Вычисление результатов. Концентрацию растворенного в воде кислорода (Сх, мг/л) определяют по формуле:
Концентрацию растворенного в воде кислорода (Сх, мг/л) определяют по формуле:
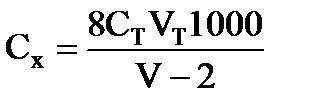 ,
,
где СТ - концентрация раствора тиосульфата натрия, моль-экв/л; VТ - объем раствора тиосульфата натрия, пошедший на титрование, мл; V - вместимость склянки для определения БПК5, мл; 2 - объем пробы, вылившийся при фиксации растворенного кислорода, мл; 8 - масса моль - эквивалента кислорода.
Концентрацию растворенного в воде кислорода в процентах от концентрации насыщения (О2, %) находят по формуле:
 ,
,
Сх - концентрация О2, найденная экспериментально, мг/л; С0 - нормальная концентрация при данной температуре, атмосферном давлении, нормальности и атмосферном давлении 760 мм рт. ст. (таблица 3.2), мг/л; Р - атмосферное давление в момент анализа, мм рт. ст.
Содержание растворенного кислорода в поверхностных водных объектах должно быть не менее 4 мг/л.
Таблица 3.2
Зависимость равновесной концентрации кислорода (С0)
от температуры (атмосферное давление 760 мм рт. ст.,
парциальное давление кислорода р = 0,209 атм)
| t, °С | Растворенный кислород, мг/л | |||||||||
| 0,0 | 0,1 | 0,2 | 0,3 | 0,4 | 0,5 | 0,6 | 0,7 | 0,8 | 0,9 | |
| 14,65 | 14,61 | 14,57 | 14,53 | 14,49 | 14,45 | 14,41 | 14,37 | 14,33 | 14,29 | |
| 14,25 | 14,21 | 14,17 | 14,13 | 14,09 | 14,05 | 14,02 | 13,98 | 13,94 | 13,90 | |
| 13,86 | 13,82 | 13,79 | 13,75 | 13,71 | 13,68 | 13,64 | 13,60 | 13,56 | 13,53 | |
| 13,49 | 13,46 | 13,42 | 13,38 | 13,35 | 13,31 | 13,28 | 13,24 | 13,20 | 13,17 | |
| 13,13 | 13,10 | 13,06 | 13,03 | 13,00 | 12,96 | 12,92 | 12,89 | 12,86 | 12,82 | |
| 12,79 | 12,76 | 12,72 | 12,69 | 12,66 | 12,62 | 12,59 | 12,56 | 12,53 | 12,49 | |
| 12,48 | 12,43 | 12,40 | 12,36 | 12,33 | 12,30 | 12,27 | 12,24 | 12,21 | 12,18 | |
| 12,14 | 12,11 | 12,08 | 12,05 | 12,02 | 11,99 | 11,96 | 11,93 | 11,90 | 11,87 | |
| 11,84 | 11,81 | 11,78 | 11,75 | 11,72 | 11,70 | 11,67 | 11,64 | 11,61 | 11,58 | |
| 11,55 | 11,52 | 11,49 | 11,47 | 11,44 | 11,41 | 11,38 | 11,35 | 11,33 | 11,30 | |
| 11,27 | 11,24 | 11,22 | 11,19 | 11,16 | 11,14 | 11,11 | 11,08 | 11,06 | 11,03 | |
| 11,00 | 10,98 | 10,95 | 10,93 | 10,90 | 10,87 | 10,85 | 10,82 | 10,80 | 10,77 | |
| 10,75 | 10,72 | 10,70 | 10,67 | 10,65 | 10,62 | 10,60 | 10,57 | 10,55 | 10,52 | |
| 10,50 | 10,48 | 10,45 | 10,43 | 10,40 | 10,38 | 10,36 | 10,33 | 10,31 | 10,28 | |
| 10,26 | 10,24 | 10,22 | 10,19 | 10,17 | 10,15 | 10,12 | 10,10 | 10,08 | 10,06 | |
| 10,03 | 10,01 | 9,99 | 9,97 | 9,95 | 9,92 | 9,90 | 9,88 | 9,86 | 9,84 | |
| 9,82 | 9,79 | 9,77 | 9,75 | 9,73 | 9,71 | 9,69 | 9,67 | 9,65 | 9,63 | |
| 9,61 | 9,58 | 9,56 | 9,54 | 9,52 | 9,50 | 9,48 | 9,46 | 9,44 | 9,42 | |
| 9,40 | 9,38 | 9,36 | 9,34 | 9,32 | 9,30 | 9,29 | 9,27 | 9,25 | 9,23 | |
| 9,21 | 9,19 | 9,17 | 9,15 | 9,13 | 9,12 | 9,10 | 9,08 | 9,06 | 9,04 | |
| 9,02 | 9,00 | 8,98 | 8,97 | 8,95 | 8,93 | 8,91 | 8,90 | 8,88 | 8,86 | |
| 8,84 | 8,82 | 8,81 | 8,79 | 8,77 | 8,75 | 8,74 | 8,72 | 8,70 | 8,68 | |
| 8,67 | 8,65 | 8,63 | 8,62 | 8,60 | 8,58 | 8,56 | 8,55 | 8,53 | 8,52 | |
| 8,50 | 8,48 | 8,46 | 8,45 | 8,43 | 8,42 | 8,40 | 8,38 | 8,37 | 8,35 | |
| 8,33 | 8,32 | 8,30 | 8,29 | 8,27 | 8,25 | 8,24 | 8,22 | 8,21 | 8,19 | |
| 8,18 | 8,16 | 8,14 | 8,13 | 8,11 | 8,10 | 8,08 | 8,07 | 8,06 | 8,04 | |
| 8,02 | 8,01 | 7,99 | 7,98 | 7,96 | 7,95 | 7,93 | 7,92 | 7,90 | 7,89 | |
| 7,87 | 7,86 | 7,84 | 7,83 | 7,81 | 7,80 | 7,78 | 7,77 | 7,75 | 7,74 | |
| 7,72 | 7,71 | 7,69 | 7,68 | 7,66 | 7,65 | 7,64 | 7,62 | 7,61 | 7,59 | |
| 7,58 | 7,56 | 7,55 | 7,54 | 7,52 | 7,51 | 7,49 | 7,48 | 7,47 | 7,45 | |
| 7,44 | 7,42 | 7,41 | 7,40 | 7,38 | 7,37 | 7,35 | 7,34 | 7,32 | 7,31 |
Химическое потребление кислорода (ХПК) в водах
Определение ХПК основано на окислении органических веществ избытком дихромата калия в растворе серной кислоты при нагревании в присутствии катализатора - сульфата серебра. Остаток K2Cr2O7 находят титрованием раствором соли Мора и, исходя из полученных результатов, определяют количество дихромата калия, израсходованное на окисление органических веществ.
Определению мешают хлориды, сульфиды, соединения железа (II), нитриты и другие неорганические вещества, способные окисляться K2Cr2O7 в кислой среде.
Мешающее влияние хлоридов при концентрациях менее 300 мг/л устраняется за счет присутствия в пробе Ag2SO4. При С(Cl-) ³ 300 мг/л к анализируемой пробе добавляют сульфат ртути (II) из расчета 100 мг HgSO4 на 10 мг хлоридов.
Мешающее влияние сульфидов и соединений железа (II) устраняют предварительной продувкой пробы воздухом, если она не содержит летучих органических соединений, или учитывают при расчете ХПК. В последнем случае определяют их концентрации и пересчитывают на величины ХПК, исходя из того, что 1 мг H2S и 1 мг Fe2+ эквивалентны соответственно 0,47 и 0,14 мг О2. Таким же образом учитывают влияние нитритов: 1 мг 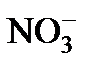 эквивалентен 0,35 мг О2.
эквивалентен 0,35 мг О2.
Дата добавления: 2015-04-11; просмотров: 492; Мы поможем в написании вашей работы!; Нарушение авторских прав |