
КАТЕГОРИИ:
АстрономияБиологияГеографияДругие языкиДругоеИнформатикаИсторияКультураЛитератураЛогикаМатематикаМедицинаМеханикаОбразованиеОхрана трудаПедагогикаПолитикаПравоПсихологияРиторикаСоциологияСпортСтроительствоТехнологияФизикаФилософияФинансыХимияЧерчениеЭкологияЭкономикаЭлектроника
Равновесие в гетерогенных системах с участием газов.
Рассмотрим химическое равновесие в гетерогенной системе при наличии газовой, жидкой и твёрдой фаз:

Предположим, что А, В, С не растворяются в D. Равновесные парциальные давления идеальных газов обозначим РА и РС. Тогда условия равновесия для такой системы запишутся так

|
(7.7)
где μВ и μD не зависят от количества В и D, т. к. они образуют отдельные

|

|
Фазы. Величины
и
Не зависят и от давления из-за малости

|
| ). Следовательно, (7.7) можно переписать |
мольных объёмов конденсированных фаз (напомним уравнение

|
Выражение под логарифмом зависит только от температуры и тоже есть константа равновесия

|
Рп
В константу равновесия входят только газовые компоненты. Окончательно запишем
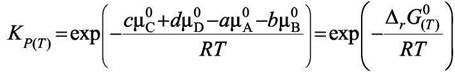
|
(7.8)
Необходимо обратить внимание на то, что константа равновесия зависит от природы конденсированных фаз(см. правую часть уравнения 7.8), хотя в саму  конденсированные фазы не входят. Все выводы останутся справедливыми, если твёрдое вещество "В" будет растворяться в жидкости "D". В этом случае вместо
конденсированные фазы не входят. Все выводы останутся справедливыми, если твёрдое вещество "В" будет растворяться в жидкости "D". В этом случае вместо  в формулы войдёт величина
в формулы войдёт величина 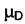 - химический потенциал D в насыщенном растворе "В" в "D", отличающийся от химического потенциала чистой жидкости. Отметим, что химический потенциал "В" в насыщенном растворе совпадает с
- химический потенциал D в насыщенном растворе "В" в "D", отличающийся от химического потенциала чистой жидкости. Отметим, что химический потенциал "В" в насыщенном растворе совпадает с 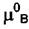 вследствие фазового равновесия для вещества "В".
вследствие фазового равновесия для вещества "В".
Дата добавления: 2014-12-23; просмотров: 282; Мы поможем в написании вашей работы!; Нарушение авторских прав |