
КАТЕГОРИИ:
АстрономияБиологияГеографияДругие языкиДругоеИнформатикаИсторияКультураЛитератураЛогикаМатематикаМедицинаМеханикаОбразованиеОхрана трудаПедагогикаПолитикаПравоПсихологияРиторикаСоциологияСпортСтроительствоТехнологияФизикаФилософияФинансыХимияЧерчениеЭкологияЭкономикаЭлектроника
Восстановительные свойства углерода
1. Тщательно перемешать небольшие равные количества оксида меди (II) и измельченного в порошок древесного угля и поместить смесь в тугоплавкую пробирку. Прогреть всю пробирку пламенем спиртовки до изменения цвета смеси с черного на красный. Описать и объяснить наблюдаемые явления. Написать уравнение реакции.
2. В цилиндрическую пробирку поместить 2-3 капли концентрированной серной кислоты (плотность 1,84 г/см3) и маленький кусочек угля. Укрепить пробирку в штативе и на маленьком пламени горелки осторожно подогреть ее. Наблюдать выделение пузырьков газа. По запаху определить один из выделяющихся газов. Написать уравнение реакции восстановления углем серной кислоты.
Получение и восстановительные свойства оксида углерода (II).
Оксид углерода (II) - яд! Осторожно! Опасен для здоровья
Работать в вытяжном шкафу!
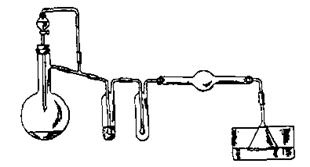
| 1. Собрать прибор (рис. 57). В колбу Вюрца внести 2-3 капли концентрированный серной кислоты (d=1,84 г/см3) и 4-6 капель муравьиной кислоты (НСООН). В хлоркальциевую трубку насыпать немного оксида меди. Осторожно нагреть трубку с оксидом меди до высокой температуры и слегка подогреть смесь в реакционной колбе. |
| Рис. 57. Прибор для синтеза оксида углерода (II) |
Наблюдать изменение окраски порошка в трубке. Избыток оксида углерода (II) можно поджечь у выхода из газоотводной трубки. Описать и объяснить наблюдаемые явления. Написать уравнения реакции.
2. В пробирку внести 2-3 капли концентрированной серной кислоты (d=1,84 г/см3) и 4-6 капель муравьиной кислоты. Пробирку закрыть пробкой с газоотводной трубкой, слегка подогреть и выделяющейся газ пропустить через аммиачные растворы нитрата серебра и хлорида меди (5-6 капель). Написать уравнения реакций.
Дата добавления: 2014-12-30; просмотров: 340; Мы поможем в написании вашей работы!; Нарушение авторских прав |