
КАТЕГОРИИ:
АстрономияБиологияГеографияДругие языкиДругоеИнформатикаИсторияКультураЛитератураЛогикаМатематикаМедицинаМеханикаОбразованиеОхрана трудаПедагогикаПолитикаПравоПсихологияРиторикаСоциологияСпортСтроительствоТехнологияФизикаФилософияФинансыХимияЧерчениеЭкологияЭкономикаЭлектроника
Печатается по решению редакционно-издательского совета Иркутского государственного технического университета.
Этот метод позволяет предсказать структуру (геометрию молекул). В 1940 г его предложили Сиджвик и Пауэлл, а в 1957 г он был усовершенствован Гиллеспи и Найхамом.
1. Расположение электронных пар вокруг центрального атома в молекуле зависит от числа таких пар: они принимают пространственное положение, сводящее к минимуму их взаимное отталкивание.
2. По степени взаимного отталкивания электронные пары располагаются в ряд: НП−НП > НП−СП > СП−СП (отталкивание убывает). НП − несвязывающая (неподеленная) электронная пара ближе расположена к ядру и облако неподеленной пары электронов занимает большее пространство, чем связывающей электронной пары (СП).
3. Электронные пары занимают такие позиции, чтобы углы между ними были максимальны, а отталкивание минимально. Поэтому из нескольких возможных структур, включающих взаимодействие под углом 90°, наиболее благоприятна структура, обладающая наименьшим числом взаимодействий под углом 90° с неподеленной парой.
4. Электронное облако двойной связи занимает большее пространство, чем облако одинарной связи.
5. Чем более электроотрицателен атом − партнер центрального атома, тем меньше пространства вблизи центрального атома требуется для электронной пары. Так как она оттянута к атому-сосоду.
Подсчитывают стерическое число (СЧ) для центрального атома в молекуле, и в зависимости от его значения − такова и геометрия.
СЧ есть сумма связывающих электронных пар (т.е. число связей) и неподеленных электронных пар:
СЧ = СП + НП.
Если у центрального атома нет неподеленных пар, то СЧ = СП.
Кратность связи не влияет на предсказанные структуры: СЧ(ВН2) = СЧ(СО2) = 2.
Если один из присоединенных атомов заменен неподеленной парой, то геометрия молекулы меняется:
| АВ3 | АВ2Е |
| СЧ = 3 | СЧ = 2 + 1 |
| А − центральный атом; В − заместители (периферические атомы); Е − неподеленная электронная пара плоская треугольная молекула угловая молекула |
или
| АВ4 | АВ3Е | АВ2Е2 |
| СЧ (СН4) = 4 + 0 | СЧ(:NH3) = 3 + 1 | СЧ(Н2  :) = 2 + 2 :) = 2 + 2
|
| тетраэдрическое строение | тригональная пирамида | угловая |
| валентный угол 109,5° | валентный угол 107,3° | валентный угол 104,5° |
| Тип гибридизации центрального атома А | Стерическое число для центрального атома СЧ = СП + НП | Состав молекулы | Структура молекулы | Примеры | |
| СЧ | НП | ||||
| sp или dp | АВ2 | 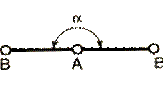 линейная
линейная
| BeCl2; HgCl2; CO2 | ||
| sp2, dp2 или sd2 | АВ3 |  плоская треугольная
плоская треугольная
| BF3; SO3; NO3−; CO32−; COCl2 | ||
| АВ2Е |  угловая (изогнутая)
угловая (изогнутая)
| SnCl2; SO2; O3 | |||
| sp3 или sd3 | АВ4 |  тетраэдрическая
тетраэдрическая
| CH4; CCl4; NH4+; PO43−; POCl3 | ||
| АВ3E |  тригональная призма
тригональная призма
| NH3; PF3; AsCl3; H3O+ | |||
| АВ2E2 |  угловая (изогнутая)
угловая (изогнутая)
| H2O; H2S; SF2 | |||
sp3d  или spd3 или spd3
| АВ5 | 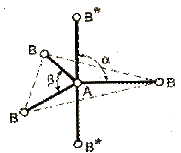 тригональная бипирамида
тригональная бипирамида
| PF5 | ||
| АВ4E |  искаженная тетраэдрическая
искаженная тетраэдрическая
| SF4 | |||
| АВ3E2 |  Т − образная
Т − образная
| ClF3 | |||
| АВ2E3 |  линейная
линейная
| XeF2; I3−; IF3 | |||
| sp3d2 (dxy, dyz) | АВ6 |  октаэдрическая
октаэдрическая
| SF6; PF6−; SiF62− | ||
| АВ5E |  квадратная пирамида
квадратная пирамида
| IF5 | |||
| АВ4E2 |  квадратная плоская
квадратная плоская
| XeF4; IF4− | |||
| sp3d4 | АВ8 |  додекаэдр
додекаэдр
|
 |
Печатается по решению редакционно-издательского совета Иркутского государственного технического университета.
Английский язык. Программа, методические указания и контрольные задания для студентов-заочников Иркутского государственного технического университета / сост. Дементьева О.В., Новоселова И.Н., Развозжаева О.Ю., Ханхараева М.Ф. - Иркутск, ИрГТУ, 2001 - 69с.
Пособие состоит из программы, методических указаний и контрольных работ. Пособие предназначено для изучения и закрепления грамматических структур английского языка, лексики по специальности "юриспруденция" и "мировая экономика", а также для формирования навыков работы с текстом. Задания контрольных работ составлены но принципу "от простого к сложному", что облегчает овладение материалом.
Цель пособия: помочь студентам заочного обучения овладеть навыками самостоятельной работы с грамматическим материалом, с текстом и сформировать умение работы со словарем.
Составители: к.ф.н., доцент О.В. Дементьева
ст. преподаватель И.Н. Новоселова, ст. преподаватель О.Ю. Развозжаева, ст. преподаватель М.Ф. Ханхараева
Рецензенты:к.л.н., доцент кафедры иностранных языков Иркутского юридического института Генеральной прокуратуры РФ Милорадов С.А.
к.ф.н., доцент кафедры иностранныхязыков Иркутского государственного технического университета Попова М.И.
Дата добавления: 2015-01-01; просмотров: 264; Мы поможем в написании вашей работы!; Нарушение авторских прав |