
КАТЕГОРИИ:
АстрономияБиологияГеографияДругие языкиДругоеИнформатикаИсторияКультураЛитератураЛогикаМатематикаМедицинаМеханикаОбразованиеОхрана трудаПедагогикаПолитикаПравоПсихологияРиторикаСоциологияСпортСтроительствоТехнологияФизикаФилософияФинансыХимияЧерчениеЭкологияЭкономикаЭлектроника
Применение комплексных соединений в медицине и химическом анализе
Как упоминалось ранее, в состав комплексных соединений в качестве лигандов входят и биологически важные соединения: аминокислоты, белки, полипептиды, нуклеиновые кислоты, порфирины, АТФ. Изучение процессов, протекающих в организме с образованием комплексных соединений, может иметь большое значение для профилактики и лечения ряда заболеваний.
Белки являются полидентатными лигандами и хорошо связываются с тяжелыми металлами. При отравлении солями тяжелых металлов пострадавшему дают пить молоко и сырые яйца, которые содержат много белков. Образующиеся комплексные соединения не всасываются в кровь из кишечника и тяжелые металлы таким образом выводятся из организма.
Наибольшее распространение в живой природе получили порфирины (рис. 4.1), которые входят в состав гемоглобина, хлорофилла и некоторых ферментов (каталаза, пероксидаза). Порфирины имеют донорные атомы азота и образуют прочные координационные соединения с катионами различных элементов. Так, в качестве центрального атома может выступать ион магния Mg2+. В результате образуется активный центр хлорофилла - зеленого пигмента растений. Если присутствуют ионы Fe2+ или Си+, обра-
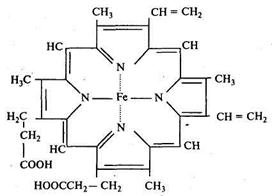
Рис. 4.1. Кольцо порфирина с ионами Fe2+
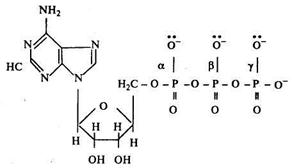
Рис. 4.2. АТФ
зуются активные центры гемоглобина и гемоцианина. Ион кобальта Со3+ является центральным атомом в витамине В12, который представляет собой бионеорганическое комплексное соединение порфиринового ряда.
Главным источником энергии для многих биологических процессов является АТФ, которая находится в организме в виде комплексных солей кальция и магния. Атомы кислорода в фосфатных группах являются донорами, причем донорные свойства наиболее сильно выражены у кислорода β- и γ-фосфатов(рис.4.2). Препараты АТФ применяются при мышечных дистрофиях, стенокардии и спазмах сосудов.
В медицинской практике и в аналитической химии широко используются комплексоны. Среди них наиболее важное значение имеет ЭДТА, строение которого нами рассматривалось ранее. С помощью этой соли ускоряется выведение из организма токсичных металлов: свинца, ртути, кадмия, бария и др. Образующиеся комплексные соединения водорастворимы и практически не расщепляются в биологической среде, что является их фармакологической особенностью. ЭДТА способствует выведению из организма плутония. Важно заметить, что плутоний реагирует с ЭДТА «раньше», чем с солями кальция, и последний не будет извлекаться из крови и костей. Способность к образованию прочных комплексных соединений со многими металлами проявляется и у других солей ЭДТА — кальциевых, кобальтовых. Например, кальциевая соль СаNа2ЭДТА (тетацин) широко используется при отравлении свинцом.
Некоторые комплексы платины замедляют рост злокачественных заболеваний, а комплексы золота с α-тиоспиртами оказывают лечебное действие при туберкулезе и проказе.
Жизненно необходимые элементы Zn, Cu, Fe, Mn, Со, Мо входят в состав определенных ферментов, которые называются металлоферментами. Они выполняют специфические функции в организме. Наиболее известные металлоферменты: карбоангидраза, ксантиноксидаза, цитохромы – в активных центрах содержат цинк, молибден и железо соответственно. Лигандами в металлоферментах выступают белки, а комплексообразователями — ионы металлов.
Реакции комплексообразования лежат в основе многих методов химического анализа. Их широко используют для обнаружения, определения, маскировки ионов, растворения, разделения и концентрирования веществ.
Обнаружение отдельных ионов в качественном анализе осуществляется с помощью комплексных соединений. Процесс обнаружения сопровождается разрушением исходных и образованием новых комплексных соединений, что ведет к появлению или изменению цвета осадков или растворов. Например, это наблюдается при проведении реакций обнаружения ионов К+, Fe2+, Fe3+, Cu2+ и др.:
Na3[Co(NO2)6] + 2KCl = K2Na[Co(NO2)6]↓ + 2NaCl;
Желтый
3FeSO4 + 2K3[Fe(CN)6] = Fe3[Fe(CN)6]2↓+ 3K2SO4;
Темно-синий
4FeCl3 + 3K4[Fe(CN)6] = Fe4[Fe(CN)6]3↓ + 12KCl;
Синий
CuSO4 + 4NH3 = [Cu(NH3)4]SO4.
Избыток Ярко-синий
Комплексные соединения используются также для устранения мешающего влияния некоторых ионов («маскировка» ионов). Например, ион железа Fe3+, мешающий определению ряда катионов, маскируют, связывая его в комплекс с фторид-ионами [FeF6]-3 или винной, или лимонной кислотами.
При обнаружении ионов Zn2+ в присутствии ионов Fe3+ с помощью реактива (NH4)2[Hg(SCN)4] катионы Fe3+ образуют соединение Fe(SCN)3, имеющее кроваво-красную окраску. Поэтому в присутствии ионов Fe3+ белый осадок комплексного соединения цинка не виден.
Комплексные соединения применяются для изменения кислотно-основных и окислительно-восстановительных свойств катионов и анионов. При связывании слабых кислот в комплекс их сила увеличивается вследствие ослабления связи аниона с ионами водорода. Например, кислотные свойства щавелевой кислоты увеличиваются в присутствии ионов магния Mg2+, так как образующийся комплекс H2[Mg(C2O4)2] обладает большей силой как кислота. Аналогично возрастает сила борной кислоты при ее связывании в комплекс с глицерином или маннитом, имеющими несколько гидроксильных групп. При анализе катионов и анионов комплексообразование может усиливать или ослаблять окислительно-восстановительные свойства соединений. Например, окислительные свойства ионов Fe3+ резко понижаются в случае образования оксалат-ионами С2С2-4, фосфат-ионами РО3-4 и фторид-ионами F- прочных комплексных ионов:
[Fe(C2O4)3]3-, [Fe(PO4)2]3-, [FeF3]3-.
Комплексообразование широко используется в анализе для перевода малорастворимых соединений в раствор и разделения ионов. Например, осадок HgI2 растворяется в избытке KI с образованием водорастворимого комплекса K2[HgI4]; осадок AgCl растворяется в растворе аммиака с образованием комплекса [Ag(NH3)2]Cl.
Способность осадка AgCl растворяться в растворе аммиака в отличие от осадка Hg2Cl2, позволяет отделить ионы Ag+ от ионов Hg22+.
Реакции комплексообразования легли в основу многих количественных определений металлов.
ВОПРОСЫ И УПРАЖНЕНИЯ
1. Какие ионы называются комплексными?
2. Чем отличаются комплексные соединения от двойных солей?
3. Как диссоциируют комплексные соединения и двойные соли в водных растворах? Приведите примеры.
4. Что такое ион-комплексообразователь? Какие ионы могут выполнять роль комплексообразователя?
5. Что такое лиганды? Приведите примеры.
6. Что такое координационное число? Какие ионы имеют координационные числа 2, 4, 6? Приведите примеры.
7. Что такое дентатность? Приведите примеры моно- би- и полидентатных лигандов.
8. Как классифицируются комплексные соединения? Приведите примеры.
9. Какие величины характеризуют устойчивость комплексных соединений?
10. Что такое хелатные и внутрикомплексные соединения. Объясните различие между ними.
11. К какому типу солей относятся K3[Fe(CN)6], (NH4)2SO4 • FeSO4,
K4[Fe(CN)6], K2CO3 • Na2CO3?
12. Определите степень окисления иона-комплексообразователя в следующих комплексных ионах: [PtCl6]2-; [Сu(СN)4]2-; [Ni(NH3)5Ci]+; [Со(NН3)2(МO2)4]-;[Сr(Н2O)4Вr2]+; [Hg(CN)4]2-; [Ag(S2O3)2]3-.
13. Укажите комплексообразователь, лиганды и координационное число в комплексных соединениях: K2[HgI4]; H3[AlF6]; H[BF4]; [PtCl(NH3)5]Cl; [Co(H2O)6](NO3)3.
14. Укажите величину и знак заряда комплексных ионов: [Сr(Н2О)4Сl2]Сl, [Ni(NH3)5Cl], [Co(NH3)5Br], K[Ag(CN)2], Zn2[Fe(CN)6].
15. Укажите внешнюю и внутреннюю координационную сферы комплексных соединений: K4[Fe(CN)6]; [Pt(NH3)5Cl]Cl3; K[Sb(OH)6]; [Co(NH3)6]SO4; Na3[Co(NO2)6]. Напишите уравнения диссоциации этих комплексных соединений.
16. Назовите комплексные соединения: K4[Fe(CN)6]; К3[Fе(СN)6]; [Cr(NH3)6](NO3)3, [Ag(NH3)2]Cl, K[Co(NH3)2(NO2) 4].
17. Напишите химические формулы следующих комплексных соединений: а ) дицианоаргентат калия; б) гексацианофер-рат (II) цинка; в) хлорид дихлоротетрааква хрома (III); г) гексахлороплатинат (IV) калия; д) бромид гексаамминкобалъта (III).
18. Составьте формулы комплексных соединений: а) комплексообразователь Со3+; координационное число 6, лиганды - молекулы, воды, во внешней координационной сфере находятся нитрат-ионы; б) комплексообразователь Pt2+, координационное число 4, лиганды - Cl-ионы, во внешней сфере находятся ионы калия; в) комплексообразователь Сr3+, координационное число 6, лиганды - три молекулы аммиака и три Cl--иона, внешней координационной сферы нет.
Дата добавления: 2014-11-13; просмотров: 643; Мы поможем в написании вашей работы!; Нарушение авторских прав |