
КАТЕГОРИИ:
АстрономияБиологияГеографияДругие языкиДругоеИнформатикаИсторияКультураЛитератураЛогикаМатематикаМедицинаМеханикаОбразованиеОхрана трудаПедагогикаПолитикаПравоПсихологияРиторикаСоциологияСпортСтроительствоТехнологияФизикаФилософияФинансыХимияЧерчениеЭкологияЭкономикаЭлектроника
Обратимые и необратимые процессы.
Процесс называют обратимым, если он может совершаться как в прямом, так и в обратном направлениях, причем, двигаясь в обратном направлении, он проходит те же состояния, что и в прямом направлении, и после возвращения в начальное состояние в окружающей среде не наблюдается каких-либо изменений. Это возможно только в том случае, если на произвольном элементарном участке в прямом направлении система получает тепло  и совершает работу
и совершает работу 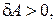 а при обратном движении на том же участке система должна отдать точно такое же количество тепла
а при обратном движении на том же участке система должна отдать точно такое же количество тепла  и над системой должна быть совершена точно такая же работа
и над системой должна быть совершена точно такая же работа  что и в прямом направлении. Тогда, действительно, в окружающей среде не произойдет никаких изменений.
что и в прямом направлении. Тогда, действительно, в окружающей среде не произойдет никаких изменений.
Если при проведении прямого, а затем обратного процессов систему нельзя вернуть в исходное состояние так, чтобы она проходила через те же промежуточные состояния, но только в обратном порядке и в среде не осталось никаких изменений, то процесс называют необратимым. Из опыта известно, что обратимых процессов в природе не существует; все процессы необратимы. Приведем примеры.
1. Пусть имеется теплоизолированный сосуд, разделенный перегородкой на две части. В одной из частей находится идеальный газ, в другой –вакуум. Если убрать перегородку, газ равномерно распространится по всему объему. Обратный процесс самопроизвольно никогда не протекает. Значит, процесс самопроизвольного расширения газа в вакуум необратим.
2. Два контактирующих тела с разными температурами 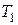 и
и 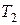 в конце концов приобретают одинаковую температуру. Обратный процесс самопроизвольного возникновения температур
в конце концов приобретают одинаковую температуру. Обратный процесс самопроизвольного возникновения температур 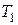 и
и 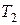 в тех же телах никогда не происходит. Таким образом, процесс теплопроводности необратим.
в тех же телах никогда не происходит. Таким образом, процесс теплопроводности необратим.
3. Необратим процесс образования раствора или смеси. Например, если смешать спирт с водой, то самопроизвольно компоненты этого раствора никогда не отделятся друг от друга.
4. Необратим любой процесс, сопровождающийся трением. При трении часть работы, совершаемой телом, всегда превращается в теплоту. Однако обратно эта теплота не может самопроизвольно собраться к трущимся поверхностям и полностью превратиться в работу.
Так как практически все реальные процессы происходят с участием сил трения и теплопроводности, то можно сказать, что действительно, все процессы в природе необратимы.
Любой из рассмотренных необратимых процессов можно провести в обратном направлении и вернуть систему в начальное состояние.
Так, газ, расширяющийся в пустоту, может быть возвращен в исходное состояние вакуумным насосом, но на приведение его в действие необходимо затратить внешнюю работу тогда как при расширении газ не совершал работу.
Во втором примере температуры тел тоже можно вернуть в исходное состояние, если использовать для этой цели холодильную машину (см. п. 2.9). Но на приведение ее в действие снова необходимо затратить внешнюю работу, в то время как при выравнивании температур тел макроскопическая работа не совершалась.
В третьем примере для разделения компонентов водного раствора спирта можно использовать ректификационную установку, затратив определенное количество теплоты, взятой от внешнего источника.
Наконец, в четвертом примере тело можно вернуть в начальное состояние, затратив внешнюю работу, равную убыли энергии тела, вызванной трением.
Следовательно, хотя каждый из рассмотренных необратимых процессов вернулся в исходное состояние, это возвращение произошло за счет необратимых изменений в окружающей систему среде, т. е. в этой среде остался след обратного процесса.
Подытоживая сказанное, можно сделать вывод: самопроизвольные процессы принципиально не могут быть обратимыми.
Однако в некоторых случаях степень необратимости может оказаться настолько незначительной, что процесс можно с достаточной точностью считать обратимым. Например, необратимый переход теплоты от более нагретого тела к менее нагретому может иметь разную степень необратимости: процесс перехода теплоты от тела с температурой 500 K к телу с температурой 50 K отстоит от обратимого процесса гораздо дальше, чем процесс перехода теплоты от тела с температурой 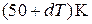 к телу с температурой 50 K. Система этих двух тел с разностью температур dT находится почти в равновесии и потому процесс теплообмена между ними может идти как в прямом, так и в обратном направлении: для того чтобы тепло переходило в обратном направлении, достаточно телу с меньшей температурой передать от внешнего источника бесконечно малое количество тепла. Если же разность температур тел конечная, то бесконечно малым количеством тепла нельзя изменить направление процесса теплообмена.
к телу с температурой 50 K. Система этих двух тел с разностью температур dT находится почти в равновесии и потому процесс теплообмена между ними может идти как в прямом, так и в обратном направлении: для того чтобы тепло переходило в обратном направлении, достаточно телу с меньшей температурой передать от внешнего источника бесконечно малое количество тепла. Если же разность температур тел конечная, то бесконечно малым количеством тепла нельзя изменить направление процесса теплообмена.
Приведем другой пример. Пусть газ находится под невесомым поршнем и расширяется в результате того, что его давление на бесконечно малую величину больше, чем внешнее давление среды.
Газ находится почти в равновесии с внешней средой. Поэтому бесконечно малым внешним воздействием можно изменить процесс расширения на обратный процесс сжатия газа. Если же давление газа больше давления окружающей среды на конечную величину, то бесконечно малым воздействием невозможно изменить процесс расширения на обратный процесс сжатия газа.
Таким образом, свойством обратимости должен обладать равновесный процесс, состоящий, как мы знаем, из непрерывной последовательности равновесных состояний, или, что то же самое, процесс, протекающий бесконечно медленно. В любой момент времени направление равновесного процесса может быть изменено на обратное бесконечно малым воздействием. Все ранее рассмотренные политропные процессы были процессами равновесными и, стало быть, обратимыми. Необратимыми являются все процессы, сопровождающиеся трением, протекающие с конечной скоростью. Необратимыми процессами также являются процессы, происходящие при конечной разности температур, процессы диффузии, процессы расширения газа в пустоту и вообще все процессы, происходящие самопроизвольно. Обратимые же процессы – всегда процессы вынужденные.
Хотя чисто обратимые процессы в природе не наблюдаются, однако теоретическое изучение их имеет большое практическое значение. В этих процессах газ при расширении производит максимально возможную работу, а при сжатии, когда газ возвращается в первоначальное состояние, затрачивается минимальная работа (см. п. 2.4). Как мы увидим в дальнейшем, КПД тепловых машин достигает максимального значения в обратимых процессах. Кроме того, для теоретического описания обратимых процессов, очевидно, требуется столько параметров, сколько их нужно для описания равновесного состояния. Для чистых веществ, не находящихся под воздействием силовых полей, таких параметров, как отмечалось ранее, два. Это существенно упрощает исследование термодинамических процессов.
Дата добавления: 2015-04-18; просмотров: 523; Мы поможем в написании вашей работы!; Нарушение авторских прав |