
КАТЕГОРИИ:
АстрономияБиологияГеографияДругие языкиДругоеИнформатикаИсторияКультураЛитератураЛогикаМатематикаМедицинаМеханикаОбразованиеОхрана трудаПедагогикаПолитикаПравоПсихологияРиторикаСоциологияСпортСтроительствоТехнологияФизикаФилософияФинансыХимияЧерчениеЭкологияЭкономикаЭлектроника
Ионный обмен и его использование для очистки газов и воды от ионных загрязнений
3. Приведите примеры уравнений реакций ионного обмена на катионите и на анионите.
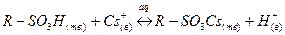
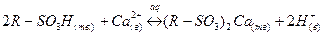
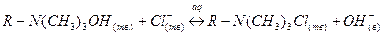
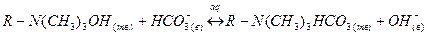
4. Приведите пример записи выражения для константы равновесия реакции ионного обмена на катионите в Н-форме.
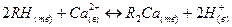 (1)
(1) 





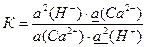 (2)
(2)
где а(Х) – активность ионов Х в водном растворе, моль/л раствора;
а(X) – активность ионов X в фазе ионита, моль/л ионита.
Согласно правилу Ле-Шателье из уравнения реакции (1), или из уравнения (2), в частности, следует, что при увеличении в растворе концентрации ионов Н+ ( при добавлении в раствор кислоты) равновесие реакции сдвигается вправо.
Следовательно:
1) при увеличении в растворе концентрации ионов водорода эффективность ионного обмена снижается;
2) отработанный катионит 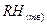 можно восстановить (регенерировать), пропуская через него раствор кислоты.
можно восстановить (регенерировать), пропуская через него раствор кислоты.
5. Сродство неорганических катионов к сульфогруппам сильнокислотных катионитов увеличивается с уменьшением радиусов гидратированных катионов и с увеличением их зарядов.
H+ < Na+ < K+ < Mg2+ < Zn2++ < Cu2+ < Ca2+ < Sr2+ < Pb2+ < Ba2+ < Al3+ < Ce4+
Пусть в очищаемой воде содержатся катионы кальция и бария. 1) Какой из катионов первым попадет в фильтрат при насыщении Н-катионита? 2) Какой - вторым? 3) Какой катион заполнит все функциональные группы катионита к моменту, когда фильтр полностью перестанет очищать воду? Ответы. 1) Ca2+. 2) Ba2+. 3) Ba2+.
6. Сродство анионов к сильноосновным анионитам увеличивается с увеличением их поляризуемости: OH- < HSiO3- < HCO3- < Cl- < CrO42- < SO42-. Пусть в воде содержатся хромат- и сульфат-ионы. Какой из анионов первым попадет в фильтрат при насыщении ОН-анионита? Какой анион заполнит все функциональные группы ионита к моменту, когда фильтр полностью перестанет очищать воду?
7. Составьте схему (рис.7.1) получения обессоленной воды с использованием ионообменных фильтров периодического действия. В какой форме должны находиться исходные катионит и анионит? Почему следует стремиться к многоступенчатой схеме фильтрации, а в пределе, к фильтрам смешанного действия?

Рис.7.1. При уменьшении количества катионита и анионита в каждом фильтре и при увеличении количества ступеней «катионит-анионит» рН фильтрата после катионитов практически не уменьшается, и, следовательно, не уменьшается эффективность ионного обмена.
8. Количественные характеристики ионитов:
1) Полная обменная емкость (ПОЕ) ионита, это количество молей эквивалентов ионогенных групп (активных центров) в 1 кг сухого ионита (или в 1 м3 ионита).
2) Статическая (равновесная) обменная емкость (СОЕ) ионита – количество молей эквивалентов ионогенных групп в расчете на 1 кг сухого ионита, обменявших свои ионы на ионы из раствора в условиях ионообменного равновесия между ионитом и раствором электролита с данной концентрацией ионов и данной температурой. Очевидно, что СОЕ ионита, определенная экспериментально для разных концентраций электролита в растворе при одной и той же температуре, может быть использована для построения графика изотермы ионообменной адсорбции.
3) Динамическая обменная емкость (ДОЕ) ионита – ее определяют экспериментально путем пропускания раствора с постоянной скоростью через колонку (ионообменный аппарат) со слоем ионита. В этом случае время контакта между ионитом и раствором недостаточно для установления ионообменного равновесия и, следовательно, ДОЕ < СОЕ.
9. Устройство ионитного фильтра переменного действия (рис.9.1).

Рис.9.1. Устройство ионитного фильтра переменного действия: 1-подвод исходной и обмывочной воды, 2 и 11 подвод и отвод регенерационного раствора, 3 и 7 –гидравлическая выгрузка и загрузка фильтрующего материала, 4 – цилиндрический корпус с днищами, 5 и 9 –верхний и нижний люки, 6 и 14 – верхнее и нижнее распределительные устройства, 8 – слой ионита, 10 – отвод отработанной воды, 12 и 15 – подвод и отвод взрыхляющей воды, 13 – поддерживающая цементная или битумная подушка.
10. Задача. Динамическая обменная емкость ДОЕ катионита КУ-2-8 равна 1000 молей экв./м3.
1) Какое количество воды, имеющей общую жесткость Жо = 3.5 ммоль экв./л, можно умягчить с помощью ионообменного фильтра с загрузкой 3.6 м3 катионита до момента появления проскока катионов?
2) Как изменится рН умягченной воды, если исходный катионит находится а) в Н-форме и б) в К-форме?
Ответы. 1) Пусть в воде содержится только соль Са(НСО3)2, следовательно
Сэ(Са2+) = 3.5 · 10-3 моль экв. Са2+/л = 3.5 моль экв. Са2+/м3
Составим и решим уравнение баланса:
Vводы · Сэ(Са2+) = Vкатионита· ДОЕ
Vводы = Vкатионита · ДОЕ/ Сэ(Са2+) = (3.6 м3·1000 молей экв/м3)/(3.5 моль экв/м3) = 1030 м3
2а) В исходной воде наряду с катионами кальция (сильный электролит) содержатся гидрокарбонат-ионы (слабый электролит). При ионном обмене в воду выделяются ионы Н+, часть которых связывается гидрокарбонат – ионами. Другая часть подкисляет воду.
2б) При ионном обмене в воду выделяются катионы сильного основания К+. рН фильтрата не изменяется.
11. Задача. При каких рН можно удалить из воды катионы Fe3+ с помощью ионообменного фильтра при следующих условиях: температура 20оС, начальная концентрация С(Fe3+) = 10-4 г/л, произведение растворимости ПР(Fe(OH)3) = 6.3 ·10-38 (моль/л)4 , ионное произведение воды при 20оС Кw = 10 -14 ? Указанная в задаче концентрация железа типична для воды в бассейнах выдержки ТВЭЛов энергетических реакторов на АЭС.
Решение.
 [ОН- ] =
[ОН- ] =  3.3·10-11 моль/л, [H+]= 3·10-4 моль/л, рН = 3.5
3.3·10-11 моль/л, [H+]= 3·10-4 моль/л, рН = 3.5
13. Составьте схему получения обессоленной воды с использованием ионообменных
фильтров периодического действия. В какой форме должны находиться исходные катионит и ионит? Какие процессы протекают на катионите и анионите при обессоливании, например, раствора поваренной соли?
Дата добавления: 2015-04-21; просмотров: 257; Мы поможем в написании вашей работы!; Нарушение авторских прав |