
КАТЕГОРИИ:
АстрономияБиологияГеографияДругие языкиДругоеИнформатикаИсторияКультураЛитератураЛогикаМатематикаМедицинаМеханикаОбразованиеОхрана трудаПедагогикаПолитикаПравоПсихологияРиторикаСоциологияСпортСтроительствоТехнологияФизикаФилософияФинансыХимияЧерчениеЭкологияЭкономикаЭлектроника
Адсорбция в процессах очистки воды
14. Общие сведения
Процесс поглощения какого-либо вещества поверхностью другого называют адсорбцией. Адсорбция является одним из наиболее эффективных физико-химических методов очистки промышленных сточных вод от вредных органических примесей до норм ПДК. На практике адсорбция используется для очистки сточных вод от фенолов, пестицидов, ароматических нитросоединений, ПАВ, красителей и т.д. В качестве адсорбентов могут служить все мелкодисперсные пористые материалы, обладающие развитой удельной поверхностью: древесные опилки, зола, торф, глины, коксовая мелочь и т.д. Однако наиболее эффективными адсорбентами являются изготавливаемые по особой технологии активные угли разных марок (АГ-3, БАУ, АР-3, СКТ, КАЛ-йодный, КАЛ-молотый). Активные угли являются пористыми материалами, поры которых по своему размеру могут быть подразделены на четыре вида: макропоры размером от 1000 до 20 000 Å, переходные поры – от 40 до 1000 Å, супермикропоры – от 16 до 40 Å и микропоры – не более 16 Å. Эффективность активных углей обусловливается, главным образом, наличием в них супермикро- и микро- пор.
Характеристиками активных углей являются объем микропор, см3/г; насыпная плотность, кг/м3; механическая прочность (устойчивость к истиранию), %; диаметр зерен, мм; изотерма адсорбции данного вещества, цена и т.д.
Справка: 1 Å = 10-10 м = 10-4 мкм. Размер молекул воды 3.1 Å.
Теоретические основы процесса адсорбции. Адсорбция – самопроизвольно протекающий экзотермический процесс, складывающийся из трех стадий:
1) перенос вещества из сточной воды к поверхности зерен адсорбента путем конвекции и диффузии – внешняя диффузионная область,
2) процесс адсорбции на внешней поверхности зерен,
3) перенос вещества внутрь зерен по порам – внутридиффузионная область.
Как правило, лимитирующими (ограничивающими скорость процесса адсорбции) стадиями являются первая или третья, хотя в некоторых случаях процесс может лимитироваться одновременно этими двумя стадиями.
В зависимости от характера взаимодействия адсорбата и адсорбента различают физическую адсорбцию и хемосорбцию. Одной из характеристик адсорбента является изотерма адсорбции, определяющая зависимость удельной адсорбции адсорбента а(Х) от концентрации С(Х) адсорбата Х в условиях равновесия при Т = const: a(X)= f(С(Х)|Т). При адсорбционной очистке сточных вод является важной также кинетика процесса, т.е. скорость адсорбции, от которой производительность адсорберов.
Процесс адсорбционной очистки сточных вод проводят или при интенсивном перемешивании зерен адсорбента с водой, или при фильтровании сточной воды через неподвижный слой зерен адсорбента. Процесс проводят или периодически, или непрерывно в одну или в несколько ступеней. На практике наиболее широкое применение нашла периодическая одноступенчатая адсорбция. Более эффективно и при меньшем расходе адсорбента процесс протекает при использовании многоступенчатой адсорбции.
Расход адсорбента при периодическом одноступенчатом процессе определяется уравнением материального баланса
 , (1)
, (1)
Для многоступенчатой адсорбционной установки периодического действия с последовательным введением свежего адсорбента в воду на каждой ступени расчет проводят по формулам:
 , (2)
, (2)
 ,(3)
,(3)
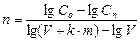 , (4)
, (4)
где m – масса адсорбента, вводимого в воду на каждой из ступеней; V – объем сточной воды в смесителе n-ой ступени; С0 и Сn – концентрации адсорбируемого вещества в сточной воде перед очисткой и после очистки в n-ой ступени; а – статическая удельная адсорбция; k – коэффициент распределения, определенный из изотермы адсорбции, k = а/С; n – число ступеней (или номер ступени).
При выводе формул (1) – (4) предполагается, что
- на каждой ступени адсорбции достигается равновесие;
- изотерма адсорбции линейна (a = k× C).
Последнее предположение выполняется для приближенно линейного начального участка любой изотермы.
При расчете по формуле (2) определяется концентрация вредного вещества в воде после n-ой ступени. Задаются масса адсорбента m, объем V сточной воды в емкости каждой ступени и число ступеней n, а также С0 и k.
При расчете по формуле (3) определяется масса m адсорбента, которую нужно вводить в смеситель каждой из n ступеней. Задаются концентрация вредного вещества Cn после последней n-ой ступени, объем сточной воды V смесителя каждой ступени, число n ступеней, а также С0 и k.
При расчете по формуле (4) определяется число ступеней n. Задаются концентрация адсорбата Сn в очищенной воде после последней n-ой ступени очистки, доза адсорбента m, вводимого в смеситель каждой ступени установки, а также С0 и k.
Формулы (2), (3) и (4) обращаются в формулу (1) при n = 1.
Для исследования динамики адсорбции используются «выходные кинетические кривые» (рис.14.1), которые апроксимируются экспонентой вида:
 , (5)
, (5)
где С(t) – концентрация загрязняющего вещества в растворе к моменту времени t при контакте раствора с адсорбентом; С* – концентрация загрязняющего вещества в растворе, равновесная с загрязняющим веществом в фазе адсорбента при t ® ¥; a – кинетический коэффициент, 1/с:
 , (6)
, (6)
Каждой концентрации адсорбата в растворе соответствует при равновесии определенная концентрация адсорбата в фазе адсорбента:
 . (7)
. (7)
При t → ∞ в системе устанавливается равновесие:
 , (8)
, (8)
Для приближенного определения числа ступеней в многоступенчатой адсорбционной установке периодического действия можно использовать графический метод (рис.14.2). Он заключается в построении в координатах (а, С) линии равновесия и рабочих линий для каждой ступени. Линией равновесия является изотерма адсорбции. Рабочие линии строятся по уравнению (7) и показывают зависимость между параметрами а и С на каждой ступени.
На рис.14.3 показана схема адсорбционной установки непрерывного действия. Схема установки периодического действия такая же, но тогда при расчетах величина скорости подачи угля 
 в смеситель заменятся на m, а объемный расходсточной жидкости L – наобъем смесителя V.
в смеситель заменятся на m, а объемный расходсточной жидкости L – наобъем смесителя V.
 |
 |
Рис.14.1. Выходная кинетическая кривая. Зависимость концентрации адсорбата в сточной воде от времени после введения в нее зерен свежего адсорбента.
Рис.14.2. Линия равновесия – изотерма адсорбции (экспериментальные данные по зависимости а* от С*) и рабочая линия процесса (график уравнения (7)).
 Рис.14.3. Схема многоступенчатой адсорбционной установки непрерывного действия с последовательным введением свежего адсорбента в воду на каждой ступени.
Рис.14.3. Схема многоступенчатой адсорбционной установки непрерывного действия с последовательным введением свежего адсорбента в воду на каждой ступени.
Дата добавления: 2015-04-21; просмотров: 630; Мы поможем в написании вашей работы!; Нарушение авторских прав |