
КАТЕГОРИИ:
АстрономияБиологияГеографияДругие языкиДругоеИнформатикаИсторияКультураЛитератураЛогикаМатематикаМедицинаМеханикаОбразованиеОхрана трудаПедагогикаПолитикаПравоПсихологияРиторикаСоциологияСпортСтроительствоТехнологияФизикаФилософияФинансыХимияЧерчениеЭкологияЭкономикаЭлектроника
Билет №13
1. Реакции элиминирования (дегидрогалогенирование, дегидратация). Повышенная СН-кислотность как причина реакций элиминирования, сопровождающих нуклеофильное замещение у sp3-гибридизированного атома углерода.
Наличие слабого СН – кислотного цента в монофункциональных производных углеводородов типа  , (где Х-галоген, ОН и т.д) предопределяет возможность его атаки основанием. Поскольку каждый нуклеофил в то же время является основанием в субстратах, содержащих β-водороные атомы, с реакцией нуклеофильного замещения конкурирует реакция отщепления (элиминирования).
, (где Х-галоген, ОН и т.д) предопределяет возможность его атаки основанием. Поскольку каждый нуклеофил в то же время является основанием в субстратах, содержащих β-водороные атомы, с реакцией нуклеофильного замещения конкурирует реакция отщепления (элиминирования).

Дегидрогалогенирование алкилгалогенидов проводят по действием сильных оснований – концентрированного раствора гидроксида щелочного металла в спирте или алкоксида щелочного метала. Дегидратация спиртов проводится при нагревании их в сильнокислой среде, например в присутствии концентрированных серной или фосфорных кислот.

Элиминирование легче проходит от третичных алкил галогенидов и спиртов. В случае вторичных и особенно первичных производных реакция протекает в значительно более жестких условиях.
С бимолекулярным нуклеофильным замещением часто конкурирует реакция элиминирования Е2. Этой реакции отщепления благоприятствует повышенная температура и использование нуклеофилов, являющихся сильными основаниями. Такие нуклеофилы способны атаковать не только электронодефицитный атом углерода субстрата, связанный с электроотрицательным гетероатомом, но и атом водорода, находящийся у соседнего углеродного атома, на котором за счет –I-эффекта гетероатома возникает частичный полжительный заряд HàCδ+δ+àCδ+àXδ-. Примером Е2 процесса служит образование этилена из этилбромида при действии на него концентрированной щелочи или спиртового раствоа алкоксида щелочного металла при нагревании.
Реакция элиминирования E2 становится преобладающей при взаимодействии вторичных, а темболее третичных алкилгалогенидов с нуклеофилами – сильными основаниями. Элиминроване Е2 может сопровождать протекающее через ониевые интермедиаты нуклеофильное замещение в спиратх, тиолах, аминах и их производных. В частности, один из общих методов получения алкенов основан на ращеплении при нагревании четвертичных аммониевых оснований (гофмановский распад).
Многим процессам SN1-замещения обычно соспутсвуют реакции элиминирования Е1. Это обусловлено возможностью стабилизации врзникающего промежуточного карбокатиона иным путем – элиминированием протона от соседнего атома С. Процессы SN1 и E1 имеют общую стадию образования карбкатиона. По механизму Е1 протекает отщепление воды от третичных спиртов в сильнокислой среде. В реакциях отщепления галогеноводорода от алкил галогенида или воды от спирта наблюдается преимущественное отщепление протона от атома С, содержащего минимально число атомов Н, т.е. наименее гидрогенизированного атома С.
2. Нуклеиновые кислоты. Пиримидиновые и пуриновые основания. Лактим-лактамная таутомерия. Реакции дезаминирования. Водородные связи в комплементарных парах нуклеиновых оснований (тимин-аденин, цитозин-гуанин).
Нуклеиновые кислоты представляют собой высокомолекулярные соединения, молекулярная масса которых колеблется от 25 тыс. до 1 млн и более. Полимерные цепи нуклеиновых кислот построены из мономерных единиц – нуклеотидов, в связи с чем нуклеиновые кислоты называют полинуклеотидами. Обычно «неделимое» мономерное звено (например, аминокислотный остаток в белках) у нуклеотидов представляет собой трехкомпонентное образование, включающее гетероциклическое основание, углеводный остаток и фосфатную группу.

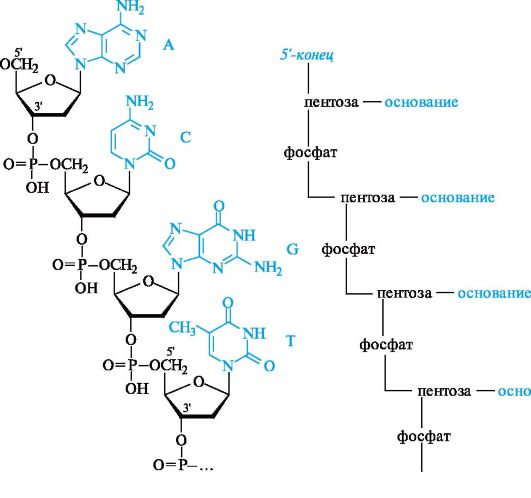
В полинуклеотидных цепях нуклеотидные звенья связаны через фосфатную группу. Фосфатная группа образует две сложноэфирные связи: с С-3' предыдущего и с С-5' последующего нуклеотидных звеньев. Каркас цепи состоит из чередующихся пентозных и фосфатных остатков, а гетероциклические основания являются «боковыми» группами, присоединенными к пентозным остаткам. Нуклеотид со свободной 5'-ОН группой называют 5'-концевым, а нуклеотид со свободной З'-ОН группой – З'-концевым.
Принцип построения цепи РНК такой же, как и у ДНК, с двумя исключениями: пентозным остатком в РНК служит D-рибоза, а в наборе гетероциклических оснований используется не тимин, а урацил. Первичная структура нуклеиновых кислот определяется последовательностью нуклеотидных звеньев, связанных ковалентными связями в непрерывную цепь полинуклеотида.

Важной характеристикой нуклеиновых кислот служит нуклеотидный состав, т.е. набор и количественное отношение нуклеотидных компонентов. Нуклеотидный состав устанавливают, как правило, путем исследования продуктов гидролитического расщепления нуклеиновых кислот.
ДНК и РНК различаются поведением в условиях щелочного и кислотного гидролиза. ДНК устойчивы к гидролизу в щелочной среде. РНК легко гидролизуются в мягких условиях в щелочной среде до нуклеотидов, которые, в свою очередь, способны в щелочной среде отщеплять остаток фосфорной кислоты с образованием нуклеозидов. Нуклеозиды в кислой среде гидролизуются до гетероциклических оснований и углеводов.

Для большинства нуклеотидов характерна лактим-лактамная таутомерия (рассмотрим на примере урацила):



Пуриновые и пиримидиновые основания претерпевают последующие изменения и превращаются в те или иные простейшие азотсодержащие продукты, которые либо выводятся из организма, либо откладываются в нем. Первая фаза распада пуриновых и пиримидиновых оснований заключается в дезаминировании под влиянием специфических аминогидролаз тех из них, которые имеют аминогруппу. В результате пуриновые основания – аденин превращается в гипоксантин, а гуанин – в ксантин.
Пиримидиновое основание, содержащее аминогруппу (цитозин) переходит в урацил.
Дезаминирование идет не только на уровне свободных пиримидиновых и пуриновых оснований, но и на уровне нуклеозидов и нуклеотидов, причем в последнем случае – с большей интенсивностью.
3. Приведите проекционные формулы стереизомеров этилового эфира β-гидроксимасляной кислоты. Имеются ли среди них диастереомеры?
СН3COОC2H5 СН3COОC2H5
 |  |

 HO Н Н OH
HO Н Н OH
CH3 CH3
L-форма D-форма
Среди стереоизомеров этой кислоты отсутствуют диастереомеры, так как в молекуле есть только один центр хиральности, и единственная пара стереоизомеров является энантиомерной парой.
4. Напишите уравнение реакции ацилирования бутанола ацетилфосфатом. Укажите механизм.
Эта реакция идёт по механизму электрофильного замещения.

5. Составьте схему реакции последовательного гидролиза крахмала, укажите условия.
Гидролиз крахмала ступенчатый. Протекает при нагревании в кислой среде. В пищеварительном тракте гидролизуется под действием ферментов.
Крахмал → растворимый крахмал (амилоза) → олигосахариды (декстрины) → дисахарид (мальтоза) → α-глюкоза.
(С6Н10О5)n + nН2О → nС6Н12О6
Дата добавления: 2015-02-10; просмотров: 1051; Мы поможем в написании вашей работы!; Нарушение авторских прав |