
КАТЕГОРИИ:
АстрономияБиологияГеографияДругие языкиДругоеИнформатикаИсторияКультураЛитератураЛогикаМатематикаМедицинаМеханикаОбразованиеОхрана трудаПедагогикаПолитикаПравоПсихологияРиторикаСоциологияСпортСтроительствоТехнологияФизикаФилософияФинансыХимияЧерчениеЭкологияЭкономикаЭлектроника
Общие свойства и способы получения металлов металлов
232. Свободные металлы в химических реакциях проявляют свойства:
А) Восстановителей
В) Окислителей
С) И окислителей, и восстановителей
D) Присоединения электронов
Е) Понижения степени своего окисления
233. Химические реакции с участием свободных металлов идут с:
А) Образованием положительно заряженных ионов металлов
В) Образованием отрицательно заряженных ионов металлов
С) Понижением степени окисления металлов
D) Восстановлением металлов
Е) Присоединением электронов к атомам металлов
234. В химических реакциях для свободных металлов характерно свойство:
А) Образовывать отрицательно заряженные ионы
В) Понижать свою степень окисления
С) Окисляться
D) Восстанавливаться
Е) Присоединять электроны
235. Лишнее в перечне общих физических свойств металлов:
А) Пластичность
В) Металлический блеск
С) Хрупкость
D) Электрическая проводимость
Е) Теплопроводность
236. Лишнее в перечне общих химических свойств металлов – это взаимодействие с:
А) Неметаллами
В) Водой
С) Кислотами
D) Растворами солей
Е) Основаниями
237. С водой в обычных условиях не реагирует:
А) Натрий
В) Литий
С) Кальций
D) Цинк
Е) Барий
238. В обычных условиях хрупким является металл:
А) Железо
В) Цинк
С) Медь
D) Серебро
Е) Никель
239. Тип кристаллической решетки железа (условия обычные):
А) Гексагональная
В) Кубическая гранецентрированная
С) Кубическая объемноцентрированная
D) Моноклинная
Е) Триклинная
240. Один из характерных для металлов типов кристалличесой решетки:
А) Моноклинная
В) Триклинная
С) Тетрагональная
D) Ромбическая
Е) Кубическая
241. Усиление металлических свойств элемента характеризуется:
А) Уменьшением радиуса атома
В) Увеличением электроотрицательности
С) Легкостью отдачи элетронов атомоми
D) Увеличением энергии ионизации
Е) Легкостью присоединения электронов атомами
242. Только электролизом расплава его соли можно получить металл:
A) Свинец;
B) Калий;
C) Медь;
D) Серебро;
E) Железо.
243. Из перечня элементов - Li, Na, Ag, Au, Ca, Ba - к щелочным металлам относятся:
A) Все металлы;
B) Li, Na;
C) Li, Na, Ag, Au;
D) Li, Na, Ca;
E) Ag, Au.
244. В ряду от Li к Fr :
A) Усиливаются металлические свойства;
B) Уменьшаются металлические свойства;
C) Уменьшается атомный радиус;
D) Усиливается связь валентных электронов с ядром;
E) Уменьшается активность по отношению к воде.
245. Самым распространенным металлом в земной коре является:
A) Fe;
B) Al;
C) Ti;
D) Na;
E) Ca
246. Среди металлов 2-ое место по распространенности в земной коре занимает:
А) Fe;
В) Al;
С) Ti;
D) Na;
Е) Ca
247. Цифры, обозначающие металлы (1. Кальций; 2. Алюминий; 3. Железо) в порядке убывания распространенности металлов в земной коре расположатся:
A) 1 2 3;
B) 2 3 1;
C) 3 2 1;
D) 1 3 2;
E) 2 1 3.
248. Из указанных металлов самый легкоплавкий:
A) Li;
B) Na;
C) K;
D) Rb;
E) Cs.
249 . Самый легкий металл:
A) Li;
B) Na;
C) K;
D) Rb;
E) Cs.
250. К металлам не относится последовательность элементов:
A) Ca, Zn, Cd;
B) Ti, Cr, Mn;
C) B, As, Te;
D) Na, Cu, Ni;
E) K, Ag, V.
251. В электротехнике для производства ламп накаливания используют вольфрамовую металлическую нить, поскольку этот металл обладает наибольшей:
A) Электропроводностью;
B) Теплопроводностью;
C) Тугоплавкостью;
D) Легкоплавкостью;
E) Пластичностью.
252. Из указанных металлов самый легкоплавкий:
A) Hg;
B) Na;
C) Cs;
D) Mg;
E) Pb.
253. Из перечисленных металлов способен вытеснять водород из воды при комнатной температуре:
A) Медь;
B) Железо;
C) Натрий;
D) Цинк;
E) Хром.
254. С концентрированной азотной кислотой не будет взаимодействовать:
A) Сu
B) Al
C) Zn;
D) Au;
E) Mg.
255. С концентрированной соляной кислотой не будет взаимодействовать:
A) Cu;
B) Al;
C) Zn;
D) Mg;
E) Cr.
256. В четырех пробирках находятся порошки оксида меди (II), оксида железа (III), серебра и железа. Для того, чтобы точно распознать эти вещества, используя только один реактив, в каждую пробирку необходимо прилить раствор:
A) Na2CO3;
B) HCl;
C) NaOH;
D) BaCl2;
E) Ca(OH)2.
257. Произойдет химическая реакция (электролит берется в виде водного раствора) между:
A) Pb и MgCl2;
B) Zn и MgCl2;
C) Zn и Pb(NO3)2;
D) Zn и NaCl;
E) Fe и K2SO4.
258. Расплавленные металлы при смешивании взаимодействует друг с другом, образуя химические соединения, как например, CuZn3; Na2Pb; Ca3Sb2. Такие соединения называют:
A) Твердыми растворами;
B) Интерметаллидами;
C) Соединениями внедрения:
D) Сплавами;
E) Бинарными соединениями
259. В самородном состоянии встречается металл:
A) Магний;
B) Алюминий;
C) Серебро;
D) Цинк;
E) Хром.
260. Металлы достаточно большой чистоты получают способом водородотермии. К этому способу относится получение металлов по реакции:
A) ZnO + C 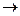 Zn + CO
Zn + CO
B) MoO3 + 3H2 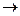 Mo + 3H2O
Mo + 3H2O
C) TiCI4 + 2Mg 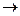 Ti + 2MgCI2
Ti + 2MgCI2
D) Fe2O3 + CO 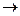 Fe + CO2
Fe + CO2
E) Cr2O3 + AI 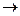 AI2O3 + Cr
AI2O3 + Cr
261. При электролизе раствора сульфата меди (II) на инертных электродах выделяются:
A) Cu, O2;
B) Cu, SO2;
C) Cu, H2;
D) Cu, SO3;
E) H2, SO2.
262. При полном восстановлении порошка оксида меди (II) массой 79,5 г водородом образовалась металлическая медь массой:
A) 32,75 г;
B) 63,5 г;
C) 79,5 г;
D) 16,37 г;
E) 46,25 г.
263. Алюминотермией получают металл:
A) Cu;
B) Cr;
C) K;
D) Na;
E) Fe .
264. Самый тугоплавкий металл:
A) Железо;
B) Ванадий;
C) Вольфрам;
D) Платина;
E) Молибден.
265. Для получения металлов из оксидов в промышленности в качестве восстановителя используют:
A) H2S;
B) HI;
C) C;
D) NH3;
E) Na.
266. Состав железной руды магнетит:
A) Fe2O3
B) Fe3O4
C) Fe2O3*H2O
D) FeS2
E) FeCO3
267.Для получения металлов высокой чистоты используют термическое разложение:
А) Карбоната металла
В) Нитрата металла
С) Оксида металла
D) Иодида металла
Е) Гидроксида металла
268. Лишнее в перечне методов получения металлов высокой чистоты:
А) Перегонка в вакууме
В) Зонная плавка
С) Карбонильный процесс
D) Иодидный способ
Е) Сульфидный способ
Дата добавления: 2015-02-10; просмотров: 329; Мы поможем в написании вашей работы!; Нарушение авторских прав |