
КАТЕГОРИИ:
АстрономияБиологияГеографияДругие языкиДругоеИнформатикаИсторияКультураЛитератураЛогикаМатематикаМедицинаМеханикаОбразованиеОхрана трудаПедагогикаПолитикаПравоПсихологияРиторикаСоциологияСпортСтроительствоТехнологияФизикаФилософияФинансыХимияЧерчениеЭкологияЭкономикаЭлектроника
НАПРАВЛЕНИЕ ПРОТЕКАНИЯ ХИМИЧЕСКИХ РЕАКЦИЙ
Самопроизвольному протеканию химических процессов в изобарно-изотермических условиях способствуют уменьшение энтальпии и увеличение энтропии системы. Первая тенденция характеризуется энтальпийным фактором и выражается через DН, а вторая - характеризуется энтропийным фактором и количественно выражается через T×DS .
Совместное влияние энтальпийного и энтропийного факторов учитывает изменение энергии Гиббса DG ( 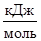 )
)
DG = DН - T×DS ,
где Т - абсолютная температура, К.
Самопроизвольно при Р,Т = const в прямом направлении могут протекать реакции, для которых DG < 0. Если DG реакции больше нуля, то такой процесс может протекать самопроизвольно только в обратном направлении. Реакции, имеющие DG = 0, находятся в состоянии равновесия, то есть для них равновероятно прямое и обратное течение процесса.
Расчет изменения энергии Гиббса реакции в стандартных условиях DG  можно осуществить двумя способами:
можно осуществить двумя способами:
1. По уравнению DG  = DН
= DН  - Т×DS
- Т×DS  . Расчет DН
. Расчет DН  и DS
и DS  подробно рассмотрен ранее.
подробно рассмотрен ранее.
2. По формуле, аналогичной при расчете DН  реакции через энтальпии образования участников реакции. В этом случае для реакции вида
реакции через энтальпии образования участников реакции. В этом случае для реакции вида
aA + bB = dD + fF
DG  = d DG
= d DG 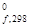 (D) + f DG
(D) + f DG 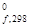 (F) - a DG
(F) - a DG 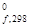 (A) - b DG
(A) - b DG 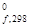 (B),
(B),
где DG 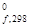 - стандартная энергия Гиббса образования вещества,
- стандартная энергия Гиббса образования вещества, 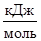 .
.
Стандартной энергией Гиббса образования вещества DG 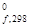 называют изменение энергии Гиббса реакции образования 1 моль соединения из простых веществ, находящихся в стандартных условиях. DG
называют изменение энергии Гиббса реакции образования 1 моль соединения из простых веществ, находящихся в стандартных условиях. DG 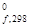 простых веществ равны нулю, а для сложных веществ - определены и содержаться в справочной литературе (см. приложение).
простых веществ равны нулю, а для сложных веществ - определены и содержаться в справочной литературе (см. приложение).
Направление химической реакции, прежде всего, определяется ее природой. Так, для экзотермических реакций (DН < 0), сопровождающихся возрастанием числа моль газообразных веществ (DS > 0), при любой температуре изменение энергии Гиббса будет отрицательным. То есть независимо от температуры такие реакции могут протекать только в прямом направлении. Наоборот, эндотермические реакции (DН > 0), сопровождающихся уменьшением числа моль газообразных веществ (DS < 0), независимо от значения температуры в системе могут протекать только в обратном направлении, так как в этом случае DG всегда положительное.
При сочетании DН > 0, DS > 0 или DН < 0, DS < 0 возможность протекания реакции в прямом направлении будет зависеть от температуры. При невысоких температурах 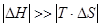 , поэтому энтальпийный фактор вносит больший вклад в значение DG. При высоких температурах, когда
, поэтому энтальпийный фактор вносит больший вклад в значение DG. При высоких температурах, когда  , знак DG будет определяться знаком энтропийного фактора.
, знак DG будет определяться знаком энтропийного фактора.
Пример 1. Вычислите DG  реакции двумя способами 2SO2 + О2 = 2SО3 .
реакции двумя способами 2SO2 + О2 = 2SО3 .
Р е ш е н и е
1. Вычислим DG  , используя справочные данные о DG
, используя справочные данные о DG 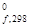 :
:
DG  = 2DG
= 2DG 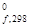 (SO3) - 2DG
(SO3) - 2DG 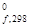 (SO2) - DG
(SO2) - DG 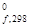 (O2) =
(O2) =
= 2(-371,17) - 2(-300,21) - 0 = -141,92 кДж.
2. Вычислим DG  , используя справочные данные об энтальпии образования и энтропии веществ:
, используя справочные данные об энтальпии образования и энтропии веществ:
DS  = 2S
= 2S  (SO3) - S
(SO3) - S  (O2) - 2S
(O2) - 2S  (SO2) = 2×256,7 - 205,0 -2×248,1 = -187,8
(SO2) = 2×256,7 - 205,0 -2×248,1 = -187,8  ;
;
DН  = 2DН
= 2DН 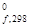 (SО3) - 2DН
(SО3) - 2DН 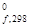 (SO2) = 2(-395,9) - 2(-296,9) = -198,0 кДж;
(SO2) = 2(-395,9) - 2(-296,9) = -198,0 кДж;
DG  = DН
= DН  - Т×DS
- Т×DS  = -198000 - 298×(-187,8) = -142036 Дж = -142,0 кДж.
= -198000 - 298×(-187,8) = -142036 Дж = -142,0 кДж.
Пример 2. Определите знак DG, не прибегая к расчетам для реакции
СаОт + СО2, г = СаСО3, т ; DН  = -178,1 кДж/моль.
= -178,1 кДж/моль.
Р е ш е н и е
Реакция экзотермическая, так как DН  < 0. Протекает с уменьшением числа моль газообразных веществ, следовательно, DS
< 0. Протекает с уменьшением числа моль газообразных веществ, следовательно, DS  < 0. Тогда при невысоких температурах
< 0. Тогда при невысоких температурах 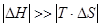 , а знак DG
, а знак DG  отрицательный (реакция протекает в прямом направлении). При высоких температурах
отрицательный (реакция протекает в прямом направлении). При высоких температурах  , следовательно, DG
, следовательно, DG  положительное.
положительное.
Пример 3. Определите температуру равновероятного протекания реакции в прямом и обратном направлении, если DН = -235 кДж, а DS = -95  .
.
Р е ш е н и е
При равновероятном протекании реакции в прямом и обратном направлении DG = 0. Тогда DН - T×DS = 0. Отсюда
T = 
 K.
K.
Дата добавления: 2015-04-16; просмотров: 422; Мы поможем в написании вашей работы!; Нарушение авторских прав |