
КАТЕГОРИИ:
АстрономияБиологияГеографияДругие языкиДругоеИнформатикаИсторияКультураЛитератураЛогикаМатематикаМедицинаМеханикаОбразованиеОхрана трудаПедагогикаПолитикаПравоПсихологияРиторикаСоциологияСпортСтроительствоТехнологияФизикаФилософияФинансыХимияЧерчениеЭкологияЭкономикаЭлектроника
ПРИЛОЖЕНИЕ. Стандартные термодинамические свойства веществ Вещество DН , кДж/моль S
Стандартные термодинамические свойства веществ
| Вещество | DН 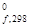 , кДж/моль , кДж/моль
| S  , , 
| DG 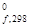 , кДж/моль , кДж/моль
|
| Alт | 42,55 | ||
| Сграфит | 5,74 | ||
| Feт | 27,15 | ||
| Н2, г | 130,52 | ||
| I2, ж | 137,00 | ||
| I2, г | 260,60 | ||
| N2, г | 191,50 | ||
| О2, г | 205,04 | ||
| Ркрасный | 22,80 | ||
| Рбелый | 41,09 | ||
| Pbт | 64,81 | ||
| Sромб | 31,92 | ||
| Al2O3, т | -1675,69 | 50,92 | -1582,27 |
| СОг | -110,53 | 197,55 | -137,15 |
| СО2, г | -393,51 | 213,66 | -394,37 |
| СН4, г | -74,85 | 186,27 | -50,85 |
| С2Н2, г | 226,75 | 200,82 | 209,21 |
| С2Н4, г | 52,30 | 219,45 | 68,14 |
| Cr2O3, т | -1140,56 | 81,17 | -1058,97 |
| CuOт | -162,00 | 42,63 | -134,26 |
| FeSт | -100,42 | 60,29 | -100,78 |
| FeOт | -264,85 | 60,75 | -244,30 |
| Fe2O3, т | -822,16 | 87,45 | -740,34 |
| Fe3O4, т | -1117,13 | 146,19 | -1014,17 |
| НСlг | -92,31 | 186,79 | -95,30 |
| Н2Ож | -285,83 | 69,95 | -237,23 |
| Н2Ог | -241,81 | 188,72 | -228,61 |
| Н2Sг | -20,60 | 205,70 | -33,50 |
| H2SO4, ж | -813,99 | 156,90 | -690,14 |
| KCl | -436,68 | 82,55 | -408,93 |
| KСlO3 | -391,20 | 142,97 | -289,80 |
| KNO3 | -492,46 | 132,88 | -392,75 |
| NH3, г | -45,94 | 192,66 | -16,48 |
| NH4Cl | -314,22 | 95,81 | -203,22 |
| NH4NO3 | -365,43 | 151,04 | -183,93 |
| NOг | 91,26 | 210,64 | 87,58 |
| NO2, г | 34,19 | 240,06 | 52,29 |
| N2Oг | 82,01 | 219,83 | 104,12 |
| NiOт | -239,74 | 37,99 | -211,60 |
| PbOт | -217,61 | 68,70 | -188,20 |
| SO2, г | -296,90 | 248,07 | -300,21 |
| SO3, г | -395,85 | 256,69 | -371,17 |
| ZnOт | -348,11 | 43,51 | -318,10 |
| ZnSт | -205,18 | 57,66 | -200,44 |
Литература
1. Угай Я.А. Общая и неорганическая химия. М.: Высш. шк., 1997.
2. Ахметов Н.С. Общая и неорганическая химия. М.: Высш. шк., 1998.
3. Коровин Н.В. Общая химия. М.: Высш. шк., 1998.
4. Гольбрайх З.Е., Маслов Е.И. Сборник задач и упражнений по химии. М.: Высш. шк., 1997.
5. Лидин Р.А., Молочко В.А., Андреева Л.Л. Задачи по неорганической химии. М.: Высш. шк., 1990.
6. Романцева Л.М., Лещинская З.Л., Суханова В.А. Сборник задач и упражнений по общей химии. М.: Высш. шк., 1991.
7. Коршунов Б.Г., Стефанюк С.Л. и др. Задачник по общей химии для металлургов. М.: Высш. шк., 1977.
8. Зайцев О.С. Познавательные задачи по общей химии. М.: Изд-во Моск. ун-та, 1982.
9. Ахметов Н.С., Азизова М.К., Бадыгина Л.И. Лабораторные и семинарские занятия по общей и неорганической химии. М.: Высш. шк., 1999.
10. Рабинович В.А., Хавин З.Я. Краткий химический справочник. СПб.: Химия, 1994.
11. Краткий справочник физико-химических величин / Под ред. А.А. Равделя и А.М. Пономаревой. - Л.: Химия, 1983.
Содержание
Первый закон термодинамики ................................................................. 3
Основы термохимии ................................................................................. 9
Энтропия. Второй закон термодинамики ................................................ 17
Направление протекания химических реакций ....................................... 22
Приложение .............................................................................................. 27
Литература ................................................................................................ 28
Дата добавления: 2015-04-16; просмотров: 249; Мы поможем в написании вашей работы!; Нарушение авторских прав |