
КАТЕГОРИИ:
АстрономияБиологияГеографияДругие языкиДругоеИнформатикаИсторияКультураЛитератураЛогикаМатематикаМедицинаМеханикаОбразованиеОхрана трудаПедагогикаПолитикаПравоПсихологияРиторикаСоциологияСпортСтроительствоТехнологияФизикаФилософияФинансыХимияЧерчениеЭкологияЭкономикаЭлектроника
Контрольная работа 1. Химическая термодинамика
Химическая термодинамика. Химическая кинетика и равновесие
Вариант 16
1. Что такое энтропия? Сформулируйте второй закон термодинамики для изолированных систем.
2. Исходя из теплового эффекта реакции:
3СаО (кр) + Р2О5 (кр) ® Са3(РО4)2 (кр); ΔrН˚298 = -739 кДж,
определите ΔfН˚298 ортофосфата кальция.
3. Рассчитайте ΔrG˚298 следующей реакции: Pb (кр) + CuO (кр) ® PbO (кр) + Cu (кр). При расчёте используйте значения ΔfH˚298 и S˚298 веществ – участников реакции. Укажите, будет ли данная реакция идти самопроизвольно?
4. Не проводя вычислений, установите знак ΔrS˚ следующих процессов:
2NH3 (г) ® N2 (г) + 3Н2 (г);
2NO (г) + О2 (г) ® 2NO2 (г);
2СН3ОН (г) + 3О2 (г) ® 4Н2О (г) + 2СО2 (г);
2НCl (г) ® Н2 (г) + Сl2 (г).
5. Каково значение энергии активации реакции, скорость которой при 300 К в 10 раз больше, чем при 280 К.
6. Найдите константу равновесия реакции: N2O4 « 2NO2, если начальная концентрация N2O4 составляла 0,08 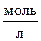 , а к моменту наступления равновесия диссоциировало 50% N2O4.
, а к моменту наступления равновесия диссоциировало 50% N2O4.
Контрольная работа 1
Химическая термодинамика. Химическая кинетика и равновесие
Вариант 17
1. Исходя из уравнения реакции:
СН3ОН (ж) +  О2 (г) ® СО2 (г) + Н2О (ж); ΔrН˚298 = -2360 кДж,
О2 (г) ® СО2 (г) + Н2О (ж); ΔrН˚298 = -2360 кДж,
определите стандартную теплоту образования метилового спирта.
2. Рассчитайте ΔrG˚298 следующей реакции:
8Al (кр) + 3Fe3O4 (кр) ® 9Fe (кр) + 4Al2O3 (кр)
7. При расчёте используйте значения ΔfH˚298 и S˚298 веществ – участников реакции. Укажите, будет ли данная реакция идти самопроизвольно?
3. От каких факторов зависят скорость химической реакции и константа скорости химической реакции? Сформулируйте закон действующих масс.
4. При 150°С некоторая реакция заканчивается за 16 мин. Принимая температурный коэффициент скорости реакции равным 2,5, рассчитайте, через какое время закончится эта реакция, если проводить её при 200°С.
5. Чему равна энергия активации реакции, если при повышении температуры от 290 до 300 К скорость её увеличится в 2 раза?
6. В замкнутом сосуде протекает реакция АВ (г) « А (г) + В (г). Константа равновесия реакции равна 0,04, а равновесная концентрация вещества В составляет 0,02 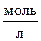 . Найдите начальную концентрацию вещества АВ. Сколько процентов вещества АВ разложилось?
. Найдите начальную концентрацию вещества АВ. Сколько процентов вещества АВ разложилось?
Дата добавления: 2015-04-16; просмотров: 286; Мы поможем в написании вашей работы!; Нарушение авторских прав |