
КАТЕГОРИИ:
АстрономияБиологияГеографияДругие языкиДругоеИнформатикаИсторияКультураЛитератураЛогикаМатематикаМедицинаМеханикаОбразованиеОхрана трудаПедагогикаПолитикаПравоПсихологияРиторикаСоциологияСпортСтроительствоТехнологияФизикаФилософияФинансыХимияЧерчениеЭкологияЭкономикаЭлектроника
Контрольная работа 1. Химическая термодинамика
Химическая термодинамика. Химическая кинетика и равновесие
Вариант 6
1. Вычислите изменение энтропии для реакций, протекающих по уравнениям:
2SO2 (г) + О2 (г) ® 2SO3 (г);
Ca(OH)2 (кр) ® CaO (кр) + Н2О (г);
Н2 (г) + Cl2 (г) ® 2HCl (г).
Почему в этих реакциях ΔrS˚298 имеет значения >0, <0, »0?
2. В каком направлении будет протекать реакция получения аммиака:
NH4Cl (кр) + NaOH (кр) ® NaCl (кр) + Н2О (г) + NH3 (г),
если реагирующие вещества взяты в стандартных условиях?
3. Вычислите стандартную теплоту образования сахарозы С12Н22О11, если тепловой эффект реакции: С12Н22О11 (кр) + 12О2 (г) ® 12СО2 (г) + 11Н2О (ж) равен –5646,73 кДж.
4. Какие химические процессы называются обратимыми и необратимыми? Приведите примеры практически обратимых и совершенно необратимых процессов.
5. Вычислите во сколько раз возрастает скорость реакции при увеличении температуры на 40°С, если температурный коэффициент этой реакции равен 3.
6. Константа скорости гетерогенной реакции: FeO (кр) + СО (г) « Fe (кр) + СО2 (г) равна 0,5. Чему равны равновесные концентрации СО и СО2, если их начальные концентрации равны ( 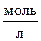 ): С (СО) = 0,05; С (СО2) = 0,01?
): С (СО) = 0,05; С (СО2) = 0,01?
Контрольная работа 1
Химическая термодинамика. Химическая кинетика и равновесие
Вариант 7
1. Сформулируйте закон Гесса и следствия из него. Приведите примеры использования закона Гесса.
2. При образовании 2,69×10-2 кг хлорида меди (II) из простых веществ выделяется 41,17 кДж теплоты. Найдите теплоту образования хлорида меди (II).
3. Исходя из величин ΔfG˚298 соединений, участвующих в реакции, определите, возможна ли реакция: Al2O3 (кр) + 2SO3 (г) ® Al2(SO4)3 (кр).
4. В чём состоит различие в выражениях констант равновесия гомогенных и гетерогенных процессов (приведите примеры)?
5. Во сколько раз изменится константа скорости реакции при увеличении температуры от 500 до 1000 К, если энергия активации равна 95,5 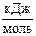 .
.
6. При синтезе фосгена имеет место равновесие реакции: Cl2 (г) + СО (г) « СОCl2 (г). Определите исходные концентрации хлора и оксида углерода, если равновесные концентрации равны ( 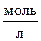 ): [Cl2] = 2,5; [CO] = 1,8; [COCl2] = 3,2. Рассчитайте константу равновесия.
): [Cl2] = 2,5; [CO] = 1,8; [COCl2] = 3,2. Рассчитайте константу равновесия.
Дата добавления: 2015-04-16; просмотров: 294; Мы поможем в написании вашей работы!; Нарушение авторских прав |