
КАТЕГОРИИ:
АстрономияБиологияГеографияДругие языкиДругоеИнформатикаИсторияКультураЛитератураЛогикаМатематикаМедицинаМеханикаОбразованиеОхрана трудаПедагогикаПолитикаПравоПсихологияРиторикаСоциологияСпортСтроительствоТехнологияФизикаФилософияФинансыХимияЧерчениеЭкологияЭкономикаЭлектроника
Контрольная работа 1. Химическая термодинамика
Химическая термодинамика. Химическая кинетика и равновесие
Вариант 4
1. Почему при низких температурах критерием, определяющим направление самопроизвольного процесса реакций, может служить знак DH , а при достаточно высоких температурах таким критерием является знак DS?
2. При растворении 16 г СаО в воде выделяется 19,3 кДж теплоты. Определите стандартную теплоту образования Са(ОН)2.
3. Вычислите изменение энтропии при стандартных условиях в следующей реакции:
СН4 (г) + 4Cl2 (г) ® ССl4 (ж) + 4HCl (г)
S˚298(СCl4 ж) = 216,19 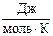 .
.
4. В каких единицах выражается концентрация газообразных и жидких веществ (укажите размерность)?
5. Константа скорости реакции А + 2В ® 3С равна 0,6 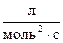 . Начальные концентрации А и В равны соответственно 2,0 и 2,5
. Начальные концентрации А и В равны соответственно 2,0 и 2,5 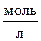 . В результате реакции концентрация вещества В оказалась равной 0,5
. В результате реакции концентрация вещества В оказалась равной 0,5 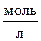 . Вычислите, какова концентрация вещества А и начальная скорость реакции.
. Вычислите, какова концентрация вещества А и начальная скорость реакции.
6. Рассчитайте константу равновесия К химической реакции при 1000 К, если стандартная энергия Гиббса реакции равна при этой температуре –19,1 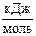 .
.
Дата добавления: 2015-04-16; просмотров: 239; Мы поможем в написании вашей работы!; Нарушение авторских прав |