
КАТЕГОРИИ:
АстрономияБиологияГеографияДругие языкиДругоеИнформатикаИсторияКультураЛитератураЛогикаМатематикаМедицинаМеханикаОбразованиеОхрана трудаПедагогикаПолитикаПравоПсихологияРиторикаСоциологияСпортСтроительствоТехнологияФизикаФилософияФинансыХимияЧерчениеЭкологияЭкономикаЭлектроника
Задача 4. Газ массой m занимает объем V1 и находится под давлением p1
Газ массой m занимает объем V1 и находится под давлением p1. При нагревании давление газа возросло до p2 при неизменном объеме, а затем газ расширился при постоянном давлении до объема V3. Найти изменение внутренней энергии  газа, совершенную им работу А и теплоту Q, переданную газу. Построить график процесса в осях (p;V), (p;T) и (V;T), выбрав масштаб самостоятельно.
газа, совершенную им работу А и теплоту Q, переданную газу. Построить график процесса в осях (p;V), (p;T) и (V;T), выбрав масштаб самостоятельно.
Таблица 4
| Вариант | газ | m, кг | V1, л | p1, МПа | p2, кПа | V3, м3 |
| водород | 1,5 | 0,12 | 18,0 | |||
| водород | 1,4 | 0,13 | 19,0 | |||
| углекислый газ | 3,0 | 0,11 | 1,95 | |||
| углекислый газ | 3,2 | 0,13 | 1,80 | |||
| углекислый газ | 3,4 | 0,125 | 1,90 | |||
| азот | 4,0 | 0,11 | 5,00 | |||
| азот | 4,1 | 0,115 | 4,60 | |||
| азот | 4,2 | 0,12 | 4,40 | |||
| кислород | 2,2 | 0,12 | 1,56 | |||
| кислород | 2,5 | 0,14 | 1,82 |
Пример 4.Кислород массой m = 2 кг занимает объем V1 = 1 м3 и находится под давлением р1 = 0,15 МПа. При нагревании газ расширился при постоянном давлении до объема V2 = 1,3 м3, а затем его давление возросло до р3 = 0,21 МПа при неизменном объеме. Найти изменение внутренней энергии  газа, совершенную им работу А и теплоту Q, переданную газу. Построить график процесса в осях (р;V).
газа, совершенную им работу А и теплоту Q, переданную газу. Построить график процесса в осях (р;V).
Дано: m = 2 кг; М = 0,032 кг/моль; V1 = 1 м3, V2 = V3 = 1,3 м3;
р1 = р2 = 0,15 МПа, р3 = 0,21 МПа.
Найти:  ,
,  ,
, 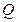 .
.
Решение. Изменение внутренней энергии газа выражается формулой
 .
.
В данном случае  .
.  , (1)
, (1)
где i – число степеней свободы молекул газа (для двухатомных молекул кислорода i = 5 ).
Температуры газа в каждом состоянии найдем, используя уравнение Менделеева – Клапейрона
 .
.
Отсюда  .
.
Подставим численные значения параметров каждого из трех состояний
Т1 = 289 К;
Т2 = 375 К;
Т3 = 526 К.
Подставляя в выражение (1) числовые значения находим
DU = 307,7 кДж.
Работа расширения газа при постоянном давлении выражается формулой A = p(V2 – V1). Используя уравнениеМенделеева – Клапейрона, получим  .
.
Работа газа при  равна нулю.
равна нулю.
 .
.
Таким образом, полная работа, совершаемая газом, равна
А = А12 = 44,7 кДж.
Согласно первому началу термодинамики теплота Q, переданная газу, равна сумме изменения внутренней энергии  и работы А:
и работы А:  , следовательно,
, следовательно,
Q = 307,7 кДж + 44,7 кДж = 352,4 кДж = 0,35 МДж.
График процесса в осях (p;V) приведен на рисунке.
 р, МПа
р, МПа


 0,21 3
0,21 3




 0,15 1 2
0,15 1 2
 |
0 1 1,3 V, м3
Дата добавления: 2015-02-10; просмотров: 500; Мы поможем в написании вашей работы!; Нарушение авторских прав |