
КАТЕГОРИИ:
АстрономияБиологияГеографияДругие языкиДругоеИнформатикаИсторияКультураЛитератураЛогикаМатематикаМедицинаМеханикаОбразованиеОхрана трудаПедагогикаПолитикаПравоПсихологияРиторикаСоциологияСпортСтроительствоТехнологияФизикаФилософияФинансыХимияЧерчениеЭкологияЭкономикаЭлектроника
Коррозия
Коррозия металлов – это разрушение металлов или сплавов под воздействием окружающих условий, в результате чего они теряют присущие им свойства.
Различают химическую и электрохимическую коррозию металлов. Химическая коррозия металлов вызывается окислительно–восстановительными реакциями, происходящими в результате взаимодействия металла с газами и неэлектролитами. Электрохимическая коррозия металлов возникает при контакте двух металлов под воздействием электролитов.
Электродные процессы:
- на аноде окисляется корродирующий металл;
- на катоде происходит восстановление атомов или ионов окружающей среды.
Пример 1
Цинковую и железную пластинки опустили в раствор сульфата меди. Составьте электронные и ионные уравнения реакций, происходящих на пластинках. Какие процессы будут проходить на пластинках, если наружные концы их соединить проводниках.
Решение:
а) Zn + CuSO4  ZnSO4 + Cu
ZnSO4 + Cu
(Цинковая пластина постепенно растворяется, на ней выделяется мет. медь)
Zn0 – 2e  Zn2+ (восстановитель) φ0 = –0,76 В
Zn2+ (восстановитель) φ0 = –0,76 В
Cu2+ + 2e  Cu0 (окислитель) φ0 = 0,34 В
Cu0 (окислитель) φ0 = 0,34 В
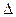 E = φ0 (окислителя) –φ0 (восстановителя)
E = φ0 (окислителя) –φ0 (восстановителя)
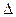 E = 0,34 – (–0,76) = 1,1 В
E = 0,34 – (–0,76) = 1,1 В
б) Fe + CuSO4 = FeSO4 + Cu
(железная пластина растворяется, на ней выделяется металлическая медь)
Fe0 *– 2e  Fe2+ (восстановитель) φ0 = –0,44 В
Fe2+ (восстановитель) φ0 = –0,44 В
Cu2+ + 2e  Cu0 (окислитель) φ0 = 0,34 В
Cu0 (окислитель) φ0 = 0,34 В
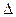 E = φ0 (окислителя) –φ0 (восстановителя)
E = φ0 (окислителя) –φ0 (восстановителя)
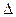 E = 0,34 В – (–0,44 В) = 0,78 В
E = 0,34 В – (–0,44 В) = 0,78 В
Если соединить наружные концы пластинок проводником, то получим гальванический элемент, где пластинки будут играть роль электродов. Согласно значению потенциалов система Zn2++ 2e  Zn по отношению к системе Fe2+ + 2e
Zn по отношению к системе Fe2+ + 2e  Fe является восстановителем, т.е. в растворе электроны будут переходить от Zn к Fe2+.
Fe является восстановителем, т.е. в растворе электроны будут переходить от Zn к Fe2+.
Zn + Fe2+ = Zn2+ + Fe и Zn – 2e = Zn2+ – анод
Fe2+ + 2e = Fe – катод
Пример 2
Составить схему процесса атмосферной коррозии оцинкованного железа.
Решение: Оцинкованное железо – это железо, покрытое цинком. Стандартные электродные потенциалы (таблица) железа равен –0,44В, цинка равен –0,76В. Т.к. потенциал цинка отрицательнее потенциала железа φ0(Zn/Zn2+) = –0,76 В;
φ0(Fe/Fe2+) = –0,44 В, то цинк является анодом в коррозионном процессе.
Схема реакций:
А(–):Zn – 2e–  Zn2+
Zn2+
К(+):(Fe)O2 + 4e–+2Н2О  4ОН–
4ОН–
Суммарная реакция с учетом электролитов:
2Zn + O2 + 2H2O  2Zn(OH)2
2Zn(OH)2
Задачи
161. Как происходит атмосферная коррозия лужёного и оцинкованного железа при нарушении целости покрытия? Составьте электронные уравнения анодного и катодного процессов.
162. Медь не вытесняет водород из разбавленных кислот. Почему? Однако, если к медной пластинке, опущенной в кислоту, прикоснуться цинковой, то начнется бурное выделение водорода. Дайте этому объяснение, составив электронные уравнения анодного и катодного процессов. Напишите уравнения протекающей химической реакции.
163. Хромированная деталь автомобиля состоит из железа, покрытого тонким слоем никеля, который, в свою очередь, покрыт слоем хрома. Расположите эти металлы в ряд по лёгкости окисления. Для чего нужен слой хромового покрытия? Какую роль играет покрытие?
164. Как происходит атмосферная коррозия луженой меди при нарушении цельности покрытия. Составьте электронные уравнения анодного и катодного процессов.
165. Если пластинку из чистого цинка опустить в разбавленную кислоту, то начинающееся выделение водорода вскоре почти прекращается. Однако при прикосновении к цинку медной палочкой, на последней начинается бурное выделение водорода. Дайте этому объяснение, составив электронные уравнения анодного и катодного процессов. Напишите уравнение протекающей химической реакции.
166. В чем заключается сущность протекторной защиты металлов от коррозии? Приведите пример протекторной защиты никеля в электролите, содержащем растворенный кислород. Составьте электронные уравнения анодного и катодного процессов.
167. Если на стальной предмет нанести каплю воды, то коррозии подвергается средняя, а не внешняя часть смоченного металла. После высыхания капли в ее центре появляется пятно ржавчины. Чем это можно объяснить? Какой участок металла, находящийся под каплей воды, является анодным и какой катодным? Составьте электронные уравнения соответствующих процессов.
168. Если гвоздь вбить во влажное дерево, то ржавчиной покрывается та его часть, которая находится внутри дерева. Чем это можно объяснить? Анодом или катодом является эта часть гвоздя? Составьте электронные уравнения соответствующих процессов.
169. В раствор соляной кислоты поместим цинковую пластинку и цинковую пластинку, частично покрытую медью. В каком случае процесс коррозии цинка происходит интенсивнее? Ответ мотивируйте, составив электронные уравнения соответствующих процессов.
170. Почему химически чистое железо является более стойким против коррозии, чем техническое железо? Составьте электронные уравнения анодного и катодного процессов, происходящих при коррозии технического железа во влажном воздухе и в сильнокислой среде.
171. Какое покрытие металла называется анодным и какое катодным? Назовите несколько металлов, которые могут служить для анодного и катодного покрытия железа. Составьте электронные уравнения анодного и катодного процессов, происходящих при коррозии железа, покрытого медью во влажном воздухе и в сильнокислой среде.
172. Железное изделие покрыли кадмием. Какое это покрытие – анодное или катодное? Почему? Составьте электронные уравнения анодного и катодного процессов коррозии этого изделия при нарушении цельности покрытия во влажном воздухе и в соляной кислоте. Какие продукты коррозии образуются в первом и во втором случаях?
173. Железное изделие покрыли свинцом. Какое это покрытие - анодное или катодное? Почему? Составьте электронные уравнения анодного и катодного процессов коррозии этого изделия во влажном воздухе и в соляной кислоте. Какие продукты коррозии образуются в первом и во втором случаях?
174. Две железные пластинки, частично покрытые одна оловом, другая медью, находятся во влажном воздухе. На какой из этих пластинок быстрее обрадуется ржавчина? Почему? Составьте электронные уравнения анодного и катодного процессов коррозии этих пластинок. Каков состав продуктов коррозии?
175. В обычных условиях во влажном воздухе оцинкованное железо при нарушении цельности покрытия не ржавеет, тогда как при температуре выше 70°С оно покрывается ржавчиной. Чем это можно объяснить? Составьте электронные уравнения анодного и катодного процессов коррозии оцинкованного железа в первом и во втором случаях.
176. Как влияет рН среды на скорость атмосферной коррозии железа и цинка? Почему? Составьте электронные уравнения анодного и катодного процессов атмосферной коррозии этих металлов.
177. Если пластинку из чистого железа опустить в соляную кислоту, то выделение на ней водорода идет медленно и со временем почти прекращается. Однако, если цинковой палочкой прикоснуться к железной пластинке, то на последней начинается бурное выделение водорода. Почему? Какой металл при этом растворяется? Составьте электронные уравнения анодного и катодного процессов.
178. Цинковую и железную пластинки опустили в раствор сульфата меди. Составьте электронные и ионные уравнения реакций, происходящих на каждой из этих пластинок. Какие процессы будут происходить на пластинках, если наружные концы их соединить проводником?
179. В раствор электролита, содержащего растворенный кислород, опустили цинковую пластинку и цинковую пластинку, частично покрытую медью. В каком случае процесс коррозии происходит интенсивнее? Составьте электронные уравнения анодного и катодного процессов.
180. Железные бочки применяют для транспортировки концентрированной серной кислоты, но после освобождения от кислоты бочки часто совершенно разрушаются вследствие коррозии. Чем это можно объяснить? Что является анодом и что катодом? Составьте электронные уравнения соответствующих процессов.
181. Как протекает атмосферная коррозия железа, покрытого слоем никеля, если цельность никеля нарушена? Составьте электронные уравнения анодного и катодного процессов. Каков состав продуктов коррозии?
182. В чем сущность электрохимической теории коррозии металлов? Почему технический цинк взаимодействует с кислотой более интенсивно, чем химически чистый цинк?
183. Почему технические металлы подвергаются коррозии в большей степени, чем химически чистые металлы? Приведите примеры электрохимической защиты металлов от коррозии.
184. Приведите характеристику способов защиты металлов от коррозии, анодным покрытием; катодным покрытием; методом протекторов.
185. Железная пластинка, склепанная с медной, погружена в разбавленную H2SО4. На какой пластинке будет выделяться водород? Происходящие процессы изобразите электронными уравнениями.
Дата добавления: 2015-04-16; просмотров: 1371; Мы поможем в написании вашей работы!; Нарушение авторских прав |